[Ag(NH)2]CI + 2HNO3↓ → AgCI ↓ + 2NH4NO3
У відповідності з ФС, вміст хлоридів не повинен перевищувати 0,02%.
Кількісно йод визначають титруванням розчину лікарської речовини (в присутності калію йодиду для кращого розчинення йоду) стандартним розчином натрію тіосульфату:
I2 + 2Na2S2O3 → 2NaI + Na2S2O3
Як індикатор використовують крохмаль, тому титрування ведуть до знебарвлення розчину.
Спиртові розчини йоду. 10% спиртовий розчин йоду готують розчиненням йоду кристалічного в 95% спирті. Препарат нестійкий, тому що йод реагує зі спиртом:
C2H5OH + I2 → CH3─CHO + 2HI
Ступінь зміни препарату визначають шляхом встановлення в ньому вмісту йодоводневої кислоти титруванням її стандартним розчином натрію гідроксиду після знебарвлення йоду натрію тіосульфату.
Готують препарат на короткий час – до 1 місяця. 5% і 2% розчини йоду більш стійкі при зберіганні, тому що їх готують на розведеному (до 46%) спирті з додаванням калію йодиду. При кількісному аналізі таких препаратів визначають вміст як йоду так і калію йодиду. Спочатку препарат титрують 0,1 М розчином натрію тіосульфату для визначення йоду. Далі суму йодидів відтитровують стандартним розчином аргентуму нітрату (індикатор – натрію еозинат):
NaI + AgNO 3 → AgI↓ + NaNO3
KI + AgNO3 → AgI↓ + KNO3
Різниця між об’ємами розчину аргентуму нітрату і натрію тіосульфату включають в розрахунок вмісту калію йодиду:
(VAgNO3 ∙ K ─ VNa2S2O3 ∙ R) ∙ T ∙100
X(%) = ───────────────────────
a
де Х - вміст калію йодиду,%
V - об’єми стандартних розчинів аргентуму нітрату і натрію тіосульфату, які пішли на титрування, мл;
К - поправочні коефіцієнти титрантів;
Т – титр за визначуваною речовиною (титриметричний фактор перерахунку);
а – об’єм розчину, взятого для аналізу.
Кислота хлороводнева. Лікарськими засобами є розчини хлороводню: кислота хлороводнева (вміст хлороводню 24,8-25,2%) і кислота хлороводнева розведена (8,2-8,4%).
Обидва препарати – безбарвні рідини. Кислота хлороводнева – летка рідина, тому її зберігають в склянках з притертими пробками. Відносится до сильних кислот, тому кількісне визначення вмісту хлороводню можна провести методом алкаліметрії.
Хлорид – іон в препараті визначають реакцією з аргентуму нітратом або при взаємодії з окислювачами. Хлорид-іон проявляє слабкі відновні властивості і окислюється до молекулярного хлору при дії сильних окислювачів- таких, як калію перманганат, марганцю (IV)оксид, калію дихромат:
4НСІ + МпО2 → МпСІ2 + СІ2 + 2Н2О
Хлор, який виділяється, можна виявити реакцією з калію йодидом:
СІ2 + 2КІ → І2 + 2КСІ
За допомогою цієї ж реакції визначають недопустиму домішку хлору в кислоті хлороводневій.
Специфічну недопустиму домішку в препараті – сульфітну кислоту виявляють реакцією з молекулярним йодом. Обезбарвлення розчину йоду вказує на присутність домішки:
Н2SO3 + I2 → H2SO4 + 2HI
Фармакопейною методикою кількісного визначення кислоти хлороводневої є алкаліметрія.
Кислоту хлороводневу використовують в медицині у вигляді мікстури (разом з пепсином) при недостатній кислотності шлункового соку. Нерідко її призначають разом з препаратами феруму, тому що вона сприяє його засвоєнню.
Натрію і калію хлориди. Вони відносяться до сильних електролітів, водні розчини мають нейтральну реакцію. Хімічні властивості даних лікарських речовин зумовлені наявністю відповідних іонів. Так катіони натрію і калію забарвлюють полум”я відповідно в жовтий і фіолетовий колір.
Солі натрію утворюють жовтий кристалічний осад (нерозчинний в кислоті оцтовій) з цинку уранілацетатом:
Na++Zn2++[(UO2)3(CH3COO)8]2-+CH3COOH+6H2O→
→NaZn[(UO2)3(CH3COO)9]∙6H2О+ Н+
Гексагідроксостибіат-іон в нейтральному середовищі утворює з іонами натрію білий кристалічний осад натрію гексагідроксостибату:
Na+ + [ Sb(OH)6 ]‾ → Na[Sb(OH)6 ↓
Солі калію з розчином гексанітритокобальтату(ІІІ) натрію утворюють жовтий кристалічний осад гексанітритокобальтату (Ш) натрію і калію:
К+ + Na3[Co(NO2)6] → NaK2[Co(NO2)6]↓ + Na+
Осад не розчиняється в оцтовій кислоті, але розчиняється в мінеральних кислотах. В сильнокислому середовищі утворюється нестійка гексанітритокобальтова кислота Н3[Со(NO2)6], яка розкладається в момент утворення. В лужному середовищі утворюється бурий осад Со(ОН)3.
Іони амонію заважають реакції, вони дають з реактивом осад, а тому для видалення солей амонію препарат попередньо прокалюють.
З розчином кислоти винної солі калію утворюють осад калію гідротартрату білий, який не розчиняється в кислоті оцтовій, але розчиняється в мінеральних кислотах і лугах:
НО─ СН─ СООН НО─ СН─СООК
К+ + │ ─→ │ ↓ + Н+
НО─ СН─ СООН НО─ СН─СООН
Хлорид-іон в даних лікарських засобах визначають взаємодією з розчином аргентуму нітрату: СІ‾ + Ag+ → AgCI↓
Утворюється білий сирнистий осад. Реакцію проводять в середовищі кислоти нітратної, в якій не розчиняються галогеніди аргентуму.
Особливість аргентуму хлориду (на відміну від броміду і йодиду) заключається в його здатності легко розчинятись в розчинах аміаку, амонію карбонату і натрію тіосульфату:
AgCI + NH3 → [Ag(NH3)2] CI
AgCI + (NH4)2CO3 → [Ag(NH3)2]CI + CO2↑ + H2O
AgCI + 2Na2S 2 O3 → Na3[Ag(S2 O3 )2] + NaCI
Кількісне визначення натрію хлориду і калію хлориду проводять методом Мора. Титрування ведуть в нейтральному середовищі стандартним розчином аргентуму нітрату в присутності індикатора калію хромату. Аргентуму хлорид значно менш розчинний, ніж аргентуму хромат, тому хлорид іони осаджуються першими:
NaCI + AgNO3 → AgCI + NaNO3
Після повного осадження хлорид –іонів, випадає червоно-оранжевий осад аргентуму хромату:
2AgNO3 + K2CrO 4 → Ag2CrO4↓ + 2KNO3
Реакція середовища повинна бути нейтральною або слабко-лужною (рН 7,0-10,0). У кислому середовищі хромат –іон переходить в дихромат –аніон і чутливість індикатора різко знижується.
Якщо визначення хлоридів методом Мора неможливе (наприклад, при аналізі лікарських сумішей, які мають кислу реакцію середовища або якщо є речовини, які реагують, як і хлориди, з іонами аргентуму), застосовують метод зворотнього титрування Фольгарда. При цьому хлориди осаджують надлишком титрованого розчину аргентуму нітрату і відтитровують залишок аргентуму нітрату стандартним розчином амонію ціанату:
AgNO3 + NaCI → AgCI↓ + NaNO3
AgNO3(залишок) + NH4SCN → AgSCN↓ + NH4NO3
Як індикатор використовують розчини солей тривалентного феруму, наприклад, амонію феруму (Ш) сульфату (галуни ферумоамонійні – NH4Fe(SO4 )2∙ 12H2O), які з надлишковою краплиною амонію тіоціанату утворюють комплексні солі червоного кольору:
Fe3+ + nSCN‾ → [Fe(SCN)n]3 – n
Натрію і калію броміди -білі кристалічні порошки, добре розчинні у воді, реакція середовища водних розчинів нейтральна. Натрію бромід гігіроскопічний. Ступінь його зволоження регламентується шляхом визначення втрати маси при висушуванні.
Для ідентифікації застосовують реакції на катіони і аніони, тому що броміди натрію і калію (як і хлориди) є сильними електролітами.
Броміди з розчином аргентуму нітрату утворюють жовтуватий осад:
Ag+ + Br‾ → AgBr↓
Аргентуму бромід, на відміну від аргентуму хлориду, не розчиняється в розчині амонію карбонату і важко розчиняється в надлишку концентрованого розчину аміаку:
AgBr↓ + 2NH3 → [Ag(NH3)2]Br
Аргентуму бромід розчиняється(як хлориди і йодиди) в розчині натрію тіосульфату.
Броміди окиснюються до вільного галогена легше чим хлориди, тому їх ідентифікують за реакцією виділення брому в результаті окисно-відновної реакції з хлораміном в кислому середовищі. Бром, який виділяється в результаті реакції, вилучають хлороформом, в якому він розчиняється краще,
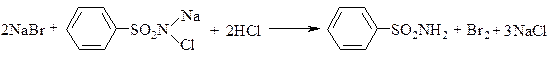 |
ніж у воді, забарвлюючи його в жовто-бурий колір:
Специфічними домішками в калій і натрій бромідах можуть бути іони йодидів, барію, кальцію, броматів. Йодиди визначають з допомогою слабкого окислювача, яким є феруму(Ш) хлорид, який не окиснює броміди:
2Fe3++2I‾→Fe2++I2
Йод, який виділився виявляють в присутності крохмалю за синім забарвленням.
Іони барію, кальцію і бромат-іон ідентифікують одним реактивом – концентрованою сульфатною кислотою. При додаванні реактиву (Н2SO4) до досліджуваного розчину у відповідності з вимогами ДФ, не повинно з’являтися помутніння або забарвлення (солі барію і кальцію утворюють нерозчинні сульфати, а бромати в присутності бромідів в кислому середовищі виділяють бром, який забарвлює розчин в жовтий колір):
BrO3‾ + 5Br‾ + 6H+ → 3Br2 + 3H2O
Кількісне визначення калію і натрію бромідів (як і калію і натрію хлоридів) за ДФ проводять методом прямого титрування (методом Мора).
Натрію хлорид є основною складовою частиною сольових і колоїдно-сольових розчинів, які використовуються як плазмозамінники. Натрію хлорид міститься в крові і тканинних рідинах організму. Концентрація його в крові 0,5 %. Основна роль натрію хлориду – забезпечувати сталість осмотичного тиску. При дефіциті натрію хлориду в організмі він вводиться внутрішньовенно або підшкірно у вигляді 0,9% розчину, який називається ізотонічним розчином. Введення його вирівнює і нормалізує осмотичний тиск крові. Крім фармакопейних препаратів, існують гіпертонічні розчини натрію хлориду:3%,5% і 10%. Їх застосовують зовнішньо для компресів при лікуванні гнійних ран. Завдяки осмотичному впливу ці розчини сприяють очищенню рани від гною.
Іон калію є основним внутрішньоклітинним іоном, в той час як натрій-іон – головним позаклітинним іоном. Взаємодія цих двох іонів відіграє важливу роль у підтриманні ізотонічності клітин.
Основним показником до застосування калію хлориду є порушення серцевого ритму, особливо в зв’язку з інтоксиікацією серцевими глікозидами, що зв’язано зі збідненням клітин міокарду на іони калію. Калію хлорид застосовується також у випадку гіпокаліємії (зниження концентрації іонів калію в крові), яка виникає при тривалому застосуванні діуретиків.
Броміди калію і натрію застосовують як заспокійливі засоби. Заспокійлива дія препаратів брому грунтується на їх здатності посилювати процеси гальмування в корі головного мозку. Броміди можуть відновлювати рівновагу між процесами збудження і гальмування, особливо при підвищеній збудливості нервової системи. Тому броміди використовуються при неврастенії, підвищеній подразливості.
Натрію і калію йодиди - безбарвні або білі кристалічні речовини; гігроскопічні,є енергійними відновниками. Вступають в реакцію з киснем повітря, внаслідок чого порошки даних лікарських засобів жовтіють при неправильному зберіганні.Світло, домішки важких металів, кисень повітря ініціюють процеси окиснення йодидів.Йодиди можуть містити специфічні домішки – іони барію, йодату, тіосульфату. ДФ регламентує вміст цих домішок.
Іони барію визначають за реакцією з кислотою сірчаною(протягом 15 хвилин розчин повинен залишатися прозорим).
Для визначення йодатів разом з H2SO4 додають крохмаль; при наявності домішки виникає синє забарвлення:
IO3‾ + 5I‾ → 3I2 + 3H2O
Поява синього забарвлення після додавання 1 краплини 0,1 М розчину йоду в присутності крохмалю вказує на відсутність тіосульфату.
Загальний спосіб кількісного визначення йодидів за ДФ – пряма аргентометрія з застосуванням адсорбційного індикатора натрію еозинату (метод Фаянса). Суть методу заключається в тому, що адсорбційний індикатор не змінює свого забарвлення (жовто-червоного) до настання точки еквівалентності. В точці еквівалентності індикатор адсорбується на осаді AgI, і колір його стає червоно-фіолетовим. До точки еквівалентності на осаді AgI адсорбувався невідтитрований йодид-іон. При цьому поверхня заряджається негативно, що перешкоджає адсорбції на ньому індикатора у вигляді аніону.
Після того, як йодид відтитрований повністю, на поверхні осаду адсорбуються іони аргентуму, позитивний заряд яких сприяє адсорбції індикатора і колір змінюється. В результаті сполука, яка знаходиться в осаді, набуває складу: AgI∙Ag+∙Ind.
Крім аргентометрії, для кількісного визначення йодидів можна застосовувати перманганатометрію і інші окисно-відновні методи.
Йодиди застосовуються як носії йоду при гіпертиреозі, ендемічному зобі. Якщо їжа або вода не містить достатньої кількості йоду, як це буває в деяких гірських місцевостях, у місцевого населення з’являється захворювання.
Натрію фторид. Безбарвні кристали або білий кристалічний порошок, розчинний у воді. Є сіллю середньої за силою кислоти фтороводневої, піддається гідролізу.
Тотожність визначають аналітичними реакціями на фторид-іон: взаємодією з іонами лужно-земельних металів. З солями кальцію і барію фториди дають білий осад:
Са2+ + 2F‾ → CaF2↓
Під дією фторидів тіоціанатні комплекси заліза (Ш) червоного кольору руйнуються і переходять в безбарні сполуки.
6F‾ + [Fe(SCN)n(H2O)6-n]3-n → [FeF6]3‾ + nSCN‾ + (6-n)H2O
Реакція з комплексною сполукою цирконію (ІV) і алізарину. Цирконій алізариновий комплекс червоного кольору руйнується фторидами. При цьому виділяється вільний алізарин жовтого кольору. Білий осад цирконію фториду, який виділяється при цьому може розчинятись в надлишку фторидів з утворенням безбарвного аніону [ZrF6]2-
Кількісне визначення проводять осадженням іонів фтору надлишком насиченого розчину РвСІ2 та зважуванням осаду РвFCI::
NaF + PbCI2 = PbFCI + NaCI
Застосовують у 2%-них розчинах або у вигляді пасти (нафестизин), що містить 75 частин препарату і 25 частин гліцерину, для профілактики захворювань зубів. Розчини, що містять 0,25г препарату і 10000 г води, вживають як антисептик. Зберігають як отруту за списком А.
Препарати елементів VI, V, IV, ІІІ і ІІ груп
1. Препарати гідроген пероксиду
Гідроген пероксид Н2О2 – безбарвна рідина з температурою кипіння 1520С. На відміну від води, гідроген пероксид проявляє слабкі кислотні властивості:
Н2О2 → Н+ + НО2‾
Солі гідроген пероксиду нестійкі. При дії на них розчинів мінеральних кислот виділяється гідроген пероксид:
ВаО2 + Н2SO4 → BaSO4 + H2O2
Гідроген пероксиду проявляє як окисні, так і відновні властивості і диспропорціонує з утворенням води і кисню:
2Н2О2 → 2Н2О + О2↑
2О‾ + 2е‾ = 2О2-
2О‾ – 2 е‾ = О20
Процес каталізується світлом, марганцю (1V) оксидом, іонами важких металів, лугами.Кислоти карбонові і їх аміди стабілізують розчини пероксиду водню, Як стабілізатор розчину пероксиду водню використовують бензоат натрію.
Препаратами гідрогену пероксиду є:
1) розчин гідрогену пероксиду концентрований, пергідроль, вміст гідрогену пероксиду 30%;
2) розчин гідрогену пероксиду, вміст гідрогену пероксиду 3%;
3) магнію пероксид, суміш пероксиду і магнію оксиду;
4) гідропірит, комплексна сполука гідрогену пероксиду з сечовиною.
Окисно-відновні властивості гідрогену пероксиду використовують для ідентифікації і кількісного визначення його в препаратах. Так, реакція окиснення гідрогену пероксиду розчином мангану перманганату лежить в основі його кількісного визначення:
2KMnO4 + 5H2O2 + 3H2SO4 → 2MnSO4 + K2SO4 + 8H2O + 5O2
При взаємодії з відновниками (наприклад калій йодидом) гідроген пероксид веде себе як окислювач:
H2O2 + KI + H2SO4 → I2 + 2H2O + K2SO4
Цю реакцію можна використати для ідентифікації і для кількісного визначення гідрогену пероксиду і його препаратів. При кількісному визначенні йод, який виділяється в даній реакції,відтитровують стандартним розчином натрію тіосульфату:
І2 + 2Na2S 2O3 → 2NaI + Na2 S 4O 6
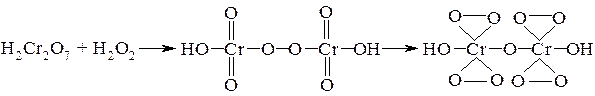 |
Специфічною реакцією на гідроген пероксид є утворення надхромових кислот при взаємодії його з розчином калію дихромату. Склад надхромових кислот залежить від умов проведення реакції – температури, рН, концентрації пероксиду. Реакція утворення надхромових кислот проводиться у середовищі сульфатної кислоти в присутності ефіру:
K2Cr2O7 + H2SO4 → H2Cr2O7 + K2SO4
Ефірний шар забарвлюється в синій колір, який через деякий час переходить в зелений внаслідок відновлення хрому (VІ) у хром (ІІІ). В ефірі надхромові кислоти стійкіші, тому забарвлення зберігається довше.
Натрію тіосульфат. Безбарвні прозорі кристали складу Na2S2O3∙5H2O.
Легко розчинний у воді. В теплому сухому повітрі вивітрюється, у вологому середовищі дещо розпливається.При температурі біля 50˚С плавиться в кристалізаційній воді.
Натрію тіосульфат є сіллю дуже нестійкої тіосульфатної кислоти. Має сильні відновні властивості і здатність до комплексоутворення, В кислому середовищі розкладається з утворенням вільної сірки і оксиду сульфуру (ІV):
Na 2S2O3 + 2HCI → 2NaCI + SO2 ↑ +S↓ + H2O
При взаємодії розчину натрію тіосульфату з водним розчином аргентуму нітрату спочатку утворюється білого кольору нерозчинна сіль – аргентуму тіосульфат:
Na2S2O3 + AgNO3 → Ag2S2O3↓ + 2NaNO3
Потім аргентуму тіосульфат розкладається внаслідок внутрішньомолекулярної окисно-відновної реакції до аргентуму сульфіду:
Ag2S2O3 + H2O → AgS↓ + H2SO4
Колір осаду при цьому змінюється послідовно від білого через жовтий і бурий до чорного.
Реакції з кислотою хлороводневою і аргентуму нітратом ДФ рекомендує для ідентифікації натрію тіосульфату. Якщо до аргентуму нітрату додавати розчин тіосульфату, білий осад, що випадає розчиняється в надлишку реактиву:
Ag2S2O3 + 3Na2S2O3 → 2 Na3[Ag(S2O3)3]
Натрію тіосульфат взаємодіє також з солями Си2+, Fe3+, Hg2+.Ці реакції (як і взаємодія з аргентуму нітратом) ідуть в 2 етапи: солеутворення і окиснення- відновлення.
Специфічними домішками в натрію тіосульфаті є сульфіти, сульфати і сульфіди. Сульфіти і сульфати визначаються в одній пробі. При цьому до досліджуваного розчину додають краплинами розчин йоду до жовтуватого забарвлення (сульфіти при цьому окиснюються до сульфатів), а потім додають розчин барію нітрату; рідина повинна залишатися прозорою (помутніння вказує на наявність домішки сульфітів або сульфатів).
Для виявлення сульфідів ДФ використовує здатність останніх як відновників взаємодіяти з натрію нітропрусидом з утворенням комплексної сполуки:
S2‾ + Na2[Fe(CN)5NO] → Na4[Fe(CN)5NOS]
Фармакопейний метод кількісного визначення натрію тіосульфату - йодометрія:
І2 + 2Na2S2O3 → 2NaI + Na2S4O6
Застосування натрію тіосульфату грунтується на його здатності виділяти сірку. Препарат використовується як протиотрута при отруєннях галогенами, ціанідами і синільною кислотою: H+
КСN + Na2S2O3 ──→ KCNS + Na2SO4
Роданід калію (КСNS), який утворюється, менш отруйний, ніж ціанід калію. Тому при отруєнні синільною кислотою або її солями як перша допомога застосовується натрію тіосульфат. Препарат може використовуватись також при отруєнні сполуками миш’яку, ртуті, свинцю; при цьому утворюються неотруйні сульфіди.
Натрію тіосульфат застосовується також при алергічних захворюваннях, артритах, невралгії, разом з хлоридною кислотою – для лікування корости.
Натрію нітрит може бути природного походження. Він утворюється з аміаку при гнитті органічних сполук. Синтетично одержують як побічний продукт при виробництві азотної кислоти:
2NO2 + Na2CO3 → NaNO2 + NaNO3 + CO2↑
Натрію нітрит – білі прозорі кристали з жовтуватим відтінком. Легко розчиняється у воді, утворюючи розчини з слабколужною реакцією, в спирті розчиняється важко. Гігроскопічний.
При додаванні до розчину NaNO2 розведеної кислоти сульфатної виділяються червоно-бурі пари оксидів азоту:
NaNO2 + H2SO4 → NaHSO4 + HNO2
HNO2 → H2O + NO↑ + NO2↑
Ця реакція приводиться в ДФ для підтвердження тотожності препарату. Нітроген в натрію нітриті (ступінь окиснення +3) може проявляти як окиснювальні, так і відновні властивості. Ця властивість натрію нітриту використовується в реакціях ідентифікації препарату:
2КMnO4 + 5NaNO2 + 3H2SO4 → K2SO4 + 2MnSO4 + 5NaNO3 + 3H2O
В даній реакції натрій нітрит діє як відновник. В реакції з бромідами і йодида в кислому середовищі натрію нітрит проявляє окисні властивості.
2NaNO2 + 2NaI + 4CH3 COOH → 2NO↑ + 4CH3COONa + I2 + 2H2O
Ці реакції можуть бути використані для ідентифікації препарату, хоч вони і не є фармакопейними. ДФ рекомендує для підтвердження тотожності натрію нітриту реакції на виявлення натрій-іону (реакція забарвлення полум’я в жовтий колір) і нітрит-іону: а) з дифеніламіном в кислому середовищі з утворенням органічного барвника яскраво-синього кольору; б) з антипірином в кислому середовищі з утворенням нітрозоантипірину, який має смарагдово-зелене забарвлення.
Кількісний вміст натрію нітриту в препараті визначається йодометричним методом. Натрію нітрит окиснюється перманганатом калію, надлишок якого визначається йодометрично (фармакопейний метод):
5NaNO2 + 2KMnO4 + 3H2SO4 → 5NaNO3 + 2MnSO4 + K2SO4 + 3H2O
2KMnO4 + 10 KI + 8H2SO4 → 5I2↓ + 6K2SO4 + 2MnSO4 + 8H2O
I2 + 2Na2S2O3 → 2NaI + Na2S4O6
Натрію нітрит застосовують як судинорозширювальний засіб при стенокардії, мігрені, внутрішньо і підшкірно. Для ін’єкцій використовують 1% розчин.
Нітрити дуже отруйні, якщо їх застосовувати у великих кількостях. Натрію нітрит застосовують також при отруєнні ціанідами.
З інших сполук нітрогену використовують розчин аміаку у воді (нашатирний спирт), для вдихання хворими у непритомному стані (збуджує дихання). Застосовують амонію хлорид (нашатир), амонію бромід (при розладах центральної нервової системи).
Натрію гідрокарбонат – білий кристалічний порошок без запаху, розчинний у воді, практично нерозчинний в спирті. Стійкий в сухому повітрі, повільно розкладається у вологому.
Натрію гідрокарбонат застосовують як антацидний засіб при підвищеній кислотності шлункового соку.Його також використовують як наповнювач при таблетуванні ЛЗ і як стабілізатор при приготуванні деяких ін’єкційних розчинів (розчин натрію тіосульфату).
Літію карбонат – білий кристалічний порошок, важко розчинний у воді, практично нерозчинний в спирті. Застосовується в психіатрії для попередження судом.
Дані лікарські препарати є солями, утвореними лужними металами і слабкою карбонатною кислотою. Розчинна у воді сіль натрію гідрокарбонату має слабколужну реакцію середовища. Ідентифікація ЛЗ проводиться за катіоном і за аніоном:
1. Реакції на іон Na+: забарвлення полум’я, із цинк уранілацетатом та KSb(OH)6.
2. Реакції на іон Li+ проводять після розчинення літію карбонату в кислоті, бо у воді він не розчиняється:
Li2CO3 + 2HCI → 2LiCI + CO2↑+ H2O
Розчинні солі літію в слабколужному середовищі з гідрофосфатами дають білий осад літію фосфату:
3Li+ + HPO42‾ + OH‾ → Li3PO4↓ + H2O
Солі літію забарвлюють безбарвне полум’я пальника в карміново-червоний колір.
3. Реакції на аніони HCO3‾ i CO32‾ грунтуються на витісненні сильною мінеральною кислотою карбонатної кислоти з її солей. Кислота карбонатна нестійка і виділяє СО2 (бульбашки газу). Якщо його пропустити через вапняну воду, то утвориться білий осад.
При кип’ятінні з насиченим розчином магнію сульфату гідрокарбонат –іон дає білий осад. Карбонат –іон дає такий же осад без кип’ятіння:
2NaHCO3 −−→ Na2CO3 + CO2↑ + H2O
4Na2CO3 + 4MgSO4 + 4H2O → 3MgCO3∙Mg(OH)2∙3H2O↓ + 4Na2SO4 + CO2↑
Чистота. У препараті натрію гідрокарбонату визначають наявність менш розчинних домішок за еталоном каламутності №4. Якщо натрію гідрокарбонат використовують для ін’єкцій або для стабілізації ін’єкційних розчинів, його розчин повинен бути прозорим.
Домішки карбонатів визначають прокалюванням. Втрата маси при цьому повинна бути не менше 36,6%. Чим більше домішок карбонатів, тим менша втрата маси при прокалюванні.
Кількісне визначення натрію гідрокарбонату і літію карбонату проводять методом ацидиметрії, титрант – 0,1 М розчин кислоти хлорадної, індикатор – метиловий оранжевий. Визначення натрію гідрокарбонату проводять прямим методом:
NaHCO3 + HCI → NaCI + H2O + CO2






