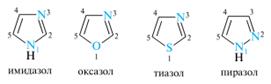
Реакционная способность азолов по отношению к электрофильным реагентам определяется π-балансом системы. Для этих гетероциклов общая π-избыточность или π-дефицитность зависит от того, какой из гетероатомов — пиррольного или пиридинового типа — оказывает большее влияние. Например, имидазол, пиразол и тиазол, для которых ниже показаны заряды на атомах цикла, относятся к слабо π-избыточным системам. В то же время оксазолу присуща незначительная π-дефицитность, вызванная электроотрицательностью атома кислорода.
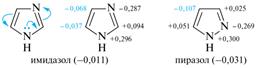
Реакционную способность молекулы будет определять общая (невысокая) π-избыточность. Из-за присутствия в цикле электроноакцепторного атома азота пиридинового типа азолы вступают в реакции электрофильного замещения намного труднее, чем их аналоги с одним гетероатомом (пиррол, фуран и тиофен), но легче, чем пиридин. Замещение в 1,3-азолах идет преимущественно по атому С-5, в 1,2-азолах — по атому С-4.
Имидазол.
Алкилирование и ацилированиепо атому азота. При нагревании с алкилирующими агентами (алкилгалогенидами или алкилсульфатами) 1-алкилимидазолы получаются с невысоким выходом, так как побочно образуются имидазолиевые соли.
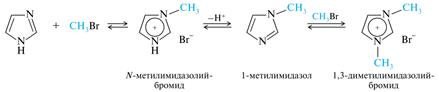
Действие на имидазол галогенангидридов или ангидридов кислот приводит к высокореакционноспособным N-ацильным производным.
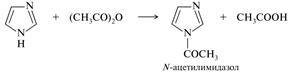
Восстановлением N-ацилимидазолов с высоким выходом могут быть получены альдегиды, а реакцией с магнийорганическими соединениями — кетоны:
Замещение по атомам углерода.
Нитрование и сульфирование.
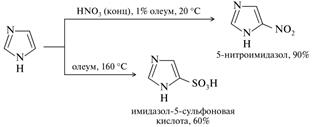
Со слабыми электрофилами в кислой среде реакции не идут вовсе. До сих пор неизвестны примеры реакций алкилирования и ацилирования имидазола по Фриделю-Крафтсу.
В щелочной среде имидазолы со свободной NH-группой и хотя бы одним незамещенным кольцевым атомом углерода вступают в реакцию азосочетания:
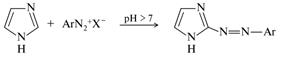
С диазотированной сульфаниловой кислотой, например, образуются продукты, окрашенные в цвета от желтого до красного, обнаружить которые можно в количестве микрограммов. Это — давно известный тест Паули на имидазолы (качественная реакция).
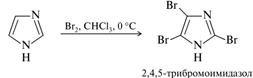
Галогенирование имидазола в нейтральной среде, когда молекула не ионизирована, очень легко.
Пиразол.
Имеет много общего с имидазолом. Это касается как алкилирования и ацилирования по пиридиновому атому азота, так и электрофильного замещения. Отличие в реакциях электрофильного замещения заключается в направлении электрофильной атаки: в пиразоле она идет, как правило, по атому C-4, где π-электронная плотность максимальна. Если атом C-4 замещен, то электрофильная атака часто становится невозможной.
Подобно имидазолу, пиразол не алкилируется и не ацилируется по Фриделю-Крафтсу, но в отличие от имидазола он не вступает и в реакцию азосочетания.
Представители.
Пиразол и его производные в природе не обнаружены, но они используются в производстве лекарственных средств (анальгин, амидопирин, антипирин) и пестицидов.
Тиазол. Важнейшее соединение ряда тиазол — тиамин (Vit В1). Многие производные — лекарственные препараты (норсульфазол, фталазол). Тиазолидиновое кольцо — структурный фрагмент пенициллина и разнообразных полусинтетических пенициллинов.
Производные пятичленных азотсодержащих ароматических гетероциклов: пиразолон и его таутомерия, лекарственные средства на основе пиразолона–3; гистидин, гистамин, бензимидазол, дибазол.
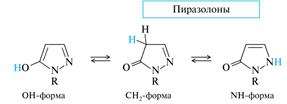
Пиразолоны. Среди производных пиразола важное место занимают 5-гидроксипиразолы. Они существуют в нескольких таутомерных формах; три наиболее устойчивые ниже. В неполярных растворителях преобладает CH2-таутомер с некоторым количеством NH-формы; эти формы имеют название пиразолоны. В водной среде основным является NH-таутомер (с примесью OH-формы).
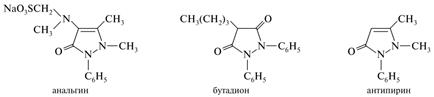
В медицине применяется ряд лекарственных средств, в основе которых лежит структура пиразолона-3. Наиболее известные из них — анальгин и диоксоаналог бутадион, обладающие противовоспалительным действием. Одним из первых синтетических анальгетиков, известным с 1884 г., был антипирин.
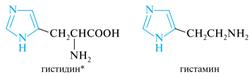
Имидазол — структурный фрагмент витамина белковой аминокислоты гистидина и ее метаболита — биогенного амина гистамина, а также некоторый лекарственный средств.
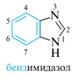
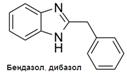
Дибазол – лекарственный препарат группы периферических вазодилататоров. Препарат оказывает выраженное сосудорасширяющее действие, способствует снижению давления, обладает спазмолитическим эффектом.
Шестичленные гетероциклы: электронное строение; основные и нуклеофильные свойства пиридина и пиримидина, лактим–лактамная таутомерия гидроксипроизводных пиридина. Представители: пиридин, хинолин, изохинолин, пиримидин.






