К растворам NaCl, HNO3, CuSO4, KNO3 прибавили раствор гидроксида натрия. В каком случае произошла реакция? Напишите молекулярные и ионные уравнения этих реакций.
Решение.
Чтобы определить, произошла или нет реакция, распишем молекулярные и ионные уравнения:
1. NaCl + NaOH = NaOH + NaCl,
Na+ + Cl- + Na+ + OH- = Na+ + OH- + Na+ + Cl-.
В левой части и правой части уравнения ионы не претерпевают никаких изменений, реакция не идет.
2. HNO3 + NaOH = NaNO3 + H2O,
H+ + NO  + Na+ + OH- = Na+ + NO
+ Na+ + OH- = Na+ + NO  + H2O,
+ H2O,
H+ + OH- = H2O.
Реакция протекает с образованием слабого электролита - воды.
3. CuSO4 + 2NaOH = Cu(OH)2¯ + Na2SO4,
Cu2+ + SO  + 2Na+ + 2OH- = Cu(OH)2¯ + 2Na+ + SO
+ 2Na+ + 2OH- = Cu(OH)2¯ + 2Na+ + SO  .
.
Cu2+ + 2OH– = Cu(OH)2
Реакция протекает с образованием трудно растворимого дигидроксида меди, который выпадает в осадок.
4. KNO3 +NaOH = KOH + NaNO3,
K+ + NO  + Na+ + OH- = K+ + OH- + Na+ + NO
+ Na+ + OH- = K+ + OH- + Na+ + NO  .
.
Реакция не идет, левая и правая части уравнения идентичны.
Задания
181. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) NaHCO3 и NаOH; б) K2SiО3 и НСl; в) BaCl2 и Na2SO4.
182. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) K2S и НСl; б) FеSO4 и (NH4)2S; в) Сг(ОН)3 и КОН.
183. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Mg2+ + СО  = MgCО3
= MgCО3
б) Н+ + ОН– = Н2О
184. Какое из веществ: AI(OH)3, H2SO4, Ba(OH)2 будет взаимодействовать с гидроксидом калия? Выразите эти реакции молекулярными и ионно-молекулярными уравнениями.
185. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) КНСОз и H2SO4 б) Zn(OH).2 и NaOH;
в) CaCI2 и AgNO3,.
186. Составьте молекулярные и инонно-молекулярные уравнения взаимодействия в растворах между: a) CuSO4 и H2S, BaCO3 и HNO3, в) FeCI3 и КОH.
187. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Сu2+ + S2– = CuS
б) SiО  + 2H+ = H2SiO3
+ 2H+ = H2SiO3
188. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия а растворах между; a) Sn(OH)2 и НС1; б) BeSO4 и КОН;
в) NH4Cl и Ba(OH)2.
189. Какое из веществ KHCO3, CH3COOH, NiSO4, Na2S будет взаимодействовать с раствором серной кислоты? Напишите для этих реакций молекулярные и ионно-молекулярные уравнения.
190. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Hg(NO3)2 и NaJ; б) Pb(NO3)2 и KJ
в) CdSO4 и Na2S.
191. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) СаСO3 + 2Н+ = Ca2+ + H2O + CO2
б) А1(ОН)3 + ОH– =А1O 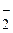 + 2Н2O
+ 2Н2O
в) РЬ2+ + 2J– =РbJ2.
192. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Ве(ОН)2 и NaOH; б) Сu(ОН)2 и HNO3;
в) ZnOHNO3 и HNO3.
193. Составите, молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) Na3PO4 и CaCl2; б) К2СО3 и BaCI2;
в) Zn(OH)2 и КОН.
194. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Fe (ОН)3 + 3Н+ = Fe3+ + 3Н2О
в) Cd2+ + 2OH– = Cd(OH)2
в) H+ + NO 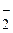 = HNO2
= HNO2
195. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) CdS и HCI; б) Cr(OH)3 и NaOH; в) Ва(ОН)2 и CoCI2.
196. Составьте молекулярные уравнения реакции, которые выражаются ионно-молекулярными уравнениями:
а) Zn2+ + H2S = ZnS + 2H+
я) HCO  + H+ = H2O + CO2
+ H+ = H2O + CO2
в) Ag+ + Cl– = AgCI
197. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) H2SO4 и Ва(ОН)2; б) FeCl3 и NH4OH;
в) CH3COONa и HCI.
198. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: a) FeCl3 и КОН; б) NiSO4 и (NH4)2S;
в) MgCO3 и HNO3.
199. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
а) Be (ОН)2 + 2 ОН– = BeO  + 2H2O
+ 2H2O
б) СН3СОО– + Н+ = СН3СООН
в) Ba2+ + SO 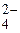 = BaSO4
= BaSO4
200. Какое из веществ: NaCl, NiSO4, Ве(ОН)2, KHCO3 будет взаимодействовать с раствором гидроксида натрия. Напишите эти реакции в молекулярной и ионно-молекулярной форме.
Гидролиз солей






