Сколько граммов оксида кальция содержится в 200 мл 0,3 н. раствора? Рассчитайте титр раствора.
Решение. Молярная концентрация эквивалентов или нормальная концентрация (Сэкв) показывает, сколько молей эквивалентов вещества содержится в 1 литре раствора, ее рассчитывают по формуле, (моль/л):
Сэкв =  .
.
Здесь m - масса растворенного вещества, г; Мэкв. - молярная масса эквивалента вещества, г/моль; V - объем раствора, мл.
Титр раствора (Т) показывает, сколько граммов вещества содержится в 1 мл раствора. Титр раствора связан с нормальной концентрацией соотношением, (г/мл):
Т =  , г/мл,
, г/мл,
Рассчитаем молярную массу эквивалента гидроксида кальция:
Мэкв.Ca(OH)2 = 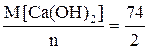 = 37 г/моль
= 37 г/моль
и массу Ca(OH)2 в 200 мл раствора по формуле
Сэкв =  . Þ Мэкв. =
. Þ Мэкв. =  = 2,22 моль/л.
= 2,22 моль/л.
Зная нормальную концентрацию раствора, можно рассчитать его титр:
Т =  = 0,0111 г/мл.
= 0,0111 г/мл.
Задания
141. Вычислите молярную и нормальную концентрации раствора с массовой долей хлорида кальция 20%, плотность которого 1,178 г/см3. Ответ: 2,1 М; 4,2 н.
142. Чему равна нормальная концентрация раствора с массовой долей NaOH 30 %, плотность которого 1,328 г/см3? К 1 л этого раствора прибавили 5 л воды. Вычислите массовую долю NaOH в полученнм растворе. Ответ: 9,96 н.; 6.3%.
143. К 3 л раствора с массовой долей HNO3 10%, плотность которого 1,054 г/см3, прибавили 5 л раствора той же кислоты с массовой долей 2% плотностью 1,009 г/см3. Вычислите массовую долю и молярную концентрации полученного раствора, если считать, что его объем равен 8 л. Ответ: 5,0 %; 0,82 М.
144. Вычислите нормальную и моляльную концентрации раствора HNO3 с массовой долей 20,8 %, плотность, которого 1,12 г/см3. Сколько граммов кислоты содержится в 4 л этого раствора? Ответ: 3,70 н.; 4,17 м; 931,8 г.
145. Вычислите молярную, нормальную и моляльную концентрации раствора с массовой долей хлорида алюминия 16 %, плотность которого 1,149 г/см3.
Ответ: 1,38 М; 4,14 н; 1,43 м.
146. Сколько и какого вещества останется в избытке, если к 75 см3 0,3 н. раствора H2SO4 прибавить 125 см3 0,2 н. раствора КОН? Ответ: 0,14 г КОН.
147. Для осаждения в виде AgCl всего серебра, содержащегося в 100 см3 раствора AgNO3, потребовалось 50 см3 0,2 н раствора НСl. Чему равна нормальная концентрация раствора AgNO3? Сколько граммов АgCl выпало в осадок?
Ответ: 0,1 н; 1,433 г.
148. Какой объем раствора с массовой долей НСl 20,01 % (плотность
1,100 г/см3) требуется для приготовления 1 л раствора с массовой долей HCl
10,17 % (плотность 1,050 г/см3)? Ответ: 485,38 см3.
149. Смешали 10 см3 раствора с массовой долей HNO3 10 % (плотность 1,056 г/см3) и 100 см3 раствора с массовой долей HNO3 30 % (плотность 1,184 г/см3). Вычислите массовую долю HNO3 в полученном растворе. Ответ: 28,38 %.
150. Какой объем раствора с массовой долей КОН 50 % (плотность
1,538 г/см3) требуется для приготовления 3 л раствора с массовой долей КОН 6 % (плотность 1,048 г/см3)? Ответ: 245,5см3.
151. Какой объем раствора с массовой долей карбоната натрия 10 % (плотность 1,105 г/см3) требуется для приготовления 5 л раствора с массовой долей карбоната натрия 2 % (плотность 1,02 г/см3)? Ответ: 923,1 см3.
162. На нейтрализацию 31 см3 0,16 н. раствора щелочи требуется 217 см3 раствора H2SO3. Чему равны нормальная концентрация и титр раствора H2SO4?
Ответ: 0,023 н.; 1,127×10–3 г/см3.
153. Какой объем 0,3 н. раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaOH в 40 см3? Ответ: 26,6 см3.
154. На нейтрализацию I л раствора, содержащего 1,4 г КОН, требуется 50 см3 раствора кислоты. Вычислите нормальную концентрацию раствора кислоты.
Ответ: 0.53 н.
155. Сколько граммов HNO3 содержалось в растворе, если на нейтрализацию его потребовалось 35 см3 0,4 н. раствора NaOH? Чему равен титр раствора NaOH? Ответ: 0,882 г, 0,016 г/см3.
156. Сколько граммов NaNO3 нужно растворить в 400 г воды, чтобы приготовить раствор с массовой долей NaNO3 20 %? Ответ: 100 г.
157. Смешали 300 г раствора с массовой долей NaCl 20 % и 500 г раствора c массовой долей NaCl 40 %. Чему равна массовая доля NaCl в полученном растворе? Ответ: 32,5%.
158. Смешали 247 г раствора с массовой долей серной кислоты 62 % и 145 г раствора с массовой долей серной кислоты 18%. Какова массовая доля серной кислоты в полученном растворе после смешения?
Ответ: 45,72 %.
159. Из 700 г раствора серной кислоты с массовой долей 60 % выпариванием удалили 200 г воды. Чему равна массовая доля серной кислоты в оставшемся растворе? Ответ: 84 %.
160. Из 10 кг раствора с массовой долей растворенного вещества 20 % при охлаждении выделилось 400 г соли. Чему равна массовая доля растворенного вещества охлажденного раствора? Ответ 16,7 %.
Свойства растворов






