КОНСПЕКТ ЛЕКЦИЙ ПО УЧЕБНОЙ ДИСЦИПЛИНЕ
«ГИДРОГАЗОДИНАМИКА»
Направление/специальность: __ 20.03.01 Техносферная безопасность _
(код, наименование специальности /направления)
Профиль/специализация: Безопасность жизнедеятельности в техносфере
Квалификация (степень) выпускника: __ бакалавр _____ ____________ __ Форма обучения: __ заочная_________ ___ ____
МОСКВА
Раздел 1. ОСНОВЫ ГИДРОСТАТИКИ.
| Содержание: |
| 1.1. Основные физические свойства жидкостей и газов. |
| 1.2. Гидростатика. |
ОСНОВНЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА ЖИДКОСТЕЙ И ГАЗОВ
Характеристика жидкостей и газов
Жидкостью называется физическое тело, обладающее легкой подвижностью частиц, то есть текучестью.
Жидкости с точки зрения физико-механических свойств разделяются на два класса - капельные жидкости (или малосжимаемые) и газы (или сжимаемые жидкости). Жидкость рассматривается в гидравлике обычно как сплошная (непрерывная), однородная и изотропная среда, обладающая одинаковыми свойствами во всех точках и по всем направлениям.
Основными физическими свойствами жидкости и газов, базируясь на которых в гидравлике устанавливаются общие законы ее равновесия и движения, являются:
1) текучесть, 2) весомость, 3) изменяемость объема и 4) вязкость.
Текучесть
Текучестью называется неспособность жидкости сопротивляться внутренним сдвигающим усилиям, вызванным сколь угодно малыми силами.
Свойство текучести выражает физически главное отличие жидкого тела от твердого тела.
Вследствие текучести, жидкость, находясь в покое, растекается под действием собственного веса и принимает форму того сосуда, в котором находится. Растекаясь в сосуде и занимая часть его объема, жидкость всегда образуют свободную поверхность.
Газы, растекаясь, всегда занимают весь объем сосуда и не образуют свободной поверхности.
Удельный вес и плотность
Удельным весом g называется вес единицы объема жидкости, который определяется по формуле
 , (1.1)
, (1.1)
где: G – вес жидкости в объеме W.
Удельный вес - величина размерная. Его размерность

Плотностью r называется масса, заключенная в единице объема жидкости, которая определяется по формуле
 (1.2)
(1.2)
где: М - масса жидкости, заключенная в объеме W.
Размерность плотности:
в системе СИ



Зависимость между удельным весом и плотностью жидкости легко получить, помня, что по второму закону Ньютона
G = Mg.
Разделив обе части уравнения на объем W, получим
g = r g. (1.3)
Это равенство выражает второй закон Ньютона, записанный для единицы объема жидкости.
Удельный объем V – объем единицы массы вещества - величина, обратная плотности.
V = W/m=1/ρ.
Размерность – [м3/кг].
Изменяемость объема жидкостей и газов под действием температуры и давления
Изменяемость объемаот давления и температуры для капельных жидкостей.
Свойство жидкости изменять объем под действием давления называется сжимаемостью и характеризует упругость жидкости.
Изменение объема жидкости  при изменении давления на
при изменении давления на 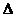 р (рис. 1.1)
р (рис. 1.1)
 (1.4)
(1.4)
Величина  , характеризующая изменение объема жидкости при изменении давления, отрицательна, так как при сжатии жидкости положительному приращению давления соответствует отрицательное приращение объема.
, характеризующая изменение объема жидкости при изменении давления, отрицательна, так как при сжатии жидкости положительному приращению давления соответствует отрицательное приращение объема.
Сжимаемость жидкости оценивается коэффициентом объемного сжатия bw
 соответственно
соответственно 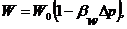
 (1.5)
(1.5)
где: W 0 - начальный объем жидкости; ΔW - изменение объема при изменении давления на Δ p.
Коэффициент объемного сжатия b w представляет собой относительное уменьшение объема жидкости (по отношению к начальному объему) при увеличении давления на единицу и имеет размерность обратную размерности давления


| |
Величина обратная коэффициенту объемного сжатия является модулем упругости жидкости при всестороннем сжатии
 (1.6)
(1.6)
Капельные жидкости, как и твердые тела, представляют собой малосжимаемую, малоупругую среду (модуль упругости воды E=2,1.103 кгс/см2, стали E=2.106 кгс/см2). В связи с этим при решении очень многих практических задач гидравлики сжимаемостью жидкости можно пренебречь, полагая, что жидкость не изменяет своего объема при изменении давления (bw=0), а, следовательно, ее удельный вес и плотность остаются постоянными: g=const и r=сonst.
В отдельных случаях сжимаемость должна учитываться, например, при гидравлическом ударе, связанном с упругими колебаниями жидкости.
Температурное расширение - изменение объема жидкости при увеличении температуры при Р = const.
Изменение объема жидкости  при изменении температуры на
при изменении температуры на 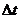 равно
равно
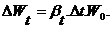 (1.7)
(1.7)
Изменение объема жидкости при изменении температуры характеризуется коэффициентом объемного (температурного) расширения b t.
 соответственно
соответственно 

 (1.8)
(1.8)
где: W - начальный объем жидкости;
dW - изменение объема при изменении температуры на Δt.
Величина b t выражает относительное изменение объема жидкости при изменении температуры на единицу и имеет размерность

Объем жидкости с увеличением температуры увеличивается. Однако это увеличение незначительно. Например, у воды при изменении температуры от 0 до 100°С при давлениях от I до 100 ат величина b t изменяется в пределах
 ,
,
т.е.достигает максимум 0,07 % при увеличении температуры на 1°С, Поэтому при решении многих практических задач влиянием изменения объема жидкости при изменении температуры на величину ее удельного веса и плотности можно пренебречь, полагая bt = 0, а, следовательно, g = const и r = const. Однако, следует учитывать, что увеличение объема жидкости при повышении температуры может вызвать опасные последствия, например, разрушение гидравлической системы, в которой заперты без возможности расширения значительные объемы жидкости и т.п.
Изменяемость объемаот давления и температуры для газов.
В отличие от капельных жидкостей газы характеризуются значительной сжимаемостью и высокими значениями коэффициента температурного расширения.
Характерной особенностью изучения сжимаемых жидкостей является необходимость учитывать соотношение между давлением p, плотностью (удельным весом) g= g r, удельным объемом  и температурой T °К (Кельвина).
и температурой T °К (Кельвина).
Это соотношение, устанавливающее зависимость между физическими величинами, определяющими состояние газа (давлением газа р, его объёмом V и абсолютной температурой Т) называется уравнением состояния.
Для идеального газа уравнение состояния (уравнение Клапейрона - Менделеева) записывается в следующем виде:
 или
или 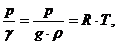 (1.9)
(1.9)
где: R = 29,27 м/°К – универсальная газовая постоянная;
g = 9,81 м/c2 - ускорение силы тяжести.
Газовая постоянная имеет физический смысл работы расширения 1 моля (моль - число граммов химического вещества, равное его молекулярной массе) идеального газа под постоянным давлением при нагревании на 1°. Газовая постоянная обычно численно выражается в следующих единицах: 8,3143 ± 0,0012 дж/град-моль, 8,314-107 эрг/град-моль, 1,986 кал/град-моль, 82,05-10-3 л·атм/град-моль.
Универсальная газовая постоянная, отнесённая не к 1 молю, а к 1 молекуле, называется постоянной Больцмана. Постоянная Больцмана - одна из основных физических постоянных, равная отношению универсальной газовой постоянной R к числу Авогадро NA
k = R/NA (k = (1,38054±0,00018)´10-23дж/К).
(Число Авогадро - число молекул в 1 моле любого вещества, оно одинаково и равно 6,02252.1023. Моль любых веществ, находящихся в состоянии идеального газа, при нормальных условиях [0°С и давлении 101325 н/м 2 (760 мм. рт. ст.) ] занимают приблизительно один и тот же объём, равный 22,4 л).
Для газа, имеющего общую массу М и молекулярную массу μ, уравнение состояния записывается в виде
 или pV=NkT, (1.10)
или pV=NkT, (1.10)
где N - число частиц газа, k - Больцмана постоянная.
Уравнение состояния представляет собой уравнение состояния идеального газа, которое объединяет Бойля - Мариотта закон (зависимость между р и V при Т = const), Гей-Люссака закон (зависимость V от Т при р = const) и Авогадро закон (согласно этому закону, газы при одинаковых значениях р, V и Т содержат одинаковое число молекул N).
Уравнение Клапейрона - наиболее простое уравнение состояния, применимое с определённой степенью точности к реальным газам при низких давлениях и высоких температурах (например, атмосферный воздух, продукты сгорания в газовых двигателях и др.), когда они близки по своим свойствам к идеальному газу.
Наиболее простыми свойствами обладает газ, разреженный настолько, что взаимодействие между его молекулами может не учитываться, так называемый совершенный (идеальный) газ. Для совершенных газов справедливо уравнение Клапейрона, позволяющее определять плотность газа при известных давлении и температуре, т. е.
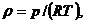 (1.11)
(1.11)
где р - абсолютное давление; R - удельная газовая постоянная, различная для разных газов, но не зависящая от температуры и давления [для воздуха R =287 Дж/(кг . К)]; Т - абсолютная температура.
Поведение реальных газов в условиях, далеких от сжижения, незначительно отличается от поведения совершенных газов, и для них в широких пределах можно пользоваться уравнениями состояния совершенных газов.
В технических расчетах плотность газа обычно приводят к нормальным физическим условиям (t=0°С; Р=101325 Па) или к стандартным условиям (t=20°С; р=101325 Па).
Плотность воздуха при R=287 Дж/(кг . К) в стандартных условиях по формуле (1.11) будет

При других условиях плотность воздуха определяется по формуле
 (1.12)
(1.12)
Для изотермического процесса (T=const) из формулы (2.10) имеем
p/ρ= const, (1.13)
а для адиабатического процесса
р/ρ k = const, (1.14)
где k = cp/ cv - адиабатическая постоянная газа (здесь с p - теплоемкость газа при постоянном давлении; сv - то же, при постоянном объеме).
Сжимаемость газов зависит от характера процесса изменения состояния:
для изотермического процесса
E0= p. (1.15)
а для адиабатического
Е0 = kp. (1.16)
Из выражения (19) следует, что изотермическая сжимаемость для атмосферного воздуха составляет ~9,8-104Па, что примерно в 20 тыс. раз превышает сжимаемость воды.
Сжимаемость сплошной среды можно также характеризовать отношением приращения давления dp к приращению ее плотности d r. Характеристикой, определяющей зависимость изменения плотности газа при изменении давления в движущемся потоке, является скорость распространения звука а.
В однородной среде скорость распространения звуковых колебаний, как отмечено выше, определяется из выражения.
а2= dp/ dρ. (1.17)
С учетом соотношений (8) и (9) из выражения (21) находим скорость звука в виде зависимости
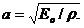 (1.18)
(1.18)
Для адиабатического процесса из выражений (18) и (14) следует: dp/ dρ =kр/ρ=kRT, откуда для газов
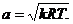 (1.19)
(1.19)
Скорость распространения звука (при t=20°С) в воздухе составляет 330 м/с, в углекислом газе - 261 м/с, в воде - 1480 м/с.
Поскольку объем газа в большой мере зависит от температуры и давления, выводы, полученные при изучении капельных жидкостей, можно распространять на газы лишь в том случае, если в пределах рассматриваемого явления изменение давления и температуры невелико.
Значительные разности давлений, вызывающие существенное изменение плотности газов, могут возникнуть при движении газов с большими скоростями. Соотношение между скоростью движения жидкости и скоростью звука в ней позволяет судить о необходимости учета сжимаемости в каждом конкретном случае. Практически газ можно принимать несжимаемым при скоростях движения, не превышающих 100 м/с.






