Каждая окислительно-восстановительная полуреакция характеризуется определенным окислительно-восстановительным потенциалом. В стандартных условиях и концентрации потенциалопределяющих частиц равной 1 моль/л, его называют стандартным э лектродным потенциалом (Е 0, В). Для многих окислительно-восстановительных систем они определены и сведены в таблицу (см. приложение).
Величина электродного потенциала зависит от природы и концентрации потенциалопределяющих частиц в растворе, температуры и рН среды. Эта зависимость выражается уравнением Нернста:
 . (1)
. (1)
В этом уравнении Е – электродный потенциал (В); Е 0- стандартный электродный потенциал (В); R = 8,31 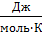 -универсальная газовая постоянная; Т -температура (К); n – число моль электронов в полуреакции; F =96500Кл–число Фарадея; a окисл-активность окисленной формы потенциалопределяющих частиц (моль/л); a восст – активность восстановленной формы потенциалопределяющих частиц (моль/л).
-универсальная газовая постоянная; Т -температура (К); n – число моль электронов в полуреакции; F =96500Кл–число Фарадея; a окисл-активность окисленной формы потенциалопределяющих частиц (моль/л); a восст – активность восстановленной формы потенциалопределяющих частиц (моль/л).
Введем несколько упрощений:
1) при стандартной температуре 298К и переходе к десятичным логарифмам, получим 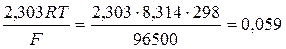 В;
В;
2) для разбавленных растворов активности с достаточным приближением могут быть заменены концентрациями (a окисл=[окисл], a восст =[восст]). В результате для стандартной температуры уравнение принимает следующий вид:
 , (2)
, (2)
где «х» и «y» коэффициенты перед окисленной и восстановленной формами потенциалопределяющих частиц в ОВ-полуреакции.
Например, для полуреакции окисления ионов Mn2+
Mn2++4H2O -5 ē = MnO4- + 8H+ Е 0=1,507 В
слева – восстановленная форма потенциалопределяющих частиц, а справа – окисленная форма, поэтому ур. (2) для стандартной температуры будет иметь следующий вид:

Электродный потенциал служит мерой окислительно-восстановительной способности веществ. Чем меньше значение Е 0, тем большими восстановительными свойствами обладает вещество. И, наоборот, чем больше Е 0, тем выше его окислительные свойства.
Например, перманганат KMnO4 является окислителем, но в зависимости от кислотно-щелочности среды он может проявлять различные окислительные свойства:
а) в кислой среде
MnO4- + 8H++ 5 ē ® Mn2+ + 4H2O  1,507 В
1,507 В
б) в нейтральной среде
MnO4- + 2H2О+ 3 ē ® MnО2 + 4OН- 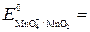 0,6 В
0,6 В
в) в щелочной среде
MnO4- + ē ® MnO42-  0,56 В
0,56 В
В кислой среде Е 0 больше, следовательно, в кислой среде MnO4- проявляет более сильные окислительные свойства.
Пероксид водорода H2O2, имеющий в своем составе кислород в промежуточной степени окисления (-1), может проявлять как окислительные, так и восстановительные свойства.
Восстановление H2O2 протекает по реакциям:
H2O2 + 2H+ + 2 ē = 2H2O  1,776 B (кислая среда)
1,776 B (кислая среда)
H2O2 + 2 ē = 2OН-  0,88 B (щелочная среда)
0,88 B (щелочная среда)
Окисление H2O2 происходит по реакци:
H2O2 - 2 ē = О2 + 2Н+  0,682 B
0,682 B






