Существует два способа определения коэффициентов в уравнениях окислительно-восстановительных реакций:
Метод электронного баланса позволяет определить коэффициент лишь перед молекулами окислителя и восстановителя, а для остальных участников они находятся подбором, с учетом уже найденного числа ионов окислителя и восстановителя. Метод основан на сравнении степеней окисления атомов в исходных и конечных веществах. Правильность написания уравнения проверяется путем подсчета атомов каждого элемента в левой и правой частях уравнения. Сумма зарядов исходных веществ также должна быть равна сумме зарядов продуктов реакции.
Более универсальный ионно-электронный метод использует представления об электролитической диссоциации. Участники процесса записываются в ионном виде. Метод применим, если реакции протекают в водном растворе. Вещества диссоциируют на ионы, реальность существования которых может быть обнаружена в растворе. В этом случае учитывают процесс диссоциации воды Н2О ↔ Н+ + ОН- и используют в качестве компонентов реакции молекулы Н2О и ионы Н+ и ОН-. Слабые электролиты и малорастворимые вещества записывают в молекулярном виде.
Чтобы составить уравнение окислительно-восстановительной реакции ионно-электронным методом необходимо соблюдать следующие правила:
1) Составить схему реакции, указав в левой части уравнения формулы веществ взятых для реакции, а в правой – полученных. Например:
Mn(NO3)2 + PbO2 + HNO3 → HMnO4 + Pb(NO3)2 + H2O
2) Составить ионную схему реакции, руководствуясь общими правилами составления ионных уравнений: сильные электролиты записать в виде ионов, а неэлектролиты, слабые электролиты, осадки и газы в виде молекул. Не изменяющиеся в результате реакции ионы в виде молекул. Не изменяющиеся в результате реакции ионы в ионную схему не включаются:
Mn2+ + PbO2 + → HMnO4 + Pb2+ … (кислая среда)
3) Составить частные электронно-ионные уравнения /полуреакции/ отдельно для процесса окисления и отдельно для процесса восстановления, руководствуясь следующим:
а) если прлдукты реакции содержат больше кислорода, чем исходные соединения, то недостающее количество кислорода пополняется в кислых и нейтральных растворах за счет воды, а в щелочных растворах – за счет гидроксид-ионов ОН-,
б) если продукты реакции содержат меньше кислорода, чем исходные вещества, то освобождающийся кислород в кислой среде реагирует с ионами водорода с образованием очень слабо диссоциирующих молекул воды, а в нейтральной среде и щелочной среде – за счет добавления воды с образованием гидроксид-ионов.
4) В каждой полуреакции подвести баланс вещества /уравнять число атомов или ионов/, а также уравнять алгебраическую сумму зарядов правой и левой части частных электронно-ионных уравнений:
Окисление: Восстановление
а/ Mn2+ → MnO4- а/ PbO2 → Pb2+
б/ Mn2+ + 4 H2O→ MnO4- + 8 H+ б/ PbO2 + 4 Н+ → Pb2+ + 2 H2O
в/ Mn2+ + 4 H2O – 5е → MnO4- + 8 H+ в/ PbO2 + 4 Н+ + 2е → Pb2+ + 2 H2O
5) Подвести баланс зарядов и вывести коэффициенты:
Mn2+ + 4 H2O – 5е → MnO4- + 8 H+ /окисление/ │2
PbO2 + 4 Н+ + 2е → Pb2+ + 2 H2O /восстановление/ │5
6) Для достижения электронного баланса умножить первое полууравнение на 2, а второе полууравнение на 5, а затем суммировать полуреакции:
2 Mn2+ + 8 H2O + 5 PbO2 + 20 H+ → 2 MnO4- +16 H+ + 5 Pb2+ + 10 H2O
7) Произвести возможные упрощения /приведение подобных членов/ в предыдущем уравнении и получить ионное уравнение в сокращенном виде:
2 Mn2+ + 5 PbO2 + 4 Н+ → 2 MnO4- + 5 Pb2++ 2 H2O
8) руководствуясь схемой реакции, приписать недостающие ионы и написать уравнение уже в молекулярном виде:
2 Mn(NO3)2 + 5PbO2 + 6HNO3 = 2HMnO4 + 5Рb(NO3)2 + 2 H2O
9) Подвести окончательный баланс с учетом прибавившихся ионов, при этом могут уточниться некоторые коэффициенты /например, 6HNO3/.
Методы оксидиметрии
Оксидиметрия – это методы количественного определения восстановителей или окислителей. При помощи титрованных растворов окислителей определяют количественное содержание восстановителей. При помощи титрованных растворов восстановителей определяют окислители. В зависимости от вещества, применяемого в качестве рабочего раствора, метод оксидиметрии подразделяется на несколько видов: перманганатометрия, иодометрия, хроматометрия и др.
Индикаторы, применяемые в методах оксидиметрии, различны. Часто это органические вещества, которые сами являются окислителями или восстановителями. Иногда это специфические реактивы, например, крахмал в иодометрии. Перманганатометрические определения производят без индикатора.
Перманганатометрией называется такой вид оксидиметрии, в котором в качестве рабочего раствора применяют перманганат калия KMnO4. Он является сильным окислителем, особенно в кислой среде. В зависимости от кислотности среды при восстановлении KMnO4 получаются различные конечные продукты.
В кислой среде ионы MnO4- восстанавливаются до бесцветных ионов Mn2+:
MnO4- + 5е + 8 Н+ → Mn2+ + 4Н2О
В слабощелочной и нейтральной среде оны MnО4- восстанавливаются до темного осадка MnO2, где марганец четырехвалентен. Этот осадок затрудняет определение конца реакции, поэтому титрование проводят в кислой среде. Для подкисления применяют только серную кислоту, так как НСl вступает в окислительно-восстановительную реакцию с перманганатом калия. Азотная кислота для подкисления также в методах оксидиметрии не применяется.
Ионы MnO4- придают раствору красно-фиолетовую окраску, в процессе титрования раствор обесцвечивается. В момент, когда в растворе не остается восстановителя, от прибавления одной капли MnO4- тируемая смесь приобретает розовую окраску. Таким образом, точка эквивалентности фиксируется при помощи самого же рабочего раствора и индикатор в этом методе не применяется.
Для убыстрения реакции титрование рекомендуется проводить в нагретом растворе. Реакция ускоряется также за счет действия катализатора, роль которого выполняют ионы Mn2+, образующиеся в процессе титрования.
Перманганатометрия применяется для анализа ряда лекарственных препаратов, обладающих свойствами восстановителей – пероксида водорода Н2О2, пероксида магния MgO2, нитрата натрия, восстановленного железа. Методом перманганатометрии при клиническом анализе в крови определяется сахар, мочевая кислота, кальций, калий и фермент катализа. Метод нашел также применение в санитарно-гигиеническом анализе при исследовании питьевых и сточных вод.
Иодометрия – это один из методов оксидиметрии, в основе которого лежит реакция выделения или поглощения иода, а рабочими растворами являются растворы J2 и тиосульфата натрия Na2S2O3. В основе метода иодометрии лежат две реакции:
J2 + 2е = 2J-
2J- – 2е = J2
Индикатором является I %-ный раствор крахмала. Иод с крахмалом образует интенсивно синее соединение. В момент эквивалентности, когда восстанавливается весь иод, синяя окраска исчезает и раствор становится бесцветным.
Методом иодометрии определяют как окислители, так и восстановители. Реакции окисления-восстановления в методе иодометрии нельзя проводить в сильно щелочной среде, так как могут возникнуть побочные реакции. Рабочие растворы иода и тиосульфата натрия хранят в темном месте в закрытых склянках, индикатор крахмала используется не более 2-3 дней, если окраска крахмала при добавлении иода становится красно-бурой, раствор непригоден. Раствор крахмала необходимо прибавлять в самом конце титрования, когда титруемый раствор будет иметь светло-желтую окраску, в противном случае раствор легко перетитровать. Все иодометрические определения ведут на холоду, т.к. при нагревании иод может частично улетучиться.
Метод иодометрии нашел широкое применение в анализе неорганических органических лекарственных препаратов. Из неорганических препаратов методом иодометрии анализируют иод, перманганат калия, арсенат натрия каломель, сульфат меди. Многие органические лекарственные препараты – формалин, акрихин, антипирин, анальгин, коразол, аскорбиновая кислота, пенициллин и др. определяют количественно методом иодометрии. В клиническом анализе методом иодометрии пользуются при определении в крови сахара и фермента пероксидазы, в санаторно-гигиеническом анализе – для определения «активного» хлора в хлорной извести, остаточного хлора в хозяйственно-питьевой воде.
Примеры решения задач
Пример 1.
Закончите уравнение реакции и подберите коэффициенты методом электронного баланса: KI + KMnO4 + H2SO4 = I2 + ….
Решение:
1. Дописываем уравнение реакции:
KI + KMnO4 + H2SO4 = I2 + MnSO4 + K2SO4 + H2O.
2. Определяем степени окисления в реагентах и продуктах, находим элементы, которые изменили свои степени окисления:
KI-1 + KMn+7O4 + H2SO4 = I20 + Mn+2SO4 + K2SO4 + H2O.
3. Составляем уравнения электронного баланса:
2I-1 – 2e ® I2 ï 5 восстановитель, окисление;
Mn+7 + 5e ® Mn+2 ï 2 окислитель, восстановление.
4. Проставляем коэффициенты с учетом множителей:
10KI + 2KMnO4 + H2SO4 = 2MnSO4 + 5I2 + K2SO4 + H2O.
5. Подбирают коэффициенты для остальных участников реакции:
10KI + 2KMnO4 + 8H2SO4 = 2MnSO4 + 5I2 + 6K2SO4 + 8H2O.
Пример 2.
Закончите уравнение реакции, подберите коэффициенты методом электронно-ионного баланса, и рассчитайте эквивалентую массу окислителя: NaCrO2 + NaOH + H2O2 → ….
Решение:
1) Допишем продукты реакции: NaCrO2 + NaOH + H2O2 → Na2CrO4 + H2O.
2) Запишем ионную схему реакции: CrO2- + H2O2 → CrO42- + H2O.
3) Составим частные электронно-ионные уравнения /полуреакции/:
Для процесса окисления хромата натрия:
а/ CrO2- → CrO4-;
б/ CrO2- + 4OH → CrO2-4 + 2H2O, /подведение баланса вещества/
в/ CrO2- + 4OH- - 3е → CrO2-4 + 2H2O. /соблюдение равенства зарядов/
Для процесса восстановления пероксида водорода:
Н2О2 + 2е → 2ОН-.
4) Подведем баланс зарядов и выведем коэффициенты:
CrО-2 + 4OH- - 3е → CrO42- + 2H2O, окисление │2;
H2O2 + 2е → ОН-, восстановление │3.
5) Суммируем частные уравнения реакций окисления и восстановления после умножения на соответствующие коэффициенты:
2CrО-2 + 2OH- + 3Н2О2 → 2 CrO42- + 4 H2O.
6) Приведение подобных членов и сокращение:
2CrО-2 + 2OH- + 3Н2О2 → 2CrO42- + 4H2O.
(в данном случае сокращение не требуется)
7) Записываем уравнение реакции в молекулярном виде с учетом полученных коэффициентов:
2NaCrO2 + 2NaOH + 3H2O2 = 2Na2CrO4 + 4H2O
8) Проверяем баланс по элементам в молекулярном уравнении. В данном случае никаких уточнений не требуется.
9) Рассчитаем молярную массу эквивалента окислителя, в данном случае пероксида водорода:
Э = М/z, где М – молярная масса Н2О2, равная 34 г/моль, z – число переносимых электронов.
Э(Н2О2) = 34/2 = 17 г/моль∙экв.
Пример 3.
Напишите уравнения реакций между перманганатом калия и сульфитом калия в кислой, щелочной и нейтральной средах. Уравняйте методом электронно-ионного баланса.
Решение:
а) Кислая среда
KMnO4 + K2SO3 + H2SO4 → MnSO4 + K2SO4 + H2O
MnO4- + SO32- + H+ → Mn2+ + SO42- + H2O
MnO4- + 8H+ + 5е → Mn2+ + 4H2O, восстановление | 2
SO32- + H2O – 2е → SO42- + 2H+ , окисление | 5
2MnO4- + 16 H+ + 5SO32- + 5H2O → 2Mn2+ +5SO42- + 8H2O +10H+
2MnO4- + 6 H+ + 5SO32- → 2Mn2+ +5SO42- + 3H2O
2MnO4 + 5K2 SO3 + 3H2SO4 + 2MnSO4 + 6K2SO4 + 3H2O.
б) Щелочная среда
KMnO4 + K2SO3 + KOH → KMnO4 + K2SO3 + H2O
MnO4- + SO32 + OH- → MnO4- + SO42 + H2O
MnO4- + е → MnO42-, восстановление | 2
SO32- + 2OH- - 2е → SO42- + H2O, окисление | 1
2MnO4- + SO32 + 2OH- → 2MnO4- + SO42 + H2O
2KMnO4 + K2SO3 + 2KOH = 2K2MnO4 + K2SO4 + H2O.
в) Нейтральная среда
KMnO4 + K2SO3 + H2O → MnO2 + К2SO4 + КOН
MnO4- + SO32- + H2O → MnO2 + SO42- + OH-
MnO4- + 2H2O + 3е → MnO2 + 4OH-, восстановление | 2
SO32- + 2OH- - 2е → SO42- + 2H2O, окисление | 3
2MnO4- + 4H2O + 3SO32- → 2MnO2 + 8H2O- + 3SO42- + 2H2O
2MnO4- + 3SO32- + H2O → 2MnO2 + 3SO42- + 2OH-
2KMnO4 + 3K2SO3 + H2O → 2MnO2 +3К2SO4 + 2КOН
Пример 4.
В каком направлении в стандартных условиях будет протекать реакция: КСl + Br2 = KBr + Cl2? j (Br20/2Br-) = +1,09В, j (Cl20/2Cl-) = +1,36В.
Решение: Для определения направления реакции рассчитаем ее ЭДС. Для этого определим, что является окислителем, а что является восстановителем:
КСl-1 + Br20 = KBr-1 + Cl20; Сl-1 – отдает свои электроны, следовательно, является восстановителем, Br2 – окислителем.
ЭДС рассчитываем по формуле: ∆E0 = j0ок-ля – j0вос-ля = 1,36 – 1,09 = 0,28 > 0. Т.к. ЭДС реакции больше нуля, то она протекает самопроизвольно в прямом направлении.
Ответ: реакция протекает самопроизвольно в прямом направлении.
Пример 5.
Рассчитайте молярную концентрацию нитрита натрия, если на титрование 20 мл его раствора, пошло 12,5 мл 0,01 М раствора дихромата калия в кислой среде.
Решение: Для определения концентрации нитрита натрия воспользуемся законом эквивалентов: nэкв(ox) = nэкв(red) или СN(OX)VOX = СN(RED)VRED.
Для расчета нормальной концентрации дихромата калия запишем уравнение протекающей реакции и уравнения полуреакций:
NaN+3O2 + K2Cr+62O7 + H2SO4 ® Cr+32(SO4)3 + NaN+5O3 + H2O + K2SO4;
N+3 – 2e ® N+5
2Cr+6 + 6e ® 2Cr+3
Рассчитаем нормальную концентрацию K2Cr2O7:
СN = СМ ×z,
где z – число переносимых электронов.
СN(K2Cr2O7) = 0,01× 6 = 0,06 моль×экв/л.
Найдем концентрацию нитрата натрия по закону эквивалентов:
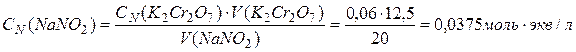 .
.
Перейдем к молярной концентрации нитрата натрия по формуле:
СМ = СN / z = 0,0375/2 = 0,01875 моль/л.
Ответ: 0,01875 моль/л.






