Термодинамічні методи все частіше застосовують для аналізу технологічних процесів.
Велика кількість публікацій присвячена ексергетичному підходу. Порівняно недавно почав розвиватись новий напрям термодинаміки, який має назву – термодинаміка за кінцевого часу і який дозволяє знайти режим процесу заданої інтенсивності, при якому мінімізується ентропія утворення. Тому цікавим є виявити подібність і відмінність цих підходів, що допоможе інженерам та проектувальникам правильно вибирати той чи інший метод термодинамічного дослідження відповідного технологічного процесу.
Подібність в підходах
Основою обох зазначених підходів є визначення і мінімізація втрат енергії, обумовлених незворотністю процесів. При ексергетичному підході вони характеризуються втратами ексергії. Нагадаємо, що ексергією називається максимальна кількість енергії системи, яка може бути перетворена в роботу за фіксованих параметрів оточуючого середовища. Ця максимальна робота виконується в оборотному процесі переходу системи з даного стану в стан рівноваги з середовищем. Необоротність процесу приводить до зменшення виконаної роботи і втратам ексергії  , яка дорівнює різниці ексергії вхідних і вихідних потоків:
, яка дорівнює різниці ексергії вхідних і вихідних потоків:
 (83)
(83)
або з врахуванням того, що ексергія потоку:
E=I - T0S + C (84)
для процесів, які не супроводжуються хімічними чи масообмінними перетвореннями:
 , (85)
, (85)
де I – ентальпія; Т0 – температура оточуючого середовища; S – ен-тропія; С – константа.
В рівнянні (85) величина в перших дужках є різницею енергій вхідних і вихідних потоків, а величина в других дужках – кількість ентропії  , яка виконується внаслідок нерівноважності процесу.
, яка виконується внаслідок нерівноважності процесу.
За відсутності теплообміну з оточуючим середовищем (тепловтрат) і фіксованому об’ємі установки величина в перших дужках перетворюється на нуль і ∆E=T0∆S або для процесу, який встановився, ∆E=T0σ, де ∆E – втрати ексергії за одиницю часу,  – середня швидкість зростання або продукування ентропії, t – час.
– середня швидкість зростання або продукування ентропії, t – час.
При використанні першого (ексергетичного) підходу втрати енергії характеризуються втратами ексергії, при застосуванні другого підходу-продукуванням ентропії. В обох зазначених підходах ці втрати служать для оцінки ефективності процесу. Відомо (і це підтверджується дослідженням балансових співвідношень для речовини енергії і ентропії), що між виробничою ентропією і традиційними показниками ефективності існують монотонні залежності. У випадку зменшення ентропії знижуються потрібні енергетичні витрати, збільшується продуктивність, покращується якість продукції, тому продукована ентропія може бути універсальним критерієм ефективності при обмежених енергетичних затратах.
Обидва підходи дозволяють (хоча і по-різному) вирішувати такі задачі, як визначення граничних можливостей процесу, оцінка ступеня термодинамічної досконалості, встановлення принципової можливості здійснення процесу (виділення відповідної області значень параметрів вхідних і вихідних потоків, в якій процес є нереалізованим), обрахування і аналіз втрат від незворотності для процесу в цілому і його стадій, виявлення перспективних направлень покращення процесу в цілому.
Відмінність підходів
Основна відмінність розглянутих підходів полягає в тому, що в першому випадку реальний процес порівнюється з явно нереальним процесом – оборотнім, тобто як еталон розглядається оборотній процес. В другому випадку еталон для порівняння синтезується: знаходиться режим процесу, при якому мінімізується продукована ентропія (при заданих інтенсивності взаємодії, рівняннях кінетики, коефіцієнтах тепло- і масопереносу). Такий режим будемо називати термодинамічно оптимальним. Фіксація вказаних величин приводить до того, що такий процес не може бути оборотнім, але є найкращим серед відповідних необоротних процесів заданої інтенсивності.
Пояснимо відмінність підходів і спосіб знаходження термодинамічно оптимального режиму на прикладі протитечійного трубчатого теплообмінника, схема потоків якого показана на рис. 70.

Рис. 70. Схема потоків в протитечійному трубчатому теплообміннику
Наприклад. Гарячий потік має початкову температуру Т20, холодний – Т10. Тепловий потік q залежить від поточних значень температур Т1 і Т2, тобто q=q(T1, T2). Ексергетичний метод дозволяє визначити втрати ексергії при заданому режимі теплообміну, коли відомі витрати потоків G1, G2 та їх початкові Т10, Т20 і кінцеві температури  ,
,  :
:
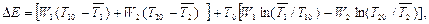
де W1=  G1 і W2=
G1 і W2=  G2 – водяні еквіваленти потоків;
G2 – водяні еквіваленти потоків;  ,
,  – теплоємності потоків. Величина в перших дужках описує тепловтрати, а в других дужках – зміну ентропії потоків.
– теплоємності потоків. Величина в перших дужках описує тепловтрати, а в других дужках – зміну ентропії потоків.
При використанні другого підходу можна знайти режим процесу, тобто такі профілі зміни температур вздовж теплообмінника Т1 (l) і Т2 (l), за яких при заданій інтенсивності теплообміну – кількості тепла Q, яке передається в одиницю часу, тобто за умови, що:
 (86)
(86)
то при заданій початковій температурі одного з потоків і фіксованій кінетиці теплопереносу продукування ентропії під час проходження процесу мінімальне:
 (87)
(87)
При цьому передбачається, що потоки рухаються в режимі ідеального витіснення.
Зміна температури Т2 визначається рівнянням:
 (88)
(88)
Зрозуміло, що для виконання умови (86) рушійна сила повинна бути кінцевою, а величина σ повинна бути більшою за нуль.
Розв’язок задачі (86)–(88) визначає умову, яку повинні задовольняти оптимальні профілі температур Т1 (l) і Т2 (l), а саме: в кожному перерізі l повинна виконуватись рівність:
 , (89)
, (89)
де  – деяка константа, яка знаходиться з використанням умов (86) і (88).
– деяка константа, яка знаходиться з використанням умов (86) і (88).
Зокрема, для лінійного закону теплопередачі:
q=k(T2-T1) (90)
умова термодинамічної оптимальності теплообміну (89) приводить до вимоги сталості відношення температур потоків в будь-якому перерізі теплообмінника:
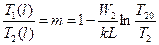 , (91)
, (91)
де k – загальний коефіцієнт теплопередачі на одиниці довжини теплообмінника з врахуванням поверхні теплообміну.
Відповідне заданому режиму мінімально можливе продукування ентропії складає:
 . (92)
. (92)
Метод визначення термодинамічно оптимального режиму можна узагальнити. Нехай в ході процесу відбуваються одночасно декілька взаємодій, наприклад, тепло- і масообмін або декілька хімічних реакцій, при цьому потоки J лінійно залежать від термодинамічних сил:
J=LX, (93)
де J –вектор потоків, X – вектор термодинамічних сил, L – матриця феноменологічних коефіцієнтів.
Задача пошуку потоків, за яких процес заданої інтенсивності (при заданих середніх величинах потоків Jo) супроводжується мінімальним продукуванням ентропії, може бути представлена у вигляді:
 (94)
(94)
або з врахуванням умови (94):
 , (95)
, (95)
де риска зверху означає операцію в часі чи довжині в залежності від поставленого завдання.
Вирішення цього завдання показує, що в оптимальному режимі термодинамічні сили і потоки повинні бути постійними. Продукування ентропії при цьому складає:
 . (96)
. (96)
Ця величина є мінімально можливою при заданій інтенсивності, оскільки знаходиться без врахування обмежень, які визначають можливість реалізації оптимальних потоків (обмежень на витраті вхідних потоків, початкові і кінцеві значення температур тощо)
Таким чином, кожен процес при заданій інтенсивності супроводжується неминучим продукуванням ентропії, мінімально можлива величина якої (що відповідає термодинамічно оптимальному режиму) може бути знайдена. До такого термодинамічно оптимального процесу потрібно наближати реальний процес (по ньому доцільно визначати граничні можливості процесу). Шляхом порівняння з таким режимом (наприклад, по відношенню мінімально можливого продукування ентропії до фактичного: η = σmin / σ) бажано оцінювати термодинамічну досконалість процесу. Для виділення області принципової нездійсненності процесу заданої інтенсивності резонно використовувати умову σ > σmin, а не σ > 0. При порівнянні стадій процесу слід знаходити не втрати ексергії на і -тій стадії, а – коефіцієнти η1 або різницю  і, виходячи з цього, вибирати шляхи покращення процесу. В пошуку реальних керуючих впливів (витрат, температур, концентрацій вхідних потоків) слід враховувати термодинамічно оптимальні закони зміни потоків. Відмітимо, що в ряді випадків – наприклад, при протитечійному теплообміні з лінійним законом тепловіддачі (92) – термодинамічно оптимальний режим може бути реалізований таким чином: величина
і, виходячи з цього, вибирати шляхи покращення процесу. В пошуку реальних керуючих впливів (витрат, температур, концентрацій вхідних потоків) слід враховувати термодинамічно оптимальні закони зміни потоків. Відмітимо, що в ряді випадків – наприклад, при протитечійному теплообміні з лінійним законом тепловіддачі (92) – термодинамічно оптимальний режим може бути реалізований таким чином: величина  доведена до одиниці. Величина σmin залежить від поверхонь контактів, а отже – від розмірів апарата. Це дозволяє пов’язати і врахувати одночасно капітальні і експлуатаційні витрати.
доведена до одиниці. Величина σmin залежить від поверхонь контактів, а отже – від розмірів апарата. Це дозволяє пов’язати і врахувати одночасно капітальні і експлуатаційні витрати.
Продовжуючи порівняння зазначених підходів, необхідно відмітити, що в хімічних процесах ексергії потоків залежать від вибору точок відліку, які містяться в оточуючому середовищі. Це може привести до умовностей і неоднозначностей та ускладнює розрахунок, який часто проводиться за емпіричними формулами або з використанням спеціальних таблиць. Продукування ентропії не залежить від параметрів оточуючого середовища і визначається організацією самого процесу.
На закінчення вкажемо деякі результати, які були отримані при використанні зазначеного підходу, що базується на мінімізації продукованої ентропії. Для теплових машин, холодильних циклів, теплових насосів (при заданих потужності, коефіцієнтах і поверхнях теплообміну) знайдені граничні значення ККД. Визначені термодинамічно оптимальні цикли двигунів внутрішнього згорання. Знайдені термодинамічно оптимальні режими процесів тепло- і масообміну для схем з різними структурами потоків. Встановлені області можливих значень параметрів вихідних потоків в процесах розділення газових сумішей. Оцінені граничні можливості процесів абсорбційного, адсорбційного, мембранного розділення, ректифікації, хімічної взаємодії тощо.
Таким чином, зазначені методологічні підходи мають загальну основу і не випадково, що при їх використанні рекомендується знижувати втрати від необоротності процесу шляхом вирівнювання рушійних сил і наближення реального процесу до еталонного. Тільки при ексергетичному підході таким еталоном є оборотній процес. При застосуванні іншого підходу такий еталон синтезується з врахуванням інтенсивності процесу, рівнянь кінетики, коефіцієнтів і поверхонь обміну, що дозволяє уточнити розв’язок відповідних задач. Одночасно, при цьому усуваються ускладнення, які пов’язані з розрахунком ексергії для масообмінних і хімічних процесів.
Запитання для самоконтролю
1. Мета й об’єкти виявлення та діагностики несправностей.
2. Які існують види несправностей технологічного устаткування?
3. Основні методи термодинамічного аналізу.
4. Критерії оптимальності та основні вимоги до них.
5. Основні оптимізуючі фактори процесу.
6. Причини виникнення обмеження.
7. Подібність ексергетичного та термодинамічного підходів.
8. Відмінність ексергетичного та термодинамічного підходів.
9. Методи контролю стану обладнання і перебігу процесів.
10. В чому полягає суть діагностики несправностей.






