ИДЕАЛЬНОГО ГАЗА
Основные законы и формулы
· Основное уравнение молекулярно-кинетической теории:
 ,
,
где  – давление газа;
– давление газа; 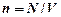 – концентрация молекул;
– концентрация молекул;  – масса одной молекулы;
– масса одной молекулы;  – средняя квадратичная скорость одной молекулы;
– средняя квадратичная скорость одной молекулы;  – плотность газа;
– плотность газа;  – абсолютная температура;
– абсолютная температура;  – постоянная Больцмана.
– постоянная Больцмана.
· Средняя кинетическая энергия поступательного движения одной молекулы
 .
.
· Изопроцессы (газовые законы) для  :
:
1)  – изотермический:
– изотермический:  ;
;
2)  – изобарный:
– изобарный:  ;
;
3)  – изохорный
– изохорный  .
.
· Уравнение Менделеева-Клапейрона:
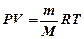 ,
,
где  – объём газа;
– объём газа;  – масса газа;
– масса газа; 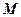 – молярная масса;
– молярная масса;  ) – универсальная газовая постоянная.
) – универсальная газовая постоянная.
· Количество вещества
 ,
,
где  – общее число молекул;
– общее число молекул;  – постоянная Авогадро.
– постоянная Авогадро.
· Скорости молекул:
 – средняя квадратичная,
– средняя квадратичная,
 – средняя арифметическая,
– средняя арифметическая,
 – наиболее вероятная.
– наиболее вероятная.
· Нормальные условия:


 -объём одного моля газа.
-объём одного моля газа.
· Закон распределения молекул идеального газа по скоростям:
 .
.
· Закон распределения молекул идеального газа по энергиям:
 .
.
Задания
5.1. В сосуде объёмом  находится газ при нормальных условиях. Определите число молекул газа в сосуде и концентрацию молекул. [
находится газ при нормальных условиях. Определите число молекул газа в сосуде и концентрацию молекул. [  ].
].
5.2. Газ находится в цилиндре под поршнем при нормальных условиях. Во сколько раз изменится концентрация молекул газа при увеличении объёма газа в 5 раз при прежней температуре? [уменьшится в 5 раз].
5.3. Газ находится в цилиндре под поршнем при нормальных условиях. Во сколько раз изменится концентрация молекул газа при увеличении температуры газа до 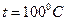 при прежнем давлении? [уменьшится в 1,37 раза].
при прежнем давлении? [уменьшится в 1,37 раза].
5.4. В баллоне находилось 10 кг газа при давлении  Найдите, какое количество газа взяли из баллона, если окончательное давление стало равно
Найдите, какое количество газа взяли из баллона, если окончательное давление стало равно  Температуру газа считать постоянной. [7,5 кг].
Температуру газа считать постоянной. [7,5 кг].
5.5. 12 г газа занимают объём  при температуре
при температуре  . После нагревания газа при постоянном давлении его плотность стала равна
. После нагревания газа при постоянном давлении его плотность стала равна  До какой температуры нагрели газ? [1400 К].
До какой температуры нагрели газ? [1400 К].
5.6. В баллоне объёмом 10 л находится гелий ( ) под давлением 1 МПа и при температуре 300 К. После того как из баллона было взято 10 г гелия, температура в баллоне понизилась до 290 К. Определите давление гелия, оставшегося в баллоне. [0,364 МПа].
) под давлением 1 МПа и при температуре 300 К. После того как из баллона было взято 10 г гелия, температура в баллоне понизилась до 290 К. Определите давление гелия, оставшегося в баллоне. [0,364 МПа].
5.7. В сосуде объёмом  находится 0,02 кг азота (
находится 0,02 кг азота (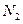 ) под давлением
) под давлением  . Определите среднюю квадратичную скорость молекул газа; число молекул, находящихся в сосуде; плотность газа. [
. Определите среднюю квадратичную скорость молекул газа; число молекул, находящихся в сосуде; плотность газа. [  ].
].
5.8. Плотность некоторого газа  , а средняя квадратичная скорость молекул этого газа равна 600 м/с. Определите давление, которое оказывает газ на стенки сосуда. [600 Па].
, а средняя квадратичная скорость молекул этого газа равна 600 м/с. Определите давление, которое оказывает газ на стенки сосуда. [600 Па].
5.9. Определите среднюю квадратичную скорость молекул некоторого газа, плотность которого при давлении  равна r=0,24 кг/м 3 Какова масса одного моля этого газа, если значение плотности дано при температуре
равна r=0,24 кг/м 3 Какова масса одного моля этого газа, если значение плотности дано при температуре  ? [1172,6 м/с; 0,005 кг/моль].
? [1172,6 м/с; 0,005 кг/моль].
5.10. 6 г углекислого газа ( ) и 5 г закиси азота (
) и 5 г закиси азота ( ) заполняют сосуд объёмом
) заполняют сосуд объёмом  . Найдите общее давление в сосуде при температуре 400 К. [
. Найдите общее давление в сосуде при температуре 400 К. [  ].
].
5.11. Определите молярную массу смеси кислорода ( ) массой 25 г и азота (
) массой 25 г и азота (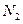 ) массой 75 г. [
) массой 75 г. [  ].
].
5.12. Определите плотность смеси газов водорода ( ) массой 8 г и кислорода (
) массой 8 г и кислорода ( ) массой 64 г при температуре 290 К и при давлении 0,1 МПа. Газ считать идеальным. [
) массой 64 г при температуре 290 К и при давлении 0,1 МПа. Газ считать идеальным. [  ].
].
5.13. Баллон вместимостью 20 л содержит смесь водорода ( ) и азота (
) и азота (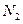 ) при температуре 290 К и давлении 1 МПа. Определите массу водорода, если масса смеси равна 150 г. [ 6,3 г].
) при температуре 290 К и давлении 1 МПа. Определите массу водорода, если масса смеси равна 150 г. [ 6,3 г].
5.14. В закрытом сосуде вместимостью 20 л находятся водород ( ) массой 6 г и гелий (
) массой 6 г и гелий ( ) массой 12 г. Определите давление и молярную массу газовой смеси в сосуде, если температура смеси 300 К. [0,75 МПа; 3.10-3 кг/моль].
) массой 12 г. Определите давление и молярную массу газовой смеси в сосуде, если температура смеси 300 К. [0,75 МПа; 3.10-3 кг/моль].
5.15. Смесь кислорода ( ) и азота (
) и азота (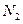 ) при температуре
) при температуре  находится под давлением 230 Па. Масса кислорода составляет 75% от общей массы смеси. Определите концентрацию молекул каждого из газов. [
находится под давлением 230 Па. Масса кислорода составляет 75% от общей массы смеси. Определите концентрацию молекул каждого из газов. [  ].
].
5.16. В сосуде вместимостью 0,3 л при температуре 290 К находится некоторый газ. На сколько понизится давление газа в сосуде, если из-за утечки выйдет  молекул? [133 Па].
молекул? [133 Па].
5.17. Два сосуда одинакового объёма содержат кислород ( ). В одном сосуде давление 2 МПа и температура 800 К, в другом давление 2,5 МПа, а температура 200 К. Сосуды соединили трубкой и охладили находящийся в них кислород до 200 К. Определите установившееся в сосудах давление. [1,5 МПа].
). В одном сосуде давление 2 МПа и температура 800 К, в другом давление 2,5 МПа, а температура 200 К. Сосуды соединили трубкой и охладили находящийся в них кислород до 200 К. Определите установившееся в сосудах давление. [1,5 МПа].
5.18. Определите среднюю кинетическую энергию поступательного движения одной молекулы и температуру газа при давлении 0,5 кПа, если концентрация молекул газа равна  . [
. [  ].
].
5.19. Во сколько раз средняя квадратичная скорость пылинки, взвешенной в воздухе, меньше средней квадратичной скорости молекул воздуха? Масса пылинки  Воздух считать однородным газом, молярная масса которого равна 0,029 кг/моль. [в
Воздух считать однородным газом, молярная масса которого равна 0,029 кг/моль. [в 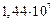 раз].
раз].
5.20. Определите среднюю квадратичную скорость молекулы газа, заключённого в сосуд вместимостью 2 л под давлением 2 кПа. Масса газа 3 г. [4 км/с].
5.21. Определите наиболее вероятную скорость молекул газа, плотность которого при давлении 40 кПа составляет  . [478 м/с].
. [478 м/с].
5.22. Определите наиболее вероятную, среднюю арифметическую и среднюю квадратичную скорости молекул азота (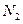 ) при 300 К. [422 м/с; 476 м/с; 517 м/с].
) при 300 К. [422 м/с; 476 м/с; 517 м/с].
5.23. При какой температуре средняя квадратичная скорость молекул кислорода ( ) больше их наиболее вероятной скорости на 100 м/с. [381 К].
) больше их наиболее вероятной скорости на 100 м/с. [381 К].
5.24. Определите среднюю арифметическую скорость молекул газа, если известно, что их средняя квадратичная скорость 1 км/с. [920 м/с].
5.25. Смесь гелия ( ) и аргона (
) и аргона ( ) находится при температуре 1200 К. Определите среднюю квадратичную скорость и среднюю кинетическую энергию поступательного движения атомов гелия и аргона. [гелий: 2730 м/с;
) находится при температуре 1200 К. Определите среднюю квадратичную скорость и среднюю кинетическую энергию поступательного движения атомов гелия и аргона. [гелий: 2730 м/с;  ; аргон: 864 м/с;
; аргон: 864 м/с;  )].
)].
5.26. Используя закон распределения молекул идеального газа по скоростям, найдите формулу наиболее вероятной скорости. [  ].
].
5.27. Используя закон распределения молекул идеального газа по скоростям, найдите среднюю арифметическую скорость молекул. [  ].
].
5.28. Используя закон распределения молекул идеального газа по скоростям, найдите среднюю квадратичную скорость. [  ].
].
5.29. Используя функцию распределения молекул идеального газа по энергиям, найдите среднюю кинетическую энергию молекул. [3/2  ].
].






