Специальные разделы курса
Моносахариды: классификация; стереоизомерия, D– и L–ряды; открытая и циклические формы на примере D–глюкозы и 2–дезокси–D–рибозы, цикло–оксотаутомерия; мутаротация. Представители: D–ксилоза, D–рибоза, D–глюкоза, 2–дезокси–D–рибоза, D–глюкозамин.
Углеводы — гетерофункциональные соединения, являющиеся альдегидо- или кетономногоатомными спиртами или их производными. Класс углеводов включает разнообразные соединения — от низкомолекулярных, содержащих от 3 до 10 атомов углерода до полимеров с молекулярной массой в несколько миллионов. По отношению к кислотному гидролизу и по физико-химическим свойствам они подразделяются на три большие группы: моносахариды, олигосахариды и полисахариды.

Моносахариды (монозы) — углеводы, неспособные подвергаться кислотному гидролизу с образованием более простых сахаров. Монозы классифицируют по числу углеродных атомов, характеру функциональных групп, стереоизомерным рядам и аномерным формам. По функциональным группам моносахариды подразделяются на альдозы (содержат альдегидную группу) и кетозы (содержат карбонильную группу).


По числу углеродных атомов в цепи: триозы (3), тетрозы (4), пентозы (5), гексозы (6), гептозы (7) и т. д. до 10. Наиболее важное значение имеют пентозы и гексозы. По конфигурации последнего хирального атома углерода моносахариды делятся на стереоизомеры D- и L-ряда. В обменных реакциях в организме принимают участие, как правило, стереоизомеры D-ряда (D-глюкоза, D-фруктоза, D-рибоза, D-дезоксирибоза и др.)
В целом название индивидуального моносахарида включает:
• префикс, описывающий конфигурацию всех асимметрических атомов углерода;
• цифровой слог, определяющий число атомов углерода в цепи;
• суффикс - оза — для альдоз и - улоза — для кетоз, причем локант оксо- группы указывают только в том случае, если она находится не при атоме С-2.
Строение и стереоизомерия моносахаридов.
Молекулы моносахаридов содержат несколько центров хиральности, поэтому существует большое число стереоизомеров, соответствующих одной и той же структурной формуле. Так, число стереоизомеров альдопентоз равно восьми (2n, где n = 3), среди которых 4 пары энантиомеров. У альдогексоз будет уже 16 стереоизомеров, т. е. 8 пар энантиомеров, так как в их углеродной цепи содержится 4 асимметрических атома углерода. Это аллоза, альтроза, галактоза, глюкоза, гулоза, идоза, манноза, талоза. Кетогексозы содержат по сравнению с соответствующими альдозами на один хиральный атом углерода меньше, поэтому число стереоизомеров (23) уменьшается до 8 (4 пары энантиомеров).
Относительная конфигурация моносахаридов определяется по конфигурации наиболее удаленного от карбонильной группы хирального атома углерода путем сравнения с конфигурационным стандартом — глицериновым альдегидом. При совпадении конфигурации этого атома углерода с конфигурацией D-глицеринового альдегида моносахарид в целом относят к D-ряду. И, наоборот, при совпадении с конфигурацией L-глицеринового альдегида, считают, что моносахарид принадлежит к L-ряду. Каждой альдозе D-ряда соответствует энантиомер L-ряда с противоположной конфигурацией всех центров хиральности.
(!) Положение гидроксильной группы у последнего центра хиральности справа свидетельствует о принадлежности моносахарида к D-ряду, слева — к L-ряду, т. е. так же, как и в стереохимическом стандарте — глицериновом альдегиде.

Природная глюкоза является стереоизомером D-ряда. В равновесном состоянии растворы глюкозы обладают правым вращением (+52,5º), поэтому глюкозу иногда называют декстрозой. Название виноградный сахар глюкоза получила в связи с тем, что ее больше всего содержится в соке винограда.
Эпимерами называются диастереомеры моносахаридов, различающиеся конфигурацией только одного асимметрического атома углерода. Эпимером D-глюкозы по С4 является D-галактоза, а по С2 — манноза. Эпимеры в щелочной среде могут переходить друг в друга через ендиольную форму, и этот процесс называется эпимеризацией.

Таутомерия моносахаридов. Изучение свойств глюкозы показало:
1) спектрах поглощения растворов глюкозы отсутствует полоса, соответствующая альдегидной группе;
2) растворы глюкозы дают не все реакции на альдегидную группу (не взаимодействуют с NaHSО3 и фуксинсернистой кислотой);
3) при взаимодействии со спиртами в присутствии «сухого» НСl глюкоза присоединяет, в отличие от альдегидов, только один эквивалент спирта;
4) свежеприготовленные растворы глюкозы мутаротируют в течение 1,5–2 часов меняют угол вращения плоскости поляризованного света.

Циклические формы моносахаридов по химической природе являются циклическими полуацеталями, которые образуются при взаимодействии альдегидной (или кетонной) группы со спиртовой группой моносахарида. В результате внутримолекулярного взаимодействия (АN механизм) электрофильный атом углерода карбонильной группы атакуется нуклеофильным атомом кислорода гидроксильной группы. Образуются термодинамически более устойчивые пятичленные (фуранозные) и шестичленные (пиранозные) циклы. Образование этих циклов связано со способностью углеродных цепей моносахаридов принимать клешневидную конформацию.

Представленные ниже графические изображения циклических форм называются формулами Фишера (можно встретить и название «формулы Колли—Толленса»).

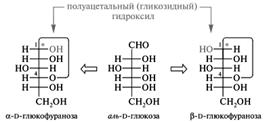
В этих реакциях С1 атом из прохирального, в результате циклизации, становится хиральным (аномерный центр).
Стереоизомеры, отличающиеся конфигурацией атома С-1 альдоз или С-2 кетоз в их циклической форме, называются аномерами, а сами атомы углерода называются аномерным центром.
Группа ОН, появившаяся в результате циклизации, является полуацетальной. Она называется еще гликозидной гидроксильной группой. По свойствам она значительно отличается от остальных спиртовых групп моносахарида.
Образование дополнительного хирального центра приводит к возникновению новых стереоизомерных (аномерных) α- и β-форм. α-Аномерной формой называется такая, у которой полуацетальный гидроксил находится с той же стороны, что и гидроксил у последнего хирального центра, а β-формой — когда полуацетальный гидроксил находится по другую сторону, чем гидроксил у последнего хирального центра. Образуется 5 взаимно друг в друга переходящих таутомерных форм глюкозы. Такой вид таутомерии называется цикло-оксо-таутомерией. Таутомерные формы глюкозы находятся в растворе в состоянии равновесия.
В растворах моносахаридов преобладает циклическая полуацетальная форма (99,99 %) как более термодинамически выгодная. На долю ациклической формы, содержащей альдегидную группу, приходится менее 0,01 %, в связи с этим не идет реакция с NaHSO3, реакция с фуксинсернистой кислотой, а спектры поглощения растворов глюкозы не показывают наличия полосы, характерной для альдегидной группы.
Таким образом, моносахариды — циклические полуацетали альдегидо- или кетоно- многоатомных спиртов, существующие в растворе в равновесии со своими таутомерными ациклическими формами.
У свежеприготовленных растворов моносахаридов наблюдается явление мутаротации — изменения во времени угла вращения плоскости поляризации света. Аномерные α- и β-формы имеют различный угол вращения плоскости поляризованного света. Так, кристаллическая α,D-глюкопираноза при растворении ее в воде имеет начальный угол вращения +112,5º, а затем он постепенно уменьшается до +52,5º. Если растворить β,D-глюкопиранозу, ее начальный угол вращения + 19,3º, а затем он увеличивается до +52,5º. Это объясняется тем, что в течение некоторого времени устанавливается равновесие между α- и β-формами: 2/3 β-формы → 1/3 α-формы.
Предпочтительность образования того или другого аномера во многом определяется их конформационным строением. Наиболее выгодной для пиранозного цикла является конформация кресла, а для фуранозного цикла — конверта или твист -конформация. Наиболее важные гексозы — D-глюкоза, D-галактоза и D-манноза — существуют исключительно в конформации 4С1. Более того, D-глюкоза из всех гексоз содержит максимальное число экваториальных заместителей в пиранозном цикле (а ее β-аномер — все).


У β-конформера все заместители находятся в наиболее выгодном экваториальном положении, поэтому этой формы в растворе 64 %, а α-конформер имеет аксиальное расположение полуацетального гидроксила. Именно α-конформер глюкозы содержится в организме человека и участвует в процессах метаболизма. Из β-конформера глюкозы построен полисахарид — клетчатка.
Формулы Хеуорса. Циклические формулы Фишера удачно описывают конфигурацию моносахаридов, однако они далеки от реальной геометрии молекул. В перспективных формулах Хеуорса пиранозный и фуранозный циклы изображают в виде плоских правильных многоугольников (соответственно шести- или пятиугольника), лежащих горизонтально. Атом кислорода в цикле располагается в удалении от наблюдателя, причем для пираноз — в правом углу.

Атомы водорода и заместители (главным образом, группы СH2OH, если таковая имеется, и он) располагают над и под плоскостью цикла. Символы атомов углерода, как это принято при написании формул циклических соединений, не показывают. Как правило, опускают и атомы водорода со связями к ним. Связи С—С, находящиеся ближе к наблюдателю, для наглядности иногда показывают жирной линий, хотя это не обязательно.
Для перехода к формулам Хеуорса от циклических формул Фишера последнюю необходимо преобразовать так, чтобы атом кислорода цикла располагался на одной прямой с атомами углерода, входящими в цикл. Если преобразованную формулу Фишера расположить горизонтально, как требует написание формул Хеуорса, то заместители, находившиеся справа от вертикальной линии углеродной цепи, окажутся под плоскостью цикла, а те, что были слева, — над этой плоскостью.
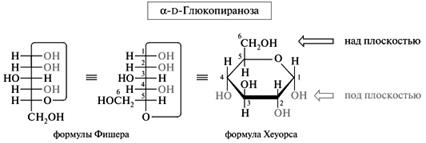
Описанные выше преобразования показывают также, что полуацетальный гидроксил у α-аномеров D-ряда находится под плоскостью цикла, у β-аномеров — над плоскостью. Кроме того, боковая цепь (при С-5 в пиранозах и при С-4 в фуранозах) располагается над плоскостью цикла, если она связана с атомом углерода D-конфигурации, и снизу, если этот атом имеет L-конфигурацию.
Представители.
D-Ксилоза — «древесный сахар», моносахарид из группы пентоз с эмпирической формулой C5H10O5, принадлежит к альдозам. Содержится в эмбрионах растений в качестве эргастического вещества, а также является одним из мономеров полисахарида клеточных стенок гемицелюллозы.
D–Рибоза представляет собой вид простых сахаров, образующих углеводный остов РНК, управляя, таким образом, всеми жизненными процессами. Рибоза также участвует в производстве аденозинтрифосфорной кислоты (АТФ) и является одним из ее структурных компонентов.



2–Дезокси–D–рибоза - компонент дезоксирибонуклеиновых кислот (ДНК). Это исторически сложившееся название не является строго номенклатурным, так как в молекуле содержатся только два центра хиральности (без учета атома С-1 в циклической форме), поэтому это соединение с равным правом может быть названо 2-дезокси-D-арабинозой. Более правильное название для открытой формы: 2-дезокси-D-эритро-пентоза (D-эритро-конфигурация выделена цветом).
D–глюкозамин– вещество, вырабатываемое хрящевой тканью суставов, является компонентом хондроитина и входит в состав синовиальной жидкости.
Моносахариды: открытая и циклические формы на примере D–галактозы и D–фруктозы, фуранозы и пиранозы; a– и β–аномеры; наиболее устойчивые конформации важнейших D–гексопираноз. Представители: D–галактоза, D–манноза, D–фруктоза, D–галактозамин (вопр. 1).
Таутомерные формы фруктозы образуются так же, как и таутомерные формы глюкозы, по реакции внутримолекулярного взаимодействия (АN). Электрофильным центром является атом углерода карбонильной группы у С2, а нуклеофилом — кислород ОН-группы у 5 или 6 атома углерода.

Представители.


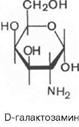
D–галактоза – в животных и растительных организмах, в том числе в некоторыхмикроорганизмах. Входит в состав дисахаридов - лактозы и лактулозы. При окислении образует галактоновую, галактуроновуюи слизевую кислоты.
D–манноза – компонент многих полисахаридов и смешанных биополимеров растительного, животного и бактериального происхождения.
D–фруктоза — моносахарид, кетогексоза, в живых организмах присутствует исключительно D-изомер, в свободном виде — почти во всех сладких ягодах и плодах — в качестве моносахаридного звена входит в состав сахарозы и лактулозы.
Моносахариды: образование простых и сложных эфиров, отношение эфиров к гидролизу; гликозидов (на примере D–маннозы); строение гликозидов, O–,N–,S–гликозиды, отношение гликозидов к гидролизу.
Поскольку циклические формы моносахаридов — это внутренние полуацетали, то при взаимодействии со спиртами, в присутствии безводного хлороводорода, они будут взаимодействовать с одним эквивалентом спирта, образуя полный ацеталь или гликозид. В гликозидах различают сахарную часть (остаток глюкозы) и несахарную часть, остаток спирта, называемую агликоном. Для названия гликозидов характерно окончание - озид.

Гликозиды могут образовываться при взаимодействии со спиртами, фенолами, другими моносахаридами (О-гликозиды); при взаимодействии с аминами, азотистыми основаниями образуются N-гликозиды; существуют и S-гликозиды. Как и все ацетали, гликозиды гидролизуются разбавленными кислотами, проявляют устойчивость к гидролизу в щелочной среде. Гликозидная связь присутствует в полисахаридах, сердечных гликозидах, нуклеотидах, нуклеиновых кислотах.

N-Гликозиды в зависимости от природы азотсодержащего агликона N-гликозиды подразделяются на три типа:
• гликозиламины — соединения, содержащие у аномерного центра аминогруппу или остаток алифатического или ароматического амина;
• гликозиламиды — соединения, в которых гликозильный остаток связан с амидным атомом азота, т. е. фрагментом —NНСОR;
• нуклеозиды — гликозильные производные гетероциклов.
В отличие от О- и N-гликозидов, S-гликозиды не получают прямой конденсацией моносахаридов с тиолами, так как в этом случае образуются преимущественно ациклические дитиоацетали.
Простые эфиры получаются при взаимодействии спиртовых ОН-групп моноз с алкилгалогенидами (метилиодид и др.) Одновременно в реакцию вступает и гликозидный гидроксил, образуя гликозид. Простые эфиры не гидролизуются, а гликозидная связь расщепляется в кислой среде.

Сложные эфиры моносахаридов. Сложные эфиры образуются при взаимодействии моносахаридов с ацилирующими агентами, например, уксусным ангидридом.

В метаболизме моносахаридов важную роль играют сложные эфиры фосфорной кислоты.

В синтетической практике применение находят ацетаты и в меньшей степени бензоаты сахаров. Они используются для временной защиты гидроксильных групп и для выделения и идентификации сахаридов.
Сложные эфиры моносахаридов, подобно всем сложным эфирам, способны гидролизоваться как в кислой, так и в щелочной среде, высвобождая гидроксильные группы. Однако для удаления ацильных групп гидролиз никогда не используется. Более удобной в препаративном отношении является переэтерификация с низшим спиртом (обычно — метанолом), который служит и растворителем. Реакция протекает количественно при комнатной температуре в присутствии каталитических количеств алкоголята или триэтиламина.

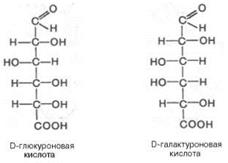
Моносахариды: окисление в гликоновые, гликаровые и гликуроновые кислоты; представители – D–глюконовая, D–глюкуроновая, D–галактуроновая кислоты; аскорбиновая кислота (витамин С).
Глюкоза и другие альдомонозы дают реакции «серебряного зеркала», Троммера, Фелинга (качественная реакция). Эти реакции проводятся в щелочной среде, что способствует смещению таутомерного равновесия в сторону образования открытой формы. В данные реакции вступают не только альдозы, но и кетозы, которые в щелочной среде изомеризуются в альдозы.

Реакция Фелинга является видоизмененной реакцией Троммера (с Cu(OH)2), так как реактив Фелинга представляет собой комплексное соединение Сu2+ с сегнетовой солью (К-, Na-винно-кислый).
CuSO4 + 2 NaOH → Cu(OH)2 + Na2SO4

Комплекс устойчив, при нагревании его синий цвет не изменяется. Однако, если его нагреть в присутствии альдоз, то алкоголят гидролизуется, отщепляя сегнетову соль и Cu(OH)2, который и окисляет моносахарид.
2 Cu(OH)2 → [O] + H2O + 2 CuOH
2 CuOH → H2O + Cu2O
При действии на моносахариды слабых окислителей окисляется только альдегидная группа и образуются гликоновые кислоты. Так, из глюкозы образуется глюконовая кислота, а из галактозы — галактоновая.

При действии сильных окислителей окислению подвергается не только альдегидная группа, но и первичная спиртовая группа. При этом образуются гликаровые (сахарные) кислоты.
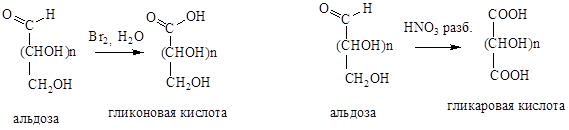
При окислении первичноспиртовой группы у последнего атома углерода альдогексоз без затрагивания альдегидной группы (путем ее защиты переводом в гликозид) образуются уроновые кислоты.

Уроновые кислоты (глюкуроновая, галактуроновая) входят в состав гетерополисахаридов, а также участвуют в детоксикации (связывании в виде гликозидов и выведении с мочой) ряда токсических соединений (фенолов, лекарственных веществ). Уроновые кислоты склонны к декарбоксилированию, в результате которого образуются соответствующие пентозы.
Представители.
D–Галактуроновая кислота (гексуроновая кислота) образуется в организмах окислением первичного гидроксила галактозы до карбоксильной группы. Галактуроновая кислота широко распространена в природе, являясь структурным компонентом ряда высших полисахаридов. Вместе с другими уроновыми кислотами, галактуроновая кислота легко образуется в тканях растений, входит в состав камедей, слизей и др.
Аскорбиновая кислота (витамин С) близка по структуре к моносахаридам и представляет собой g-лактон 2-оксо-L-гулоновой кислоты. Проявляет довольно сильные кислотные свойства (рКа = 4,2), обусловленные ОН-группами ендиольного фрагмента. Аскорбиновая кислота синтезируется растительными и многими животными организмами. Исключение составляют морские свинки, некоторые птицы, обезьяны и человек. Поэтому в организм человека аскорбиновая кислота должна поступать с продуктами питания в количестве 75 мг в сутки. Витамин С является водорастворимым антиоксидантом, а также необходим для синтеза коллагена. При недостатке витамина С развивается цинга.

Аскорбиновая кислота окисляется в мягких условиях, и этот процесс обеспечивает некоторые окислительно-восстановительные реакции в организме, например, окисление α-аминокислоты пролина.







