На основании электронных уравнений составьте уравнение реакции взаимодействия серы с азотной кислотой, учитывая, что сера окисляется максимально, а азот восстанавливается минимально.
Решение.
Определим, какие вещества могут образовываться в результате реакции. Сера в своих соединениях проявляет следующие степени окисления: (–2, +2, +4, +6). Максимальная степень окисления (+6), она реализуется в следующих соединениях: серной кислоте, триоксиде серы и сульфатах. В кислой среде образуется серная кислота.
Для азота характерны степени окисления (–3, +1, +2, +3, +4, +5). В азотной кислоте степень окисления равна (+5), а так как азот восстанавливается минимально, то он принимает один электрон и приобретает степень окисления (+4). Устойчивым соединением азота с такой степенью окисления является NO2.
Электронные уравнения:
6 | S0 – 6 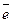 =
=  – окисление,
– окисление,
1 |  +1
+1 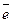 =
=  – восстановление.
– восстановление.
Уравнение реакции взаимодействия серы с азотной кислотой
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O.






