1. Актуальность темы:
Учение о растворах представляет для будущих врачей особый интерес, т.к. большинство важнейших биохимических процессов в живых клетках осуществляется в растворах, т.к. многие биологические жидкости являются водными растворами, содержащими различные неорганические ионы и органические вещества. Так, растворами являются плазма крови, спинномозговая жидкость, лимфа, моча, слюна и др. Значительное количество лекарственных веществ используется в виде жидких лекарственных форм (т.е. растворов). Лекарственные вещества эффективны лишь в растворенном состоянии или должны перейти в растворенное состояние в организме.
Большое значение во многих химических и биологических системах имеет явление осмоса. Благодаря осмосу регулируется поступление воды в клетке и клеточные структуры. Упругость клеток, обеспечивающая эластичность тканей и сохранение определённой формы органов, обусловлена осмотическим давлением. Осмотическое давление крови человека при 37°С составляет 760 кПа. Такое же давление создаёт и раствор хлорида натрия с W = 0,9% - изотонический.
2. Цель обучения:
Изучить теоретические основы учения о неэлектролитах и электролитах; рассмотреть коллигативные свойства растворов: диффузию, осмос, осмотическое давление, понижение температуры замерзания, повышение температуры кипения; решать задачи по коллигативным свойствам растворов неэлектролитов и электролитов.
3. Вопросы для обсуждения:
1. Растворы. Вода как растворитель. Аномальные свойства воды.
2. Растворимость. Факторы, влияющие на растворимость. Термодинамические процессы при растворении.
3. Механизм растворения ионных и молекулярных веществ. Сольватация. Гидратация.
4. Растворимость газов в жидкостях. Законы Генри, Сеченова, Дальтона, их биологическое значение.
5. Понятие об электролитах. Электролитный баланс в организме человека. Основные положения теории электролитической диссоциации.
6. Теории кислот и оснований (Аррениуса, Брёнстеда-Лоури, Льюиса).
7. Коллигативные свойства разбавленных растворов. Диффузия.
8. Осмос, осмотическое давление. Закон Вант-Гоффа для разбавленных растворов электролитов и неэлектролитов. Изотонический коэффициент.
9. Поведение живой клетки в гипо-, гипер-, изотонических растворах (плазмолиз, гемолиз). Осмотическое давление крови, онкотическое давление.
10. Криометрия, эбулиометрия, их применение в медико-биологических исследованиях.
4. Ситуационные задачи:
| № задачи | Текст задания: |
| 1. | Рассчитать осмотическое давление раствора сахарозы при 37С, в котором ёё масса составляет 25,2 г при объёме раствора 200 мл. Определить, является ли этот раствор изотоническим по отношению к крови? |
| 2. | Осмотическое давление крови находится в пределах 740-780 кПа. Рассчитать молярную концентрацию раствора хлорида натрия с массовой долей 0,9%, плотностью 1,01г/см3, предназначенного для введения в организм человека. |
| 3. | При 20 С осмотическое давление раствора в 100 мл которого содержится 6,33 г красящего вещества – гематина равно 243,4 кПа. Определить молярную массу вещества. |
| 4. | Рассчитать при какой температуре должен кристаллизоваться раствор, содержащий в 250 г воды 54 г глюкозы (C6H12O6)? |
| 5. | При какой приблизительно температуре будет кристаллизоваться 40% (по массе) раствор этилового спирта в воде? |
| 6. | При какой приблизительно температуре будет кипеть 50% (по массе) раствор сахарозы (С12H22O11)? |
| № задачи | Эталоны ответов: |
| 1. | По закону Вант-Гоффа для неэлектролитов.
 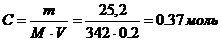  Ответ: Раствор гипертонический.
Ответ: Раствор гипертонический.
|
| 2. | По закону Вант-Гоффа для электролитов.
  

|
| 3. | 
  
|
| 4. | По закону Рауля  , где K – криоскопическая константа K(H2O)=1.86, Cm – моляльная концентрация (число молей растворённого вещества в 1000 г растворителя).
В пересчёте на 1000г воды масса глюкозы составляет 216г , где K – криоскопическая константа K(H2O)=1.86, Cm – моляльная концентрация (число молей растворённого вещества в 1000 г растворителя).
В пересчёте на 1000г воды масса глюкозы составляет 216г
 или по формуле или по формуле 
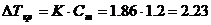
 Раствор глюкозы замёрзнет при температуре –2.23 С
Раствор глюкозы замёрзнет при температуре –2.23 С
|
| 5. |  . В пересчёте на 1000г воды масса этилового спирта составляет 666,6г . В пересчёте на 1000г воды масса этилового спирта составляет 666,6г
 Моляльная концентрация раствора равна
Моляльная концентрация раствора равна 
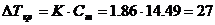 
|
| 6. | В пересчёте на 1000г воды масса сахарозы составляет 1000г
Эбуллиоскопическая постоянная для воды E(H2O)=0.52,
   Раствор сахарозы закипит при t=101.5 С
Раствор сахарозы закипит при t=101.5 С
|
5. Выполнить тестовые задания (письменно):
| 1. | Какой тип химической связи осуществляется между молекулами воды: | |
| А | ионная | |
| В | ковалентная | |
| С | водородная | |
| D | металлическая | |
| 2. | К растворимости какого газа в воде нельзя применить закон Генри: | |
| А | NН3 | |
| В | Cl2 | |
| С | О2 | |
| D | N2 | |
| 3. | Процесс электролитической диссоциации нитрата бария описывается уравненем: | |
| А | Ba(NO3)2 ↔ Ba4+ + 2 NO32- | |
| В | Ba(NO2)2 ↔ Ba2+ + 2 NO2- | |
| С | Ba(NO3)2 ↔ Ba2+ + 2 NO3- | |
| D | Ba(NO3)2 ↔ Ba2+ + NO32- | |
| 4. | К сильным электролитам относится: | |
| А | хлорид серебра | |
| В | сульфит калия | |
| С | гидроксид аммония | |
| D | хлорид натрия | |
| 5. | Выбрать неэлектролиты: | |
| А | С12H22O11 | |
| В | CH3COOH | |
| С | NaCl | |
| D | AgCl | |
| 6. | Какая будет молярная концентрация ионов калия К+ в 0,1 М растворе K2SO4? | |
| А | 2 М | |
| В | 0,2 М | |
| С | 0,1 М | |
| D | 1 M | |
| 7. | Константа диссоциации угольной кислоты H2CO3 может быть записана как: | |
| А | 
| |
| В | 
| |
| С | 
| |
| D | 
| |
| 8. | Произведение растворимости для Ca3(PO4)2 может быть записано как: | |
| А | 
| |
| В | 
| |
| С | 
| |
| D | 
| |
| 9. | В процессе осмоса: | |
| А | молекулы растворенного вещества переходят через мембрану из раствора с большей концентрацией в раствор с меньшей концентрацией. | |
| В | молекулы растворенного вещества переходят через мембрану из раствора с меньшей концентрацией в раствор с большей концентрацией. | |
| С | молекулы растворителя и растворенного вещества переходят через мембрану в различных направлениях, что не приводит к изменению концентрации растворов по разные стороны мембраны. | |
| D | молекулы растворителя переходят через мембрану из раствора с меньшей концентрацией в раствор с большей концентрацией. | |
| 10. | Одинаковое ли осмотическое давление будут иметь растворы сахарозы, калия хлорида, натрия сульфата одинаковой молярной концентрации при одинаковой температуре? | |
| А | Одинаковое | |
| В | Различное | |
| С | Зависит от атмосферного давления | |
| 11. | Для уничтожения бактерий, вызывающих ботулизм, в качестве консерванта используется раствор с высоким содержанием сахара. С чем это связано? | |
| А | С нарушением подвижности бактерий. | |
| В | С явлением плазмолиза. | |
| С | С явлением гемолиза. | |
| 12. | Какие электролиты будут иметь одинаковое осмотическое давление при одинаковой температуре и молярной концентрации. | |
| А | Na2SO4 и NaCl | |
| В | NaCl и KCl | |
| С | CaCl2 и KCl | |
| 13. | Какое осмотическое давление имеют растворы, которые применяются в медицине как изотонические или кровезаменители? | |
| А | 700 – 800 кПа | |
| В | 200 – 300 кПа | |
| С | 300 – 400 кПа | |
| D | 500 – 600 кПа | |
| 14. | Среди водных растворов одинаковых моляльных концентраций наименьшую температуру кипения будет иметь водный раствор: | |
| А | С12Н22О11 | |
| В | MgSO4 | |
| С | Na3PO4 | |
| D | KСl | |
| 15. | Эбуллиоскопия – один из методов определения молярной массы лекарственных веществ. Эбуллиоскопическая постоянная – это: | |
| А | повышение температуры кипения однопроцентного раствора | |
| В | понижение температуры замерзания одномолярного раствора | |
| С | показатель, который характеризует природу растворителя | |
| D | показатель, который характеризует природу растворенного вещества | |
| 16. | Температура кристаллизации раствора | |
| А | всегда выше, чем температура кристаллизации растворителя | |
| В | всегда ниже, чем температура кристаллизации растворителя | |
| С | всегда равна температуре кристаллизации растворителя | |
| D | зависит от полярности растворителя | |
| 17. | При обезвоживании организма происходит: | |
| А | набухание и разрыв клеток (осмотический шок) | |
| В | коллапс клеток (плазмолиз) | |
| С | резкое повышение рН внутриклеточной жидкости | |
| D | клетки находятся в тургоре | |
| 18. | Для купирования приступа глаукомы в качестве дегидратирующего средства используют внутривенные инъекции: | |
| А | 10% раствора хлорида натрия | |
| В | 30% раствора хлорида натрия | |
| С | 0,9 % раствора хлорида натрия | |
| D | 0,1% раствора хлорида натрия | |
| 19. | При лечении гнойных ран в виде компрессов и примочек применяют: | |
| А | 0,05-0,1 % раствор хлорида натрия | |
| В | 0,5-0,8 % раствор хлорида натрия | |
| С | 0,9 % раствор хлорида натрия | |
| D | 3-10% раствор хлорида натрия | |
| 20. | Для промывания верхних дыхательных путей используют: | |
| А | 0,2 % раствор хлорида натрия | |
| В | 0,9 % раствор хлорида натрия | |
| С | 2 % раствор хлорида натрия | |
| D | 20 % раствор хлорида натрия |
6. Решить самостоятельно:
1. Для внутривенных инъекций используют ампулы, содержащие 10 мл водного раствора хлорида кальция с массовой долей 10%. Рассчитать молярную концентрацию этого раствора. Определить массы воды и хлорида кальция, необходимые для изготовления 500 ампул. Плотность указанного раствора при комнатной температуре – 1,09 г\мл.
2. При какой минимальной температуре можно хранить водный раствор с массовой долей новокаина 0,25%, применяемый в хирургии для анестезии, чтобы он не замерзал? Молярная масса новокаина равна 272,8 г\моль.
3. Вычислить осмотическое давление 5% раствора глюкозы. Можно ли данный раствор использовать для внутривенного введения. Ответ пояснить.
4. В 500 мл раствора содержится 9,2 г глицерина. Определить осмотическое давление данного раствора при 00С. Что произойдет с клеткой, имеющей осмотическое давление 7 атм, при попадании в этот раствор?
5. Раствор, содержащий 10 г вещества-неэлектролита в 150 г бензола, замерзает при 2,04°С (температура кристаллизации бензола 5,450С). Определить молекулярную массу растворенного вещества.






