Особливо цікаве рівняння Ван-дер-Ваальса (9.1) тим, що воно якісно відображає головну особливість реальних газів – здатність переходити за певних умов у рідкий стан. Представлення про це виходить, якщо перетворити його в рівняння 3-го ступеня відносно v. Для цього в рів-нянні (9.1) розкриємо в лівій частині дужки:  ;
;

Помноживши обидві сторони рівності на  і розділивши на
і розділивши на  , одержуємо після приведення подібних членів:
, одержуємо після приведення подібних членів:  , (9.2)
, (9.2)
Отримане рівняння має три корені, тобто при заданих параметрах p і Т тут можливі три випадки: один корінь дійсний і два мнимих; усі три корені дійсні і різні; усі три корені дійсні і рівні.
Для виявлення фізичного змісту отриманих висновків розглянемо в системі координат p, v ізотерми, побудовані по рівнянню Ван-дер-Ваальса, для різних температур. (мал. 9.1).

З малюнка видно, що вид ізотерм змінюється в залежності від температури.
Перший випадок має місце при високих температурах, коли ізотерми мають вид гіперболічного характеру (наприклад, лінія 1-2). У цьому випадку кожному тиску відповідає цілком визначений питомий об’єм (наприклад, тиску р  відповідає питомий об’єм v
відповідає питомий об’єм v 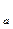 ). Це значення питомого об’єму і є дійсним коренем рівняння (9.1), обоє ж мнимих кореня в цьому випадку фізичного змісту не мають і повинні бути відкинуті. Тіло в цьому випадку при будь-яких
). Це значення питомого об’єму і є дійсним коренем рівняння (9.1), обоє ж мнимих кореня в цьому випадку фізичного змісту не мають і повинні бути відкинуті. Тіло в цьому випадку при будь-яких
Мал.9.1 тисках знаходиться в газоподібному стані. Це так звані надкритичні ізотерми Ван-дер-Ваальсівського газу, тобто ізотерми при Т > T  .
.
Другий випадок має місце при порівняно низьких температурах, коли ізотерми мають два перегини (наприклад, лінія 3-4). Це так звана до критична область, у якої Т < T  . На ізотермах одному значенню тиску р відповідає три значення питомого об’єму (наприклад, тиску р
. На ізотермах одному значенню тиску р відповідає три значення питомого об’єму (наприклад, тиску р  відповідають питомі об’єми v
відповідають питомі об’єми v  , v
, v  , v
, v  ), які і є трьома дійсними і різними коренями рівняння (9.1). Ділянка 3-b відповідає ізотермічному стиску тіла, яке знаходиться в газоподібному стані, причому в крапці b воно вже починає переходити в рідкий стан. Крапка d відповідає такому стану, коли воно вже цілком перетворилося в рідину, у відповідність з чим ділянка d-4 являє собою ізотермічний стиск рідини. Крапка с відповідає проміжному двофазному стану тіла. Ділянка кривої b-f відповідає нестійкому стану переохолодженої пари, а ділянка d-e, також нестійкому стану перегрітої рідини. Що ж стосується ділянки e-f, то вона узагалі фізичного змісту не має, оскільки в дійсності при ізотермічному стиску тіло переходить з газоподібного в рідкий стан при постійному тиску, тобто по горизонтальній лінії b-d.
), які і є трьома дійсними і різними коренями рівняння (9.1). Ділянка 3-b відповідає ізотермічному стиску тіла, яке знаходиться в газоподібному стані, причому в крапці b воно вже починає переходити в рідкий стан. Крапка d відповідає такому стану, коли воно вже цілком перетворилося в рідину, у відповідність з чим ділянка d-4 являє собою ізотермічний стиск рідини. Крапка с відповідає проміжному двофазному стану тіла. Ділянка кривої b-f відповідає нестійкому стану переохолодженої пари, а ділянка d-e, також нестійкому стану перегрітої рідини. Що ж стосується ділянки e-f, то вона узагалі фізичного змісту не має, оскільки в дійсності при ізотермічному стиску тіло переходить з газоподібного в рідкий стан при постійному тиску, тобто по горизонтальній лінії b-d.
Третій випадок має місце при цілком визначеній для кожного тіла температурі, коли т. b і d, зближаючись з підвищенням температури, зливаються в одну т. К, у який має місце перегин відповідної ізотерми, причому дотична до неї в цій крапці має горизонтальний напрямок. Для ізотерми Т=Т  характерна наявність крапки перегину К, у якій питомі об’єми v
характерна наявність крапки перегину К, у якій питомі об’єми v  , v
, v  , v
, v  збігаються, тобто три дійсні корені рівні.
збігаються, тобто три дійсні корені рівні.
Ділянку d-e і f-b на ізотермах можна відтворити експериментально тільки для «чистих» рідин і пар, з яких попередньо вилучене повітря і чисті домішки. Ділянка d-e відповідає метастабільному стану рідини (перегріта рідина). Рідину, з якої вилучені розчинені в ній гази, при спокійному нагріванні без коливань у судині можна перегрівати. Стан перегрітої рідини нестійкий. Найменше збурювання (струшування) викликає скипання і перехід процесу на лінію d-b. Ділянка f-b відповідає метастабільному стану пари (переохолоджена пара). Експериментально його можна одержати, якщо очистити пару від порошин і інших забруднень, навколо яких починають утворюватися крапельки рідини. Конденсація затримується, і пара перенасичується. Стан пари на ділянці f-b також нестійкий. Поява будь-яких центрів конденсації швидко викликає розшарування пари на дві фази, у результаті чого процес переходить на лінію d-b. Крапки на ділянці e-c-f ізотерми експериментально знайти не вдається.
Крапка К зветься критичною крапкою, а відповідні їй параметри р  , v
, v  , Т
, Т  звуться критичними параметрами.
звуться критичними параметрами.
Критична температура, існування якої було відкрито в 1861р. Д.І. Менделєєвим, характеризується тим, що при температурах вище її неможливо шляхом ізотермічного стиску домогтися переходу газу в рідкий стан.
Аналітично умови критичного стану тіла виражаються рівняннями:

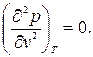 (9.3)
(9.3)
Перше з них показує, що критична ізотерма в т. К має горизонтальну дотичну, друге – що ізотерма має в т.К перегин.
Використовуючи ці рівняння разом з рівняннями стану, можна визначити значення критичних параметрів стану газу.
Стосовно до рівняння Ван-дер-Ваальса, критичні параметри визначаються таким чином:
У рівнянні (9.1) залишимо перемінну р у лівій частині, а перемінну v перенесемо в праву частину: 
Диференціюючи це вираження по v, та вважаючи, що Т=const, і прирівнюючи отримане вираження до нуля:  , (9.4)
, (9.4)
Визначаємо другу похідну і теж прирівнюємо її до нуля:
 , (9.5)
, (9.5)
Для знаходження критичних параметрів варто вирішити спільно три рівняння (9.1), (9.4), (9.5). Представивши два останніх рівняння у виді:

і 
Потім, розділивши перше з них на друге, одержимо:  або
або
2 v = 3 v - 3b; і, отже: 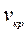 = 3b, (9.6)
= 3b, (9.6)
Підставивши отримане значення в (9.4), одержимо: 
Відкіля:  , (9.7)
, (9.7)
Далі, підставляючи в рівняння (9.1) знайдені значення v  і Т
і Т  , одержуємо:
, одержуємо:
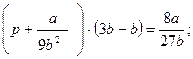 Відкіля:
Відкіля:  (9.8)
(9.8)






