Термін ентропія (від грец. entropia – міра перетворень) введений у 1865 році Клаузіусом.
Поняття про ентропію будується на основі наступних розумінь.
Рівняння 1-го закону ТТД, як відомо має вид:  чи
чи 
У цьому рівнянні  не є повним диференціалом, оскільки в праву частину рівняння входить член
не є повним диференціалом, оскільки в праву частину рівняння входить член  , який не є повним диференціалом, тому що робота є не параметром стану газу, а функцією процесу (тобто щоб проінтегрувати праву частину цього вираження потрібно знати залежність р від v, тобто процес, який робить газ). Унаслідок цього, рівняння не можна проінтегрувати в інтервалі двох довільно обраних станів газу.
, який не є повним диференціалом, тому що робота є не параметром стану газу, а функцією процесу (тобто щоб проінтегрувати праву частину цього вираження потрібно знати залежність р від v, тобто процес, який робить газ). Унаслідок цього, рівняння не можна проінтегрувати в інтервалі двох довільно обраних станів газу.
Як відомо з математики, усякий двочлен можна представити у виді повного диференціала, якщо його помножити на так званий інтегруючий множник. Таким інтегруючим множником для елементарної кількості теплоти  є 1/Т, тобто одержуємо:
є 1/Т, тобто одержуємо:
 , (3.19)
, (3.19)
Рівняння (3.19) можна представити в іншому виді:
 , так як
, так як  а р/Т=R/ v, (3.20)
а р/Т=R/ v, (3.20)
Вираження (3.20) говорить про те, що  являє собою повний диференціал деякої функції S (тобто
являє собою повний диференціал деякої функції S (тобто  =S) є параметром стану газу, оскільки вона залежить тільки від двох параметрів газу і тому не залежить від того яким шляхом газ з одного стану перейшов в інший. Цей параметр стану газу зветься ентропією газу і позначається через S і має розмірність Дж/К.
=S) є параметром стану газу, оскільки вона залежить тільки від двох параметрів газу і тому не залежить від того яким шляхом газ з одного стану перейшов в інший. Цей параметр стану газу зветься ентропією газу і позначається через S і має розмірність Дж/К.
Ентропію, віднесену до 1 кг газу звуть питомою ентропією газу, позначається s і виміряється в Дж/кг К.
Проінтегрував обидві частини рівності (3.20) по будь-якому шляху переходу зі стану 1 у стан 2, одержимо:  , (3.21)
, (3.21)
Зі сказаного випливає, що ентропія є функція будь-якої пари параметрів стану:
S = f1 (p,T); S = f2 ( ,T); S = f3 (p,
,T); S = f3 (p,  ); S = f4 (u,
); S = f4 (u,  ); S = f5 (h, T); і т.д.
); S = f5 (h, T); і т.д.
Таким чином ентропію можна визначити із рівнянь I-го закону ТТД.
 ;
; 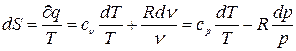

 ,(3.22)
,(3.22)
В оборотних процесах dS і  мають однаковий знак, тому що Т має тільки позитивний знак. Тоді при підведенні теплоти до робочого тіла
мають однаковий знак, тому що Т має тільки позитивний знак. Тоді при підведенні теплоти до робочого тіла  > 0 ентропія збільшується, при відводі теплоти
> 0 ентропія збільшується, при відводі теплоти  < 0 - ентропія зменшується, у процесі без відводу і підведення теплоти
< 0 - ентропія зменшується, у процесі без відводу і підведення теплоти  = 0 (адіабатний процес) ентропія залишається постійної dS = 0.
= 0 (адіабатний процес) ентропія залишається постійної dS = 0.
Таким чином по характеру зміни ентропії можна судити про напрямок процесу переносу теплоти.
З (3.21) випливає, що кількість теплоти, яка брала участь у тім чи іншому ТД процесі при зміні стану робочого тіла від стану 1 до стану 2 можна виразити таким чином:
 , (3.23)
, (3.23)
Теплова T, S – діаграма
Поняття ентропії дозволяє ввести надзвичайно зручну для ТД розрахунків T,S – діаграму, на якій (як і на p, v – діаграмі) стан ТД системи зображується крапкою, а рівноважний ТД процес – лінією, мал.3.3.
Любий оборотний ТД процес, зображений у p, v – діаграмі, може бути перенесений у T, S – діаграму. Для цього треба знати рівняння процесу f (p, v)=0 і залежність S=f (p, v) ентропії від параметрів стану p і v.
 Для відшукання крапки процесу на діаграмі по рівнянню стану і відомих значеннях v і p визначають температуру Т та значення ентропії S.
Для відшукання крапки процесу на діаграмі по рівнянню стану і відомих значеннях v і p визначають температуру Т та значення ентропії S.
T, S – діаграма дає представлення про кількість теплоти, підведеної чи відведеної до робочого тіла в процесі у виді площі під процесом (пл.1-2-2  -1
-1  ). Це випливає з рівняння
). Це випливає з рівняння  .
.
По T, S – діаграмі можна судити також про напрямок теплообміну між джерелом теплоти і робочим тілом.
Як вже відзначалося, напрямок теплового потоку повинний збігатися з алгебраїчним знаком dS, тому що абсолютна температура Т – завжди позитивна величина. Таким чином, оборотний процес зі збільшенням ентропії йде з підведенням
Мал.3.3 теплоти, а оборотний процес зі зменшенням ентропії йде з відводом теплоти від робочого тіла.
Рівняння Майєра
Відповідно до 1-го закону ТТД для закритих систем маємо:  , (3.24)
, (3.24)
З урахуванням співвідношення (3.4.а) і (3.24) маємо:
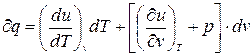 , (3.25)
, (3.25)
Для ізохорного процесу (v = const) це рівняння приймає вид:
 , з огляду на те, що
, з огляду на те, що  , одержимо:
, одержимо:
 , (3.26)
, (3.26)
т.ч. ізохорна теплоємність тіла дорівнює частинної похідної від його внутрішньої енергії по температурі і характеризує темп росту внутрішньої енергії в ізохорному процесі з ростом температури.
Для ізобарного процесу (p=const) з рівняння (3.25) і  одержуємо (підставляючи значення
одержуємо (підставляючи значення  з рівняння (3.25) у вираження
з рівняння (3.25) у вираження  :
:
 , (3.27)
, (3.27)  , (3.28)
, (3.28)
Це рівняння показує зв'язок між  і
і  . Для ідеального газу воно значно спрощується. Дійсно, внутрішня енергія ідеального газу визначається тільки його температурою і не залежить від об’єму, тому
. Для ідеального газу воно значно спрощується. Дійсно, внутрішня енергія ідеального газу визначається тільки його температурою і не залежить від об’єму, тому  і крім того, з рівняння Клапейрона випливає:
і крім того, з рівняння Клапейрона випливає:  відкіля
відкіля 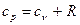 , (3.29)
, (3.29)
Це співвідношення зветься рівнянням Майєра і є одним з основних у ТТД.
Множачи всі члени рівняння (3.29) на молекулярну масу 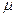 в результаті одержимо:
в результаті одержимо:
 кДж/кмоль К, (3.30)
кДж/кмоль К, (3.30)
З цього рівняння видно, що для ідеальних газів різниця мольних теплоємкостей є величина постійна, рівна універсальній газовій постійній.
ЛЕКЦІЯ 4






