Термодинамічною системою називають сукупність матеріальних тіл, (а також полів), які знаходяться у механічній і тепловій взаємодії, а також обмінюються один з одним речовиною.
Термодинамічна система має границі, які відокремлюють її від навколишнього середовища. Тіла, не вхідні в термодинамічну систему, звуться навколишнім середовищем.
Термодинамічну систему відокремлюють від навколишнього середовища контрольною поверхнею або оболонкою.
У самому загальному випадку система може обмінюватися із навколишнім середовищем речовиною (масообмінні взаємодії) і здійснювати теплові взаємодії, які містять у собі передачу теплоти між окремими тілами системи і між системою і навколишнім середовищем. Така система зветься відкритою.
Системи, у яких обмін речовин не відбувається, звуться закритимисистемами .
Система, яка не може обмінюватися теплотою з іншими системами (навколишнім середовищем) зветься теплоізольованою, або адіабатною .
Система, яка не обмінюється з зовнішнім середовищем або з іншими системами ні енергією, ні речовиною, називається ізольованою чи замкнутою.
Обмін енергією у формі теплоти або роботи здійснюється між макроскопічними тілами, які прийнято називати робочими тілами. Звичайно, це пари і гази.
Термодинамічні параметри стану
Властивості кожної термодинамічної системи характеризуються величинами, які прийнято називати термодинамічними параметрами стану. До них відносяться: абсолютна температура, абсолютний тиск, питомий об’єм, внутрішня енергія, энтальпия й ентропія. Перші три є основними.
Термічні параметри стану
Абсолютна температура, (Т) характеризує тепловий стан тіла, або, як іноді говорять, ступінь нагріву тіла.
З погляду молекулярно-кінетичної теорії температура є мірою інтенсивності теплового руху молекул, її чисельна величина однозначно зв'язана з величиною середньої кінетичної енергії молекул речовини. Для ідеального газу ця функціональна залежність визначається з рівняння
 , (1.1)
, (1.1)
де m - маса молекули; Т - абсолютна температура, К; k - постійна Больцмана, рівна 1,38054×10- Дж / К;  - середня квадратична швидкість поступального руху молекул,
- середня квадратична швидкість поступального руху молекул,
 c1, c2, cn - швидкості окремих молекул, що утворюють газ.
c1, c2, cn - швидкості окремих молекул, що утворюють газ.
З (1.1) видно, що абсолютна температура завжди позитивна, а нульове значення її відповідає стану повного спокою молекул.
У системі СІ одиницею виміру температур є градус Кельвіна (К).
В даний час приймаються і шкали Цельсія оС, Фаренгейта оF, Реомюра oR, Ранкіна oRa.
Абсолютний тиск, (p) обумовлений взаємодією молекул робочого тіла з поверхнею, чисельно дорівнює силі, яка діє на одиницю площі поверхні тіла по нормалях до останнього.
Кінетична теорія газу зв'язує тиск тіла, який знаходиться в рівновазі, наприклад газу або рідини, безпосередньо із середньою кінетичною енергією mc2/2 поступального руху молекул тіла і середнім числом їх n в одиниці об'єму, тобто розглядає р, як статистичну величину.
 , (1.2)
, (1.2)
де n - число молекул в одиниці об'єму; a - коефіцієнт стискальності.
Розрізняють атмосферний, чи барометричний тиск рб; абсолютний тиск ра, манометричний, чи надлишковий ризб тиск, розрідження, або вакуум рвак.
Слід зазначити, що параметром стану є абсолютний тиск. Саме він входить у термодинамічні рівняння.
ра = рнад.+ ратм; ра = ратм. – рвак., (1.3)
У системы СІ розмірність абсолютного тиску є Па = Н / м2. В данний час зустрічаються і позасистемні одиниці вимірювання: ат, атм, мм рт. ст., мм вод. ст.
 Питомий об’єм – фізична величина, рівна відношенню об’єму речовини до його маси V = V / m, (1.4)
Питомий об’єм – фізична величина, рівна відношенню об’єму речовини до його маси V = V / m, (1.4)
Величина, зворотна питомому об’єму, називається густиноюречовини і являє собою масу 1 м3 робочого тіла.  , (1.5)
, (1.5)
Термічні коефіцієнти
Мал. 1.1
Як відомо, кожний з основних параметрів стану системи р, v, T є функцією інших її параметрів:  ;
; 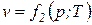 ;
; 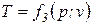 , (1.6)
, (1.6)
Рівняння (1.6) стану в диференціальній формі мають вид:
 ;
; 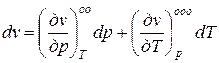 ;
;
 , (1.7)
, (1.7)
У рівняння (1.7) входить шість часток похідних, які попарно оборотні одна одній, наприклад: 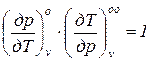 ;
; 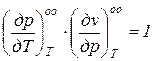
 , (1.8)
, (1.8)
Коефіцієнти при диференціалах dp, dТ, dv у рівняннях (1.7) називають термодинамічними характеристиками робочого тіла. Із шести часток похідних ( /дТ)v, (дv/
/дТ)v, (дv/  )T, (дv/дТ)p, (дТ/
)T, (дv/дТ)p, (дТ/  )v, (
)v, ( /дv)T, (д/дv)p, приймають самостійний сенс.
/дv)T, (д/дv)p, приймають самостійний сенс.
У якості незалежних вибирають часткові похідні: 
Часткова похідна (дv/  )T характеризує інтенсивність зміни об’єму при зміні тиску в умовах постійної температури. Відношення цієї величини до початкового об’єму газу Vо, узяте зі зворотним знаком, називається коефіцієнтом стиску, тобто:
)T характеризує інтенсивність зміни об’єму при зміні тиску в умовах постійної температури. Відношення цієї величини до початкового об’єму газу Vо, узяте зі зворотним знаком, називається коефіцієнтом стиску, тобто:
 , (1.9)
, (1.9)
Термічний коефіцієнт (дv/дТ)p характеризує інтенсивність збільшення об’єму при нагріванні при постійному тиску. Відношення цієї величини до початкового об’єму Vо, узяте зі зворотним знаком, називають коефіцієнтом об'ємного розширення, тобто  , (1.10)
, (1.10)
Термічний коефіцієнт ( /дТ)v характеризує інтенсивність зміни тиску при ізохорному нагріванні тіла. Відношення цієї величини до початкового тиску pо, називають коефіцієнтом тиску або коефіцієнтом термічної пружності, тобто
/дТ)v характеризує інтенсивність зміни тиску при ізохорному нагріванні тіла. Відношення цієї величини до початкового тиску pо, називають коефіцієнтом тиску або коефіцієнтом термічної пружності, тобто
 , (1.11)
, (1.11)
Ці коефіцієнти зв'язані між собою в такий спосіб:
 , (1.12) або
, (1.12) або  , (1.13)
, (1.13)
Далі, з огляду на те, що  ;
;  ;
; 
знаходимо:  , (1.14)
, (1.14)
або остаточно:  або
або  , (1.15)
, (1.15)






