Менделеев-Клапейрон теңдеуіндегі ыдыс қабырғаларының газға келтірілген p қысымы сыртқы қысым болып табылады. Нақты газ молекулаларының өзара тартылу күштерінің әсері газдың қосымша сығылуына
әкеледі, яғни қосымша p ¢ ішкі қысымды туғызады. Сондықтан реал газдың
шын мәніндегі қысымы p –дан жоғары және p + p ¢–ға тең. Сонда
(p + p ¢)(VM - b) = RT
p ¢~ 2, ал газдың тығыздығы V көлемге кері пропорционал, сондықтан
 p ¢= a
p ¢= a
|
M
Олай болса бір моль газ үшін Ван-дер-Ваальс теңдеуі:
æ
ç p +
ö
|
- b) = RT

|
è M ø
Газдың кез келген m массасы үшін Ван-дер-Ваальс теңдеуі:
|
|
p +
ö
|
- m b ö=
m RT.
|
|
|
|
|
M ø M
Теңдеудегі a және b - әр газ үшін тұрақты шамалар. Оларды тәжірибе жүзінде анықтауға болады.
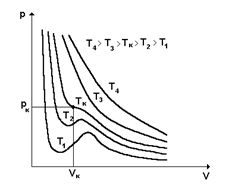 Ван-дер-Ваальс изотермалары.
Ван-дер-Ваальс изотермалары.
Ван-дер-Ваальс теңдеуін VM
–ға қатысты
жазайықта оның pV -координатадағы графиктерін әр түрлі температура үшін тұрғызайық. (сурет)
pV 3 - (pb + RT) V 2 + aV
- ab = 0
М M M
Эндрюс тәжірибесі
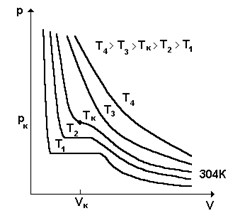 Ван-дер-Ваальс изотермалары тәртібінің физикалық мағынасын анықтау үшін ағылшын химигі Эндрюстің 1869ж. қойған тәжірибесінің нәтижелерін пайдаланған жөн. Эндрюс көмірқышқыл газдың изотермаларын зерттеген.
Ван-дер-Ваальс изотермалары тәртібінің физикалық мағынасын анықтау үшін ағылшын химигі Эндрюстің 1869ж. қойған тәжірибесінің нәтижелерін пайдаланған жөн. Эндрюс көмірқышқыл газдың изотермаларын зерттеген.
Тәжірибелік изотермалардың горизонталь аймақтары тұрақты қысымда өтетін газдың сұйық күйге айналу кезеңіне сәйкес келеді. Басқаша айтқанда, осы аймақта екі фаза - сұйық және газ - бірдей тіршілік етеді.
Өз сұйығымен динамикалық тепе-теңдікте болатын бу қаныққан бу деп аталады.
Қысымның сол жағдайдағы мәні қаныққан бу қысымы деп аталады.
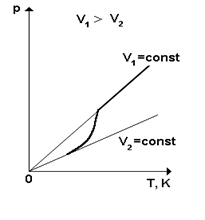
Қаныққан бу қысымы көлемге тәуелсіз. Қаныққан бу қысымының температураға тәуелділігі төмендегі суретте көрсетілген
Ауадағы су буының мөлшері ауаның ылғалдылығы деп аталады.
Ауаның абсолют ылғалдылығы дегеніміз ауа құрамындағы су буының парциал қысымы (Па).
Берілген температурада ауа құрамындағы су буының
pH O
парциал
p 0 қысымына, пайызбен
өрнектеліп алынған қатынасы, ауаның салыстырмалы ылғалдылығы деп аталады:
pH O
= 2 ×100%
p 0
Кризистік параметрлер
Берілген газ үшін кейбір Tк
температурадан жоғары теапературадағы газды
сығу арқылы сұйыққа айналдыру мүмкін емес. Сол температураны кризистік температура деп атайды. Сонда бу дегеніміз кризистік температурадан төмен температурадағы газ.
Кризистік температурадағы нақты газдың изотермасындағы К бүгілу
нүктесіне сәйкес келетін көлеммен қысымды Vк
кризистік қысым деп атайды.
кризистік көлем және pк
Газдың кризистік параметрлері a және b түзетулерімен байланысқан:
T = 8 a,
V = 3 b,
p = a.
к 27 bR к к 27 b 2






