1. “отығу Ц тотықсыздану реакци€сы мен алмасу реакци€сының қандай айырмашылығы бар? –еакци€дағы тотықтырғыш пен тотықсыздандырғыш рол≥ қандай?
2. “өмендег≥ реакци€лардың жартылай электронды иондық теңд≥ктер≥н жазып, коэффициенттер≥н қойыңдар:
Cr3+ + NaBiO3 + H + → Cr2O72- +Bi3+ + H2O
1. Co 2+ +NO2- + K+ +H+ → K3 [Co(NO2)6]↓+NO+H2O
2. MnO4-+Cr3++H2O→ MnO(OH)2↓ + Cr2O72- +H+
3. NO3-+Al+OH-+H2O→ NH3+Al(OH)4-
4. Sb2S3↓ + NO3-+H+ → HsbO3↓ +SO42- + NO2 +H2O
5. MnO4-+SO32-+ H+→ Mn2+ + SO42- + H2O
6. MnO4-+NO2-+ H+→ Mn2+ + NO3- + H2O
7. Cr2O72-+J- + H+ →Cr3++J2+H2O
8. NO3- + H2S + H+→ NO + S↓ + H2O
9. MnO4-+C2O42-+ H+→ Mn2+ + CO2 + H2O
10. J2+S2O32- → J- + S4O62-
3. Ќеге сынап H2SO4 Цде ер≥мейд≥, ал HJ-та сутег≥н бөл≥п шығарып ерид≥?
4. Ќеге HgS HNO3 Цта ер≥мейд≥, ал HNO3 пен HCl (1:3) қоспасында ерид≥?
5. “отығу Ц тотықсыздану потенциалы деген не, ол нен≥ сипаттайды?
6. —о2+/Co жұбының стандартты потенциалы -0,40 B. ќсы электрод пен қалыпты сутек электродынан тұратын гальваникалық элементте қандай электрохими€лық процестер жүред≥? ∆алпы реакци€ны теңд≥г≥н жазыңдар.
7. Mn2+/Mn жұбының Mn2+ концентраци€сы 5∙10-3 моль/л болғандағы потенциалын есептеңдер.
8. “өмендег≥ жүйелерд≥ң тотығу Ц тотықсыздану потенциалына ер≥т≥нд≥н≥ң қышқылдығы қалай әсер етед≥: 1) Cr2O72-/2Cr3+, 2) MnO4-/Mn2+; 3)SO42-/ H2S; 4) NO3-/NO; 5) AsO43-/AsO33-?
9. “өмендег≥ жүйелерд≥ң реалды потенциалын есептең≥здер: 1) 0,1 ћ S4O62-, 0,01 M S2O32-; 2) 1M MnO4-, 0,1M Mn2+, [H+]=0,1 моль/л; 3) 1M Cr3+, [H+] = 0,01 моль/л, 1ћ Cr2O72-.
10. Cr2O72-/2Cr3+ жүйес≥н≥ң реалды потенциалының мән≥н ер≥т≥нд≥н≥ң рЌ 1) 0,5; 2) 2,0; 3) 5,0; 4) 10,0 болғанда есептеңдер.
11. Fe 2+ және Fe3+ иондары бар ер≥т≥нд≥ге KCN қосқанда тотығу Ц тотықсыздану потенциалының мән≥ неге аза€ды?
12. Құрамында KMnO4, MnO2, және 0,01 M KOH бар ер≥т≥нд≥ге салынған Pt электродының потенциалы 0,74B Цқа сәйкес. ќсы ер≥т≥нд≥дег≥ KMnO4 тұзының концентраци€сы неге тең?
13. 1) 0,3 M HCOOH; 2) 5% NH4Cl ер≥т≥нд≥лер≥ндег≥ сутег≥ электродының потенциалын есептеңдер.
14. —утег≥ электродының потенциалы -0,53¬-қа тең болу үш≥н 1л 0,1ћ NH3 ер≥т≥нд≥с≥нде неше грамм NH4Cl ер≥ту керек?
15. 1л 0,1ћ CH3COONa және 100 мл 0,1 M CH3COOH араластырып алынған ер≥т≥нд≥дег≥ сутег≥ электродының потенциалын есептеңдер.
16. елт≥р≥лген металдардың қайсысы H+ иондарын H2-ге дей≥н тотықсыздандыра алады: Cd, Sn, Sb, Al, Ag?
|
|
|
17. AgJ Ц т≥ң ер≥г≥шт≥к көбейт≥нд≥с≥ 1∙10-16 , 1M HJ ер≥т≥нд≥с≥ндег≥ күм≥с электродының потенциалын есептең≥здер. ќсы ер≥т≥нд≥ден күм≥с сутег≥н ығыстырып шығара ала ма?
18. (-) Pt / H2 (газ) H2SO4 (1M) // AgNO3 (0,1M)/ Ag(+) келт≥р≥лген гальваникалық элементт≥ң Ag+/Ag жартылай элемент≥не CN- ионының концентраци€сы 1 моль/л болғанша KCN тұзы салынады. [Ag(CN)2]-комплекс≥н≥ң тұрақтылық константасы 1∙10+20. ќсы жағдайда т≥збектег≥ токтың бағыты өзгере ме?
19. “өмендег≥ тотығу тотықсыздану реакци€ларының тепетеңд≥к константаларын есептеңдер:
1) Sn 2+ + J2 ↔ Sn4+ + 2J-
2) 2MnO4- + 5NO2- + 6H+ ↔ 2Mn2+ + 5NO3- + 3H2O
3) 2Fe3+ + SnCl42- + 2Cl- ↔ 2Fe 2+ + SnCl62-
4) Cr2O72- + 6Fe2+ +14H+↔2Cr3+ + 6Fe3+ + 7H2O
5) MnO4- + 5Fe2+ + 8H+ ↔ Mn2+ + 5Fe3+ + 4H2O
6) Cr2O72- + 6J- +14H+↔2Cr3+ + 3J2 + 7H2O
7) 2S2O32- + J2 ↔ S4O62- + 2J-
“ест тапсырмалары
1. ћына бер≥лген теңдеулерд≥ң қайсысы тотығу-тотықсыздану реакци€сының тепе-теңд≥к константасы мен потенциалы арасындағы тәуелд≥л≥кт≥ дұрыс сипаттайды?
1) T lgK = 4970 n?E; 2)  ; 3)
; 3)  ;
;
4) T lgK = n?E; 5) дұрыс жауап бер≥лмеген.
2. ћына Fe3+/Fe2+-редокс жұптың (E0Fe(Ў)/Fe(11)=+0,77 B) тотыққан және тотықсызданған түрлер≥ концентраци€ларының қатынасы қандай болғанда жүйен≥ң реалды потенциалы оның стандартты потенциалы шамасынан төмен болады (E01 < E0)?
1) [Fe3+] / [Fe2+] = 1: 1;
2) [Fe3+] / [Fe2+] = 1: 10;
3) [Fe3+] / [Fe2+] = 10: 1;
4) [Fe3+] / [Fe2+] = 5: 2;
5) [Fe3+] / [Fe2+] = 5: 5.
3. Ѕер≥лген MnO4-/ Mn2+жүйес≥н≥ң реалды потенциалын қышқылдық ортада мына теңдеумен анықтауға болады:
1) 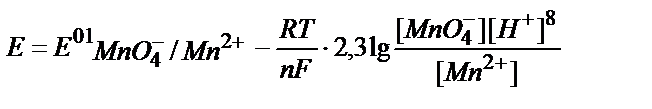 ;
;
2)  ;
;
3)  ;
;
4)  ;
;
5)  .
.
4. Ѕер≥лген тотыққан-тотықсызданған жүйелерд≥ң қайсысының потенциалдары шамасына ер≥т≥нд≥ рЌ-ның өзгеру≥ әсер етпейд≥?
1) Cr2O72-/ 2Cr3+; 2) MnO4-/ Mn2+; 3) SO42-/ H2S;
4) Fe3+/ Fe2+; 5) NO3-/ NO.
5. Hg22++2e ↔2Hgoтепе-теңд≥г≥ орнаған жүйеде мына реакци€ бойынша Hg22++ 2Cl-↔ Hg2Cl2↓ суда нашар ерит≥н қосылыс түз≥лген жағдайда (T=293 K) жүйен≥ң тотығу-тотықсыздану потенциалы қайсы теңдеу бойынша анықталады?
1) E = E0 + (0,059/2) lg ≈ Ц 0,059 lg [Cl-];
2) E = E0 + 0,029 lg ≈ Ц 0,058 lg [Cl-];
3) E = E0 Ц 0,058 lg ≈ Ц 0,058 lg [Cl-];
4) E = E0 + 0,059 lg≈ + 0,058 lg [Cl-];
5) E = E0 Ц 0,029 lg ≈ Ц 0,058 lg [Cl-].
6. Ag++ e → Agoжүйеде қатты фаза (тұнба) түз≥лген жағдайда реалды стандартты потенциал шамасы мына теңдеумен анықталады (T = 298K):
1) E01 = E0 + 0,059 lg≈ ; 2) E01 = E0 Ц 0,058 lg≈ ;
3) E01 = E0 + 0,059 p≈ ; 4) E01 = E0 Ц (RT/nF) 3,3 lg≈ ;
5) E01 = E0 + (RT/F) 2,3 ln≈ .
7. “отықтырғыштар рет≥нде қолданылатын қосылыстар қатарын анықтаңыз:
1) Na2S2O8, HNO3, Na2S2O3; 2) KJO3, PbO2, HJ;
|
|
|
3) K2Cr2O7, H2O2, SnCl2; 4) KMnO4, Na2CrO4, HNO3;
5) KClO3, H2S, H2SO4.
8. ClO3-ионы Cl--ионына дей≥н тотықсызданғанда, ClO3-/Cl-жүбының тотығу-тотықсыздану потенциалын қандай формуламен есептеуге болады?
1)  ; 2)
; 2) 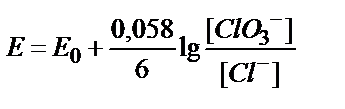 ;
;
3)  ; 4)
; 4)  ;
;
5) 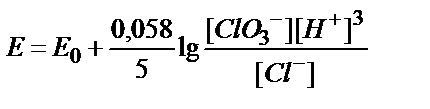 .
.
9. Қандай жағдайда MnO4-+8H++5e↔Mn2++4H2O жартылай реакци€сының потенциалы оның стандартты потенциалына тең болады?
1) aох = aRed = 1, pH = 1;
2) aох = aRed = 1, pH = 7;
3) aох = aRed (кез келген a үш≥н);
4) aох = aRed = 1, a(H+)= 1;
5) aох = aRed, pH = 1.
10. T=298K-да (Ox+ne ↔ Red) жүйес≥н≥ң тотығу-тотықсыздану потенциалы шамасына ер≥т≥нд≥н≥ң иондық күш≥н≥ң әсер≥н дұрыс ескерет≥н теңдеуд≥ көрсет≥ң≥з:
1) 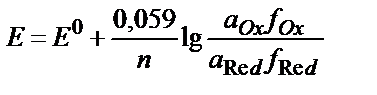 ;
;
2)  ;
;
3)  ;
;
4)  ;
;
5)  .
.
11. ћына тотықсыздандырғыштың қайсысының тотыққан түр≥ ең күшт≥ тотықтырғыш болады?
1) H2SO3 E0 (SO42-/SO32-) = +0,17B;
2) Sn2+ E0 (Sn4+/Sn2+) = +0,15B;
3) H2O2 E0 (O2/H2O2) = +0,69B;
4) Cr3+ E0 (Cr3+/Cr2+) = -0,41B;
5) Na2S2O3 E0 (S4O62-/2S2O32-) = +0,09B.
12. “ем≥р қосылысы тотықсыздандырғыш рет≥нде қатысатын процест≥ң теңдеу≥н көрсет≥ң≥з:
1) Sn2+ + 2 Fe3+ ↔ Sn4+ + 2Fe2+; 2) Fe2+ + S2+ ↔ FeS↓;
3) FeO + Mg ↔ Fe + MgO; 4) 2Fe2+ + H2O2+ 4OH-↔ 2Fe (OH)3↓;
5) Fe2O3 + 3H2 ↔ 2Fe + 3H2O.
13. —утек асқын тотығы тотықтырғыш рет≥нде қатысатын процест≥ң теңдеу≥н көрсет≥ң≥з:
1) 2CrO2-+ 3H2O2+ 2OH-↔ 2CrO42-+ 4H2O;
2) 2MnO4-+ 5H2O2+ 6H+↔ 2Mn2++ 5O2+ 8H2O;
3) O3+ H2O2↔ H2O + 2O2;
4) MnO(OH)2+ H2O2+ 2H+↔ Mn2++ O2+ 2H2O;
5) Ag2O + H2O2↔ 2Ag + H2O + O2.
14. елт≥р≥лген реакци€лардың қайсысы диспропорци€лану реакци€сына жатпайды?
1) H2O2+ H2O2↔ 2H2O + O2;
2) 4ClO3-↔ 3ClO4-+ Cl-;
3) 3Au+↔ Au3++ 2Auо;
4) 3Mn2++ 2MnO4-+ 7H2O ↔ 5MnO(OH)2↓ + 4H+;
5) дұрыс жауап бер≥лмеген.
15. Қайсы теңдеу Zn2+/Zn↓ жұбының тепе-теңд≥к потенциалы мен заттың тотыққан және тотықсызданған түрлер≥ концентраци€лары арасындағы байланысты дұрыс көрсетед≥?
1) 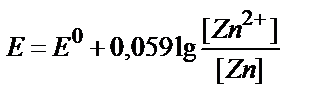 ;
;
2)  ;
;
3)  ;
;
4)  ;
;
5) E = E0 + 0,059 lg[Zn2+].
16. “отығу-тотықсыздану реакци€сының электрқозғаушы күш≥н (ЁҚ ) қалай есептеуге болады?
1) ЁҚ = EооxЦ Eоred; 2) ЁҚ = EoredЦ Eoox;
3) ЁҚ = Eoox+ Eored; 4) 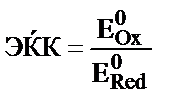 ; 5)
; 5) 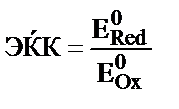 .
.
17. ≈р≥т≥нд≥де б≥рмезг≥лде б≥рге жүрген иондар қандай ретпен тотығады?
(EoSo/S2-= +0,14 B; EoSO42-/SO32-= +0,17 B; E0≤2/2≤-= +0,536 B; EoBr2/2Br-= +1,087 B)
1) Br-, ≤-, SO32-, S2-; 2) S2-, ≤-, Br-, SO32-; 3) ≤-, Br-, SO32-, S2-;
4) S2-, SO32-, ≤-, Br-; 5) SO32-, ≤-, S2-, Br-.
18. AgClқат.+e ↔Agқат.+Cl-жартылай реакци€сы үш≥н оның реалды стандартты потенциалының теңдеу≥н көрсет≥ң≥з.
1)  ;
;
2)  ;
;
3) 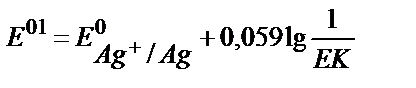 ;
;
4)  ;
;
5)  .
.
19. Sn2++2Fe3+  Sn4++2Fe2+реакци€сы үш≥н тепе-теңд≥к орнауын сипаттайтын жағдайлар:
Sn4++2Fe2+реакци€сы үш≥н тепе-теңд≥к орнауын сипаттайтын жағдайлар:
1) [Fe3+] = [Fe2+], [Sn2+] = [Sn4+]; 2) EоFe3+/Fe2+= EоSn4+/Sn2+;
3) EFe3+/Fe2+= ESn4+/Sn2+; 4) [Sn2+] > [Fe2+], [Sn4+] < [Fe3+];
5) [Sn2+] = [Fe2+]2, [Sn4+] = [Fe3+]2.
20. Қандай жүйен≥ң тотығу-тотықсыздану потенциалы мән≥не ер≥т≥нд≥ рЌ әсер етпейд≥?
1) MnO4-/Mn2+; 2) AsO43-/AsO33-; 3) 2≤O3-/≤2;
4) ≤2/2≤-; 5) Cr2O72-/2Cr3+.
“арау






