Природные газы, представляющие собой смесь различных компонентов, при определенных давлениях и температурах в присутствии воды образуют белые кристаллические вещества, названные гидратами.
Из компонентов природных газов самостоятельно образуют гидраты: метан, этан, пропан, изобутан, азот, диоксид углерода, сероводород, а также меркаптаны.
Известны две структуры гидрата: структура I состоит из 46 молекул воды, а структура II – из 136. Число молекул воды в гидрате, приходящемся на одну молекулу газа при полном заполнении всех полостей, равно: для структуры I –n=5,75, для структуры II – n=5,667.
Как правило, природные газы образуют гидраты II структуры. При содержании пропана и изобутана в составе природных газов в 0,1% образуются гидраты структуры II, а в остальных случаях – структуры I. Гидраты структур I и II различаются между собой только их кристаллографическими данными (см. таблицу 2.11).
Экспериментально установлено, что гидраты, как правило, образуются на поверхности контакта воды с газом.
Механизм гидратообразования газов заключается в следующем, На поверхности раздела фаз происходит выпрямление искривленных водородных связей между молекулами воды в поверхностном слое жидкости. Мольный объем воды увеличивается. В результате полости квазикристаллической структуры воды оказываются доступными для адсорбции ими молекул газа. Когда количество адсорбпроводных молекул газа достигает их критической величины, происходит фазовый переход. Максимальное число молей газа в полостях структуры поверхностного слоя воды, требующееся для начала процесса гидратообразования, соответствует числу его молей в больших полостях элементарной ячейки гидратной решетки.
Таблица 2.11 – Параметры элементарных ячеек газовых гидратов
| Параметр | Структура I | Структура II | ||
| Малая полость | Большая полость | Малая полость | Большая полость | |
| Идеальный состав | i1∙3i2 | 23 H2O | i1∙2i2 | 17 H2O |
| Длина ребра элементарной ячейки а0, м | 12∙10-10 | 17,4∙10-10 | ||
| Количество молекул воды в ячейке N | ||||
| Среднее число молекул воды, приходящиеся на одну полость m | 5,75 | 5,67 | ||
| Количество полостей в ячейке n |
Исследования показывают, что количество адсорбционного газа, приходящееся на единицу объема поверхностного слоя воды в условиях Р и Т, исключающих гидратообразование, значительно ближе к количеству газа, содержащегося в единице объема воды элементарной ячейки гидрата, чем количество газа в аналогичном объеме жидкой воды. Причем чем ниже температура и выше давление, тем больше соответствие количества газа, содержащегося в единице объема поверхностного слоя воды и в элементарной ячейке гидрата.
Объем элементарной ячейки гидрата определяется по формуле:
V=N0a03 (2.81)
где V – объем элементарной ячейки гидрата, м3; N0 – 0,6024∙1024 – число Авогадро; a0 – параметр кристаллической решетки гидрата, м.
По известным величинам а0, приведенным в таблице 2.11 для гидратов структуры I (a0=12∙10-10м) и структуры II (а0=17,4∙10-10м), используя формулу (2.81), можно определить объем элементарной ячейки гидрата для I и II структур: VI=1040∙10-6 м3 и VII=3173∙10-6 м3.
Мольный объем воды в элементарной ячейке гидрата находим по формуле:
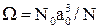 (2.82)
(2.82)
где N – число молей воды, составляющих элементарную ячейку гидрата.
Взяв из таблицы 2.11 для гидратов структуры I – NI=46 моль и для структуры II – NII=136 моль и подставив их в формулу (2.82), получаем ΩI=22,6∙10-6 м3/моль и ΩII=23,33∙10-6 м3/моль. Следовательно, при образовании газовых гидратов структуры I мольный объем воды увеличивается на (22,6–18)∙10-6=4,6∙10-6 м3/моль, а гидратов структуры II – на (23,3–18)∙10-6=5,33∙10-6 м3/моль.
Плотность воды в гидратной решетке ρвг определяется по формуле:
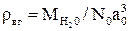 (2.83)
(2.83)
где  – масса элементарной ячейки гидратной решетки.
– масса элементарной ячейки гидратной решетки.
Для гидратов структуры I –  =46∙18=828,0 г, для гидратов структуры II –
=46∙18=828,0 г, для гидратов структуры II –  =136∙18=2448 г. С учетом этих данных из формулы (2.83) получаем ρвгI=0,7962∙103 кг/м3 и ρвгII=0,7715∙103 кг/м3.
=136∙18=2448 г. С учетом этих данных из формулы (2.83) получаем ρвгI=0,7962∙103 кг/м3 и ρвгII=0,7715∙103 кг/м3.
Массу молекул газа в элементарной ячейке можно определить по формуле:
 (2.84)
(2.84)
где n1 и n2 – соответственно число малых и больших полостей в элементарной ячейке; θ1i и θ2i – степени их заполнения молекулами i-го компонента газа; Мi – молекулярная масса i-го компонента газа.
Для структуры I – n1=2, n2=6, а для структуры II – n1=16, n2=8.
Степени заполнения полостей молекулами газа определяют по формуле:
 (2.85)
(2.85)
где Сi – постоянная Лэнгмюра для газа i-го компонента, МПа; Pi – парциальное давление i-го компонента, МПа.
Для определения Сi можно использовать формулу:
Сi=10 ехр(Аi–ВiТ) (2.86)
Значения Аi и Вi для гидратообразующих компонентов газов приведены в таблице 2.12. Парциальное давление i-го компонента газа определяется по формуле
Pi=Pxi (2.87)
где Р – давление гидратообразования, МПа; Xi - мольная доля i-го компонента в смеси.
Таблица 2.12 – Значения коэффициентов Аi и Bi
| Компонент | Малые полости | Большие полости | ||
| Аi | Bi | Аi | Bi | |
| Структура I | ||||
| CH4 | 6,9153 | 0,0316 | 6,0966 | 0,0279 |
| C2H6 | 9,4892 | 0,0406 | 11,9410 | 0,0418 |
| C2H4 | 18,1735 | 0,0729 | 20,2959 | 0,0729 |
| H2S | 6,0658 | 0,0117 | 4,4568 | 0,0117 |
| CO2 | 14,9976 | 0,0588 | 15,2076 | 0,0588 |
| N2 | 3,2485 | 0,0262 | 3,0116 | 0,0248 |
| Структура II | ||||
| CH4 | 6,0499 | 0,0284 | 6,2957 | 0,0285 |
| C2H6 | 9,4892 | 0,0406 | 11,9410 | 0,0418 |
| C2H4 | 18,1735 | 0,0729 | 20,2959 | 0,0729 |
| C3H8 | – | – | 18,2760 | 0,0462 |
| C3H6 | – | – | 9,6250 | 0,0182 |
| C4H10 | – | – | 13,6942 | 0,0277 |
| H2S | 4,8258 | 0,0093 | 2,4030 | 0,0063 |
| CO2 | 23,0350 | 0,0904 | 25,2710 | 0,0978 |
| N2 | 3,2485 | 0,0262 | 3,0116 | 0,0248 |
Плотность гидратов определяется по формуле:
 (2.88)
(2.88)
Состав гидрата также является одним из часто используемых свойств гидратов при инженерных расчетах. Для приведенного выше примера состав гидрата природного газа соответствует формуле 14,4568СН4∙0,5176× ×С2Н6∙4,8392С3Н8∙2,4367∙i-C4H10∙0,0272СО2∙136Н2О. В более общей форме состав этого гидрата можно выразить формулой 22,2784i∙136Н2О или же i∙6,11Н2О.
При решении многих прикладных задач необходимо знать теплоту гидратообразования газов. С достаточной для практики точностью полную теплоту гидратообразования газов можно определить по известным экспериментальным значениям равновесных параметров образования гидратов по формуле
 (2.89)
(2.89)
где Р1 и T1 – равновесные давления и температура гидратообразования в точке 1, а Р2 и Т2 – то же самое в точке 2; R – газовая постоянная, равная 8,31 Дж/моль∙К.
Методы определения равновесных давления и температуры гидратообразования (РИС 101-107)
Равновесные давление и температура гидратообразования определяются различными методами: экспериментально, графически и аналитически. В основу графического и аналитического методов заложены результаты экспериментального метода в обобщенном виде.
Наиболее точный метод определения условий гидратообразования – экспериментальный, реализуемый с помощью малогабаритного оборудования в лабораторных и промысловых условиях. Принципиальная схема установки по определению условий гидратообразования и технология проведения эксперимента изложены в [18].
Одним из простых и сравнительно приближенных методов является графический метод определения равновесных температуры и давления гидратообразования по кривым, построенным как для отдельных гидратообразующих компонентов, так и в целом для природных газов в зависимости от их относительной плотности. Методика определения условий гидратообразования по равновесным кривым заключается в следующем.
В соответствии с плотностью газа и расчетным распределением давления от пласта до системы осушки газа из графика показанного на рисунке 2.32, определяется температура гидратообразования. Область существования гидратов на этом графике находится выше и левее кривых. Чем больше давление и плотность газа, тем выше температура гидратообразования.
При наличии в составе газа азота, углекислого газа и сероводорода равновесные условия гидратообразования изменяются. В частности, при наличии в составе газа СО2 и H2S гидраты образуются более активно по сравнению с газом такой же плотности, но не содержащим этих компонентов. На рисунке 2.33 показаны кривые гидратообразования основных компонентов природного газа.
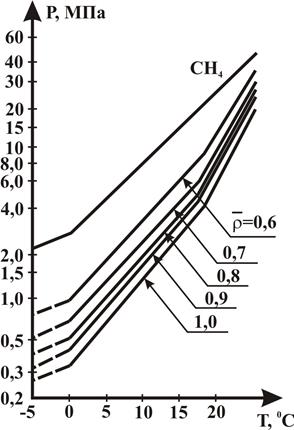
Рисунок 2.32 – Зависимость равновесных параметров гидратообразования природных газов от плотности.
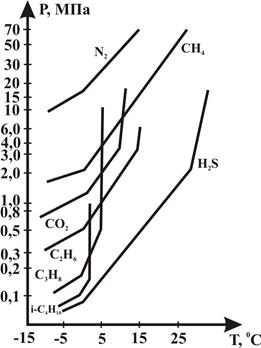
Рисунок 2.33 – Кривые гидратообразования отдельных компонентов природного газа.
Температуру гидратообразования природного газа, содержащего до 50 об.% H2S и до 10% С3Н8 в диапазоне изменений давления 0,3≤Р≤30 МПа, можно определить графически из рисунке 2.34а. Точность этого определения составляет 1,7 0С. Последовательность определения температуры гидратообразования при наличии в газе Н2S приведена в приложении.
Влияние наличия пропана в газе от 0 до 10 об.% на температуру гидратообразования учитывается с помощью вспомогательного графика, показанного на рисунке 2.34б. Поправка на влияние С3Н8 определяется следующим образом: на вспомогательном графике отыскиваются линии изоконцентрат, соответствующие содержанию H2S, равному 5%, и С3Н8, равному 0,5%. От точки пересечения этих линий проводят перпендикулярную линии H2S=5% прямую по направлению вниз до пересечения уровня, соответствующего линии Р=4 МПа, а от точки их пересечения проводят горизонтальную линию влево до пересечения с осью ординат. Значение на оси ординат температуры ΔT=-2°C соответствует поправке, вызванной наличием пропана в газе, 0,25%. Эту поправку следует вычесть из значения температуры гидратообразования, т.е. Т=Тр–ΔТ=18–2=16 0С.


Рисунок 2.34 – Номограмма для определения температуры гидратообразования сероводородсодержащих газов (а) и поправка на наличие пропана в газе (б).
Если поправка на наличие пропана будет определяться по правой части вспомогательного графика, то она прибавляется к Tр. Приведенная диаграмма может быть использована для определения Tр при наличии в газе кислых компонентов, т.е. H2S и С02, до 70% при соотношениях H2S/CO2=0,33–10.
Многочисленные эксперименты показывают, что аналитическую зависимость равновесной температуры гидратообразования от давления можно выразить формулой:
Tp=a(l+lgP)±b (2.90)
где а и b – коэффициенты, определяемые по результатам экспериментов для каждого месторождения. Значения а и b для наиболее крупных и различных по составу газа месторождений приведены в таблице 2.13.
Таблица 2.13 – Значения коэффициентов а и b для различных месторождений
| №№ п/п | Месторождение | Содержание СН4, % | а | b |
| Уренгойское (сеноманская залежь) | 98÷99,6 | 19,9 | –28,5 | |
| Уренгойское (валанжинская залежь) | 86,7 | 14,7 | –11,1 | |
| Медвежье, Ямбургское (сеноманская залежь) | 98,996 | 19,9 | –28,5 | |
| Вуктыльское | 81,2 | 12,2 | –8,2 | |
| Оренбургское | 84,2 | 16,7 | –14,2 | |
| Зальцведель-Пекензен (азот 65%) | 34,7 | 19,0 | –3,3 | |
| Карачаганакское Р<7,0 МПа Карачаганакское Р>7,0 МПа | 73,1 73,1 | 16,6 7,3 | –4,6 –12,4 | |
| Астраханское Р<7,0 МПа Астраханское Р>7,0 МПа | 51,2 51,2 | 21,5 14,0 | –9,2 –15,6 |
Из таблицы 2.13 видно, что коэффициенты а и b зависят от состава газа. Для давлений до 10 МПа температуру гидратообразования приближенно можно оценить:
в области положительных температур формулой:
Тр=18,47(1+lgP)–B;
ИЛИ
В инженерной практике равновесные условия образования гидратов для газовых смесей конкретных месторождений определяют по диаграммам, построенным на основе эксперементально полученных точек или по эмпирическим аналитическим зависимостям. В методической литературе часто рекомендуется метод Пономарева Г.В., по которому условия образования гидратов определяются по следующим зависимостям:
Lg Р = 2,0055+0,0541*(В+Т-273,15) Т >273,15 оК (3.34 )
Lg Р = 2,0055+0,0171*(В1-Т+273,15) Т <273,15 оК (3.35)
где:
Р – давление, МПа;
Т – температура, К.
Решая уравнения (3.34) и (3.35) относительно температуры и выражая давление в МПа, получаем:
для положительных температур:
Трг = 291,53+18,48*LgР-В (3.36 )
для отрицательных температур:
Трг = 215-58,48*LgР+В1 (3.37)
Здесь эмпирические величины В и В1 скоррелированы с относительной плотностью гидратообразующих компонетов.
 , (3.38)
, (3.38)
где
 - относительная плотность i –го гидратообразующего компонента;
- относительная плотность i –го гидратообразующего компонента;
 - его мольная доля.
- его мольная доля.
По апроксимации Пономарева Г.В., полученные коэффициенты В и В1 занесены в таблицу 3.1.
Таблица 3.1 – Значение коэффициентов В и В1

| В | В1 | 
| В | В1 | 
| В | В1 |
| 0,56 | 24,25 | 77,4 | 0,71 | 13,85 | 43,9 | 0,86 | 12,07 | 37,06 |
| 0,57 | 21,80 | 70,2 | 0,72 | 13,72 | 43,4 | 0,87 | 11,9 | 37,2 |
| 0,58 | 20,00 | 64,2 | 0,73 | 13,57 | 42,9 | 0,88 | 11,87 | 36,8 |
| 0,59 | 18,53 | 59,5 | 0,74 | 13,44 | 42,4 | 0,89 | 11,77 | 36,5 |
| 0,60 | 17,67 | 56,1 | 0,75 | 13,32 | 42,0 | 0,90 | 11,66 | 36,2 |
| 0,61 | 17,00 | 53,6 | 0,76 | 13,2 | 41,6 | 0,91 | 11,57 | 35,8 |
| 0,62 | 16,45 | 51,6 | 0,77 | 13,08 | 41,2 | 0,92 | 11,47 | 35,4 |
| 0,63 | 15,93 | 50,0 | 0,78 | 12,97 | 40,7 | 0,93 | 11,37 | 35,1 |
| 0,64 | 15,47 | 48,6 | 0,79 | 12,85 | 40,3 | 0,94 | 11,27 | 34,8 |
| 0,65 | 15,07 | 47,6 | 0,80 | 12,74 | 39,9 | 0,95 | 11,17 | 34,5 |
| 0,66 | 14,76 | 46,9 | 0,81 | 12,62 | 39,5 | 0,96 | 11,10 | 34,2 |
| 0,6 | 14,51 | 46,2 | 0,82 | 12,50 | 39,1 | 0,97 | 11,00 | 33,9 |
| 0,68 | 14,34 | 45,6 | 0,83 | 12,4 | 38,7 | 0,98 | 10,92 | 33,6 |
| 0,69 | 14,16 | 45,0 | 0,84 | 12,28 | 38,3 | 0,99 | 10,85 | 33,3 |
| 0,70 | 14,00 | 44,0 | 0,85 | 12,18 | 37,9 | 1,00 | 10,77 | 33,1 |
(2.91)
в области отрицательных температур формулой:
Тр= –58,5(1+lgP)+B1 (2.92)
где В и В1 – коэффициенты, определяемые из рисунка 2.35 в зависимости от отношения:
 (2.93)
(2.93)
где  – сумма парциальных плотностей изучаемого газа;
– сумма парциальных плотностей изучаемого газа; 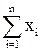 сумма в объемных долях единицы концентрации газов, обладающих гидратообразующими способностями; ε – характеризует плотность гидратообразующих компонентов рассматриваемого газа.
сумма в объемных долях единицы концентрации газов, обладающих гидратообразующими способностями; ε – характеризует плотность гидратообразующих компонентов рассматриваемого газа.
Это означает, что в коэффициенте ε не участвуют гидратообразующие компоненты газа.

Рисунок 2.35 – Зависимости коэффициентов В и В1, от ε.
При наличии в газе сероводорода и углекислого газа температуру гидратообразования можно определить по формуле:
 (2.94)
(2.94)
где Tн – нормальная температура, равная 273,15 К; а и b – коэффициенты, определяемые графически из рисунка 2.36 в зависимости от величины С:
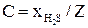 (2.95)
(2.95)
 суммарное содержание H2S и СО2 в объемных процентах в составе газа.
суммарное содержание H2S и СО2 в объемных процентах в составе газа.

Рисунок 2.36 – Зависимости коэффициентов а и b от С.
По формуле (2.94) температура гидратообразования определяется с приемлемой точностью при содержании неуглеводородных компонентов в составе газа до 30 об.%.






