При рассмотрении канонического распределения Гиббса предполагалось, что подсистема обменивается с термостатом энергией, а число частиц в ней не изменяется. Однако, чаще всего, подсистема обменивается с термостатом не только энергией, но и частицами. Описанию таких подсистем посвящено большое каноническое распределение Гиббса.
Пусть имеется макроскопическая система, находящаяся в состоянии термодинамического равновесия. Энергия этой системы равна 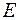 и остается величиной постоянной. Число частиц в этой системе равно
и остается величиной постоянной. Число частиц в этой системе равно 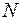 и также не изменяется со временем. Выделим в этой системе малую подсистему, энергия которой равна
и также не изменяется со временем. Выделим в этой системе малую подсистему, энергия которой равна 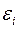 , и которая содержит
, и которая содержит  частиц. Все остальное окружение подсистемы назовем по-прежнему термостатом. Теперь рассмотрим случай, когда подсистема обменивается с термостатом и энергией и частицами и найдем вероятность того, что подсистема находится в состоянии с энергией
частиц. Все остальное окружение подсистемы назовем по-прежнему термостатом. Теперь рассмотрим случай, когда подсистема обменивается с термостатом и энергией и частицами и найдем вероятность того, что подсистема находится в состоянии с энергией 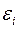 и содержит
и содержит  частиц.
частиц.
Пусть число состояний подсистемы равно 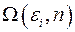 , а число состояний термостата
, а число состояний термостата 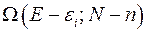 . Тогда вероятность того, что подсистема находится в состоянии с энергией
. Тогда вероятность того, что подсистема находится в состоянии с энергией 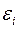 и содержит
и содержит  частиц, а термостат находится в состоянии с энергией
частиц, а термостат находится в состоянии с энергией 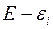 и содержит
и содержит  частиц, пропорциональна произведению числа состояний, то есть,
частиц, пропорциональна произведению числа состояний, то есть,
 (4.1)
(4.1)
Аналогично, для того, чтобы удовлетворялось условие аддитивности для энергий и числа частиц, воспользуемся понятием энтропии: 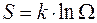 и запишем число состояний термостата:
и запишем число состояний термостата:
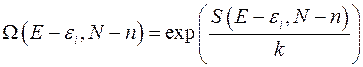 (4.2)
(4.2)
Так как 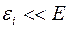 и
и 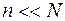 , то энтропию
, то энтропию  можно разложить в ряд по степеням
можно разложить в ряд по степеням 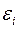 и
и  . При этом ограничимся только первыми членами разложения. Тогда получаем:
. При этом ограничимся только первыми членами разложения. Тогда получаем:
 (4.3)
(4.3)
Подставляем формулу (4.3) в формулу (4.2) и получаем:
 (4.4)
(4.4)
В этой формуле величина 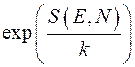 равна некоторой постоянной, величина
равна некоторой постоянной, величина 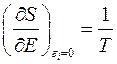 , а величина
, а величина 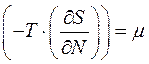 , где
, где  - химический потенциал. Тогда
- химический потенциал. Тогда 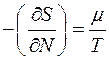 (4.5).Теперь формула (4.4) принимает вид:
(4.5).Теперь формула (4.4) принимает вид:
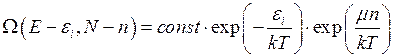 (4.6)
(4.6)
Теперь формулу (4.1), описывающую искомую вероятность можно записать в виде:
 (4.7)
(4.7)
Формула (4.7) представляет собой большое каноническое распределение Гиббса. Чтобы найти значение постоянной, воспользуемся условием нормировки, согласно которому имеем:
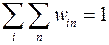 (4.8)
(4.8)
Воспользуемся этим условием:
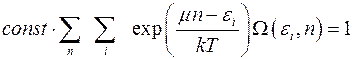 (4.9)
(4.9)
Отсюда находим неизвестную постоянную:
 (4.10)
(4.10)
Теперь большое каноническое распределение Гиббса можно записать в явном виде:
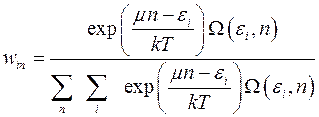 (4.11)
(4.11)
По этой формуле можно определить средние значения величин, зависящих от энергии и от числа частиц в подсистеме:
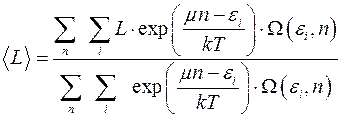 (4.12)
(4.12)
Например, можно найти среднее число частиц в подсистеме при произвольном значении ее энергии. Эта величина подробно выведена в формуле (4.13).
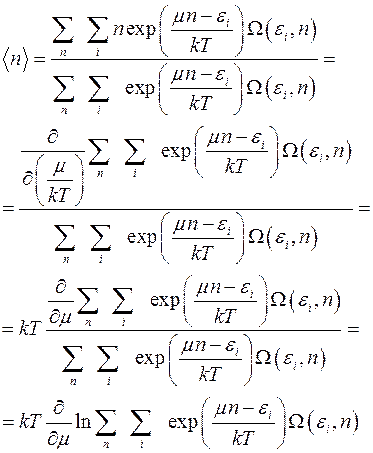 (4.13)
(4.13)
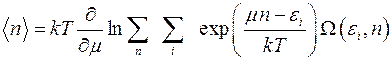 (4.13)
(4.13)
Большое каноническое распределение Гиббса, имеющее вид (4.11), можно записать в другом виде:
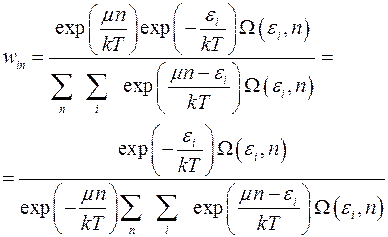 (4.14)
(4.14)
Теперь можно ввести обозначение:
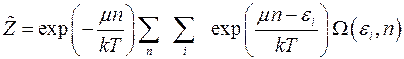 (4.15)
(4.15)
Величина 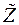 называется большой статистической суммой. Это выражение переходит в простую статистическую сумму. Если число частиц в системе постоянно. В этом случае большое каноническое распределение Гиббса переходит в каноническое распределение Гиббса.
называется большой статистической суммой. Это выражение переходит в простую статистическую сумму. Если число частиц в системе постоянно. В этом случае большое каноническое распределение Гиббса переходит в каноническое распределение Гиббса.
Статистическую сумму и большую статистическую сумму называют также функцией состояния или интегралом по состояниям.
Химический потенциал, также как и температура, является характеристикой всей системы. Он показывает, на какую величину изменяется энергия системы частиц при изменении числа частиц на единицу при неизменных других параметрах состояния.
Если в системе содержатся частицы разного сорта. То для каждого сорта частиц вводится свой химический потенциал. Поэтому в общем случае первое начало термодинамики записывается в виде:
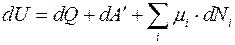 , (4.16)
, (4.16)
где 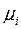 - химический потенциал частиц
- химический потенциал частиц 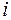 - того сорта.
- того сорта.
Выражение (4.16) можно записать в виде:
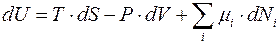 (4.17)
(4.17)
Отсюда следует смысл химического потенциала:
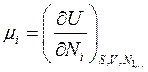 (4.18)
(4.18)
Кроме того, отсюда следует использованное выражение для связи энтропии и химического потенциала:

 при
при  и
и 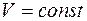 . Тогда
. Тогда
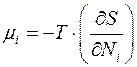 (4.19)
(4.19)






