Реакція з динітрофторбензолом (реакція Сенгера). Динітрофторбензол реагує з аміногрупою амінокислоти і, звільняючи фтористоводневу кислоту, утворює динітрофеніламінокислоту (ДНФ-ак):
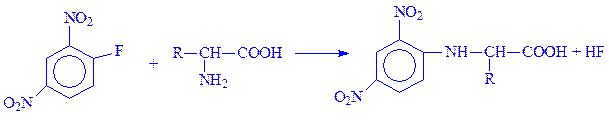
Ця реакція може відбуватися і за участю амінокислот, що входять в білок, але тільки по їх вільних аміногрупах. Якщо після завершення реакції провести гідроліз білка, то всі амінокислоти вивільняються. Гідроліз не порушує структуру ДНФ-ак. Використовуючи розчинність ДНФ-ак в органічних розчинниках, можна відділити, а отже і ідентифікувати амінокислоти, які, знаходячись у складі білка, мали вільні аміногрупи.
Реакція з 1-диметиламінонафтил-5-сульфонілхлоридом (дансилом, ДНС-метод). Більш чутливим, ніж динітрофенільний, є дансильний метод визначення N-кінцевих амінокислот. Суть цього методу полягає в тому, що N-кінцева амінокислота пептиду в лужному середовищі взаємодіє з 1-диметиламінонафтил-5-сульфонілхлоридом (дансилом). При цьому утворюється диметилнафтилсульфоніл-білок (ДНС-білок):
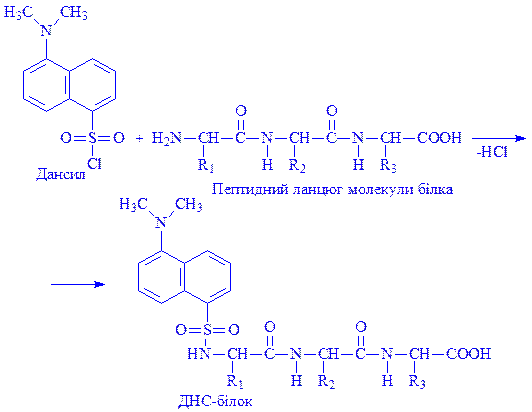
Далі здійснюють кислотний гідроліз ДНС білка 20% розчином HCl, що призводить до утворення вільних амінокислот і N-кінцевої амінокислоти у вигляді ДНС-похідного:
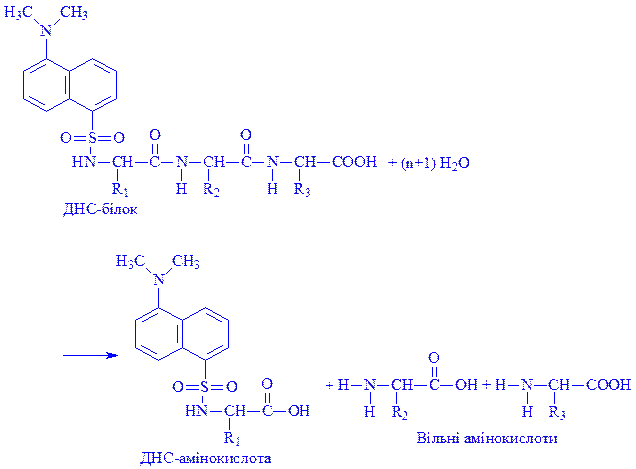
Після цього ДНС-амінокисоту, завдяки інтенсивній флуоресценції дансильних груп, виявляють і кількісно визначають.
Реакція з фенілізотіоціанатом (реакція Едмана). Фенілізотіоціанат в слаболужному середовищі реагує з аміногрупою:
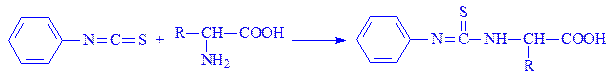
У слабокислому середовищі продукт цієї реакції циклізується. Якщо піддати амінокислоту, яка входить до складу білка, дії фенілізотіоціаната, то її можна виділити й ідентифікувати у формі фенілтіогідантоїнового (ФТГ-ак) похідного:
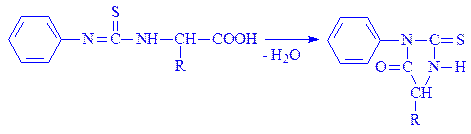
Цей метод дозволяє ідентифікувати кінцеві амінокислоти білка, аміногрупи яких вільні. Утворення ФТГ-ак не вимагає гідролізу решти частини білка.
Для визначення N-кінцевих залишків амінокислот крім хімічних методів використовують також і ферментативні. З цією метою використовують фермент з групи екзопептидаз – лейцинамінопептидазу, яка діє на пептид з N-кінця.
Кольорові реакції. Нінгідрин здійснює декарбоксилування a-амінокислот з утворенням СО2, NH3 і альдегіду, який містить на один атом вуглецю менше, ніж вихідна амінокислота. Відновлений нінгідрин реагує з вільним аміаком, утворюючи блакитний комплекс з максимумом поглинання при lmax=570 нм:
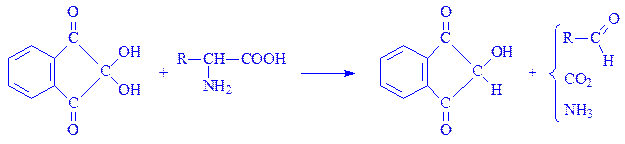
Утворення цієї забарвленої сполуки використовується в кількісному тесті на a-амінокислоти, за допомогою якого є можливість виявити їх, якщо навіть вони знаходяться у концентрації до 1мкг. Нінгідрин реагує не тільки з амінокислотами, але і з другими амінами; при цьому також утворюється блакитне забарвлення, але не виділяється вуглекислий газ. Таким чином, саме виділення СО2 є індикатором участі в реакції a-амінокислоти. Аміак і пептиди також вступають в реакцію з нінгідрином, але менш активно ніж a-амінокислоти. Продукт реакції між проліном (гідроксипроліном) і нінгідрином має жовте забарвлення.
Флуорескамін є ще більш чутливим реагентом, який дозволяє виявляти амінокислоти в кількості порядку нанограм. Як і нінгідрин, він утворює комплекс не тільки з амінокислотами, але і іншими амінами.
Утворення пептидних зв’язків. Найбільш важливою реакцією, в якій приймають участь амінокислоти, є утворення пептидних зв’язків. При цьому виділяється одна молекула води:
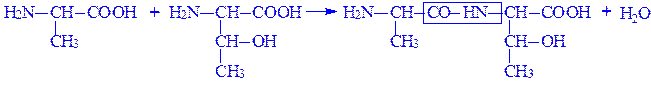
Однак, реакція здійснюється не так, як показано на малюнку, оскільки рівновага сильно зміщення в сторону гідролізу пептичного зв’язку. Для утворення пептидного зв’язку між двома амінокислотами карбоксильна група повинна бути попередньо активована. Хімічний синтез здійснюється шляхом попереднього утворення хлорангідриду. Біологічна активація включає взаємодію з АТФ.
Властивості індивідуальних амінокислот. Гліцин, найменша з амінокислот, може локалізуватися в таких областях трьохвимірної структури, які недоступні для інших.
Аліфатичні R–групи аланіну, валіну, лейцину і ізолейцину, а також ароматичні R-групи фенілаланіну, тирозину і триптофану – гідрофобні; ця властивість призводить до одного важливого наслідку – утворення впорядкованого поверхневого шару молекул води в області поверхні молекули білка, де експоновані неполярні R–групи. Заряджені R–групи основних і кислих амінокислот відіграють важливу роль в стабілізації специфічної конформації білка шляхом утворення сольових зв’язків. Крім того, амінокислоти з позитивно і негативно зарядженими R–групами, а також гістидин можуть приймати участь у формуванні систем “перенесення заряду”, які в ході ферментативного каталізу забезпечують переміщення заряду на значні відстані. І на завершення, унікальна і важлива роль у ферментативному каталізі належить гістидину – рК імідазольної групи при рН=7 може позмінно виступати в ролі основного або кислотного каталізатора.
Первинна спиртова група серину і первинна тіоспиртова група (–SH) цистеїну є добрими нуклеофілами які приймають участь в ферментативному каталізі. Хоча вторинна спиртова група треоніну теж виявляє нуклеофільні властивості, але дані про її можливу каталітичну функцію відсутні. Окрім каталітичної функції –ОН група серину приймає участь в регуляції активності деяких ключових ферментів метаболізму, активність яких залежить від фосфорилювання окремих залишків серину.
Амінокислоти не поглинають світло в видимій частині спектру (іншими словами, вони не мають забарвлення). За виключенням ароматичних кислот і гістидину, вони не поглинають світло і в ультрафіолетовій області при довжинах хвиль вище 240 нм.






