Понятие электродного потенциала применимо не только к паре Меn+|Мео, но и к любой сопряженной системе окисленная форма|восстановленная форма. Его называют окислительно-восстановительным потенциалом. Окислительно-восстановительный потенциал, измеренный при стандартных условиях, называется стандартным окислительно-восстановительным потенциалом. В электрохимии принято все электродные равновесия записывать в направлении процесса восстановления, то есть присоединения электронов:
Zn2+ + 2e– = Zn, Ео= - 0,76 В
Значения стандартных окислительно-восстановительных потенциалов сведены в справочные таблицы и используются для термодинамического анализа возможности протекания ОВР в водных растворах.
Самопроизвольно протекающие реакции характеризуются отрицательной величиной энергии Гиббса ∆Go298. Энергии Гиббса окислительно-восстановительной реакции может быть выражена как работа электрического тока, совершаемая в гальваническом элементе, и может быть связана с ЭДС элемента. Эта связь для стандартных условий дается соотношением
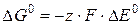 ,
,
где D G 0 – стандартная энергия Гиббса реакции, Дж; z – число молей электронов, переходящих от окислителя к восстановителю в данной реакции, моль (определяется как наименьшее общее кратное от принятых и отданных электронов); F – постоянная Фарадея, равная 96 484 Кл/моль; D E 0 – стандартная ЭДС гальванического элемента, в основе которого лежит данная реакция, В.
Значения D E 0 вычисляют через стандартные потенциалы полуреакций окисления и восстановления, причем от потенциала окислителя нужно вычитать потенциал восстановителя:
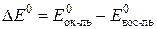 .
.
Значения стандартных потенциалов полуреакций окисления и восстановления могут быть использованы для вычисления констант равновесия реакций исходя из следующего соотношения:
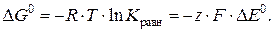
Откуда можно выразить константу равновесия реакции K равн:
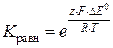 .
.
После подстановки в последнее выражение постоянных F и R, а также стандартной температуры 298 К (так как значения стандартных потенциалов приводятся при стандартной температуре) и после перехода от натурального логарифма к десятичному выражение для константы равновесия примет следующий вид:
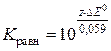 .
.
Энергия Гиббса реакции служит для определения термодинамической возможности протекания реакций и для установления направления протекания обратимых реакций. Реакция термодинамически возможна, или протекает слева направо, если
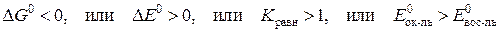 .
.
Реакция термодинамически невозможна, или протекает справа налево, если
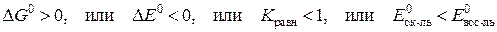 .
.
Пример. Определите возможность окисления в стандартных условиях соляной кислоты бихроматом калия. Ответ подтвердите расчетом стандартной энергии Гиббса и константы равновесия реакции.
Решение. Записываем уравнение окислительно-восстановительной реакции и составляем полуреакции окисления и восстановления:
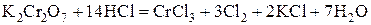
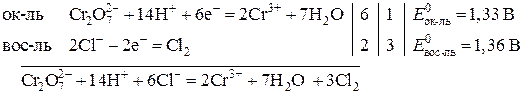
Значения стандартных потенциалов полуреакций восстановления (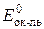 ) и окисления (
) и окисления (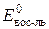 ) берем из табл. 4 в приложении. Вычисляем D E 0:
) берем из табл. 4 в приложении. Вычисляем D E 0:
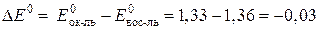 В.
В.
Рассчитываем энергию Гиббса реакции по формуле ∆Go298 = – z∙F∙∆Eo. Число молей электронов, которое переходит от окислителя к восстановителю, определяем по стехиометрическим коэффициентам в уравнении реакции. В реакции участвует 1 моль K2Cr2O7, который принимает 6 электронов от 6 ионов Cl–. Поэтому в данной реакции z = 6. Энергия Гиббса реакции в стандартных условиях равна
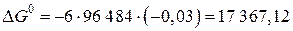 Дж.
Дж.
Определяем константу равновесия:
 .
.
Для данной реакции D G 0 > 0 и K равн < 1, следовательно, реакция термодинамически невозможна в стандартных условиях.
КОРРОЗИЯ МЕТАЛЛОВ
Коррозия металлов – это самопроизвольно протекающий процесс разрушения металлов в результате химического и электрохимического взаимодействия с окружающей средой.
Химическая коррозия обусловливается взаимодействием металлов с сухими газами (O2, SO2, H2S и т. д.) и жидкими неэлектролитами (смазочные масла, нефть, керосин).
4Ag + 2H2S + O2 = 2Ag2S + 2H2O
Этой реакцией объясняется потемнение серебряных изделий на воздухе.
Электрохимическая коррозия происходит при контакте металлов с электролитами под воздействием возникающих гальванических пар (коррозионных гальванических пар). При электрохимической коррозии протекают одновременно два процесса:
1) анодный процесс (окисление металла)
Мео – ne– = Меn+
2) катодный процесс (восстановление окислителя)
O2 + 2H2O + 4e– = 4OH– (если окислитель –кислород)
2H+ + 2e– =H2 (если окислитель – кислота)
Кислородная коррозия протекает в нейтральных и основных растворах, а водородная коррозия – в кислых растворах.
Пример. Рассмотрим процесс электрохимической коррозии оцинкованного и никелированного железа во влажном воздухе (нейтральная среда) и в соляной кислоте, если покрытие нарушено?
Решение. Исходя из положения металлов в ряду стандартных электродных потенциалов, находим, что цинк более активный металл (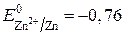 B), чем железо (
B), чем железо (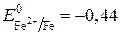 B), и в образующейся коррозионной гальванической паре цинк будет анодом, а железо – катодом. Цинковый анод растворяется.
B), и в образующейся коррозионной гальванической паре цинк будет анодом, а железо – катодом. Цинковый анод растворяется.
Анодный процесс:
Zn – 2e– = Zn2+
Электроны с цинка переходят на железо, и на границе железо – электролит происходит восстановление окислителя.
Катодный процесс:
2H+ + 2e– =H2 (кислая среда)
O2 + 2H2O + 4e– = 4OH– (нейтральная среда)
Продуктом коррозии в кислой среде является соль ZnCl2,в нейтральной среде – гидроксид Zn(OH)2:
Zn + 2НCl = ZnCl2 + H2
2Zn + O2 + 2H2O = 2Zn(OH)2
Tаким образом, цинковое (анодное) покрытие защищает железо от коррозии.
В паре Fe – Ni более активным металлом является железо (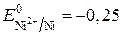 B), оно выступает в роли анода и подвергается разрушению.
B), оно выступает в роли анода и подвергается разрушению.
Анодный процесс:
Fe – 2e– = Fe2+
Катодный процесс:
2H+ + 2e– = H2 (кислая среда)
O2 + 2H2O + 4e– = 4OH– (нейтральная среда)
Продуктом коррозии в кислой среде является соль FeCl2, а в нейтральной – Fe(OH)2, который в присутствии кислорода в электролите окисляется:
Fe + 2НCl = FeCl2 + H2
2Fe + O2 + 2H2O = 2Fe(OH)2
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
При этом образуются рыхлые слои бурой ржавчины.
Покрытия железа менее активными металлами (катодные покрытия) эффективны до тех пор, пока не нарушены.
Химически чистые металлы более устойчивы к коррозии, чем сплавы металлов.
Пример. Чем вызывается коррозия чугуна?
Решение. Чугун имеет неоднородный состав. Чугун – это сплав железа с углеродом, он содержит зерна цементита Fe3C. Между свободным металлом и его соединением возникает гальваническая пара. Анодом в этом случае является металл, а катодом – зерна цементита, так как в нем часть электронов проводимости израсходована на образование химической связи. При наличии влаги железо (анод) начинает переходить в ионы Fe2+, которые дают с ионами OH–, образовавшимися на зернах цементита (катод), гидроксид железа (II), окисляющийся кислородом до ржавчины.
Анодный процесс:
Fe – 2e– = Fe2+
Катодный процесс:
O2 + 2H2O + 4e– = 4OH–
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3






