Впервые идея наложения отверстия, которое бы сообщало полость кишки с внешней средой с целью ее декомпрессии, получила свое практическое воплощение в виде операции энтеростомии, которая была выполнена больному с ущемленной грыжей французским хирургом Renaut в 1772 году. Вашп в 1879 году сообщил о наложении разгрузочной илеостомы больному со стенозирующей опухолью восходящего отдела ободочной кишки. Исход операции оказался неблагоприятным вследствие отравления ртутью, принятой больным накануне операции в качестве слабительного средства. Благоприятного исхода после такой операции впервые добился МаусН в 1883 году. С этого момента энтеростома, как метод лечения кишечной непроходимости, стала применяться в медицинских учреждениях Европы и Америки. В 1902 году на съезде германских хирургов Heidenhain доложил о применении у шести больных с паралитической непроходимостью энтеростомии, четверо из которых выздоровели. К 1910 году Krogis уже имел опыт 107 таких вмешательств. Термин «илеостома» предложил в 1913 году Brown, сообщив при этом об успешном лечении таким способом 10 больных неспецифическим язвенным колитом и кишечной непроходимостью. В России использование илеостомии при лечении перитонита и кишечной непроходимости поддержали А.А.Бобров (1899) и В.М.Зыков (1900).
Однако по мере накопления клинического материала многие хирурги стали сдержанно относиться к подобным операциям, что было связано с тяжелыми гнойно-септическими осложнениями и высокой летальностью после наложения стом. Так, И.И.Греков в 1912 году рекомендовал заменить энтеростомию опорожнением перерастянутых петель кишки путем ее пункции с последующим Ушиванием пункционного отверстия. К этому времени появляются первые сообщения об успешном лечении парезов кишечника с помощью зонда, заведенного в желудок и двенадцатиперстную кишку.
Уже в 1910 году Westermann обобщил опыт лечения 15 больных перитонитом с помощью активной аспирации желудочного

ГЛАВА 2
 содержимого и дал ей высокую оценку. По предложению Kanavel (1916) для этой цели стали использовать дуоденальный зонд. Wan-gensteen к 1913 году имел опыт лечения аналогичным способом 32 больных перитонитом и кишечной непроходимостью. Важным событием в совершенствовании способов декомпрессии кишечника следует считать предложение T.Miller et W.Abbott (1934) использовать для дренирования тонкой кишки зонд с резиновой манжетой на его конце. Перистальтические волны, проталкивая раздуваемую через отдельный канал манжету в аборальном направлении, должны были обеспечить продвижение зонад по кишечной трубке. Ввиду того» что зонд нередко сворачивался в желудке и не проходил в двенадцатиперстную и тощую кишки, он получил в дальнейшем целый ряд усовершенствование. Так» М.О.Cantor в 1946 году предложил заменить манжету на баллончик, заполненный ртутью. Продвижение зонда по желудочно-кишечному тракту осуществлялось за счет текучести ртути. В 1948 году G.A.Smith предложил гибкий стилет для управления верхушкой занда. Проведение зонда в тощую кишку осуществлялось под рентгеновским контролем. D.L.Larson et al. (1962) изобрели кишечный зонд с магнитом на конце. Передвижение зонда осуществлялось с помощью магнитного поля. Однако, несмотря на технические усовершенствования зонда Миллер-Эббота, этот сопособ в дальнейшем оказался малопригодным для дренирования тонкой кишки в условиях стойкого пареза. Он требовал продолжительных и сложных манипуляций, связанных с вынужденным положением тяжелобольных, частыми контрольными рентгенологическими исследованиями, и, кроме того, требовалось наличие перистальтической активности кишечника. По предложению G.A.Smith (1956) и J.C.Thurner et al. (1958) зонд Миллер-Эббота начали использовать для трансназальной интубации тонкой кишки во время операции.
содержимого и дал ей высокую оценку. По предложению Kanavel (1916) для этой цели стали использовать дуоденальный зонд. Wan-gensteen к 1913 году имел опыт лечения аналогичным способом 32 больных перитонитом и кишечной непроходимостью. Важным событием в совершенствовании способов декомпрессии кишечника следует считать предложение T.Miller et W.Abbott (1934) использовать для дренирования тонкой кишки зонд с резиновой манжетой на его конце. Перистальтические волны, проталкивая раздуваемую через отдельный канал манжету в аборальном направлении, должны были обеспечить продвижение зонад по кишечной трубке. Ввиду того» что зонд нередко сворачивался в желудке и не проходил в двенадцатиперстную и тощую кишки, он получил в дальнейшем целый ряд усовершенствование. Так» М.О.Cantor в 1946 году предложил заменить манжету на баллончик, заполненный ртутью. Продвижение зонда по желудочно-кишечному тракту осуществлялось за счет текучести ртути. В 1948 году G.A.Smith предложил гибкий стилет для управления верхушкой занда. Проведение зонда в тощую кишку осуществлялось под рентгеновским контролем. D.L.Larson et al. (1962) изобрели кишечный зонд с магнитом на конце. Передвижение зонда осуществлялось с помощью магнитного поля. Однако, несмотря на технические усовершенствования зонда Миллер-Эббота, этот сопособ в дальнейшем оказался малопригодным для дренирования тонкой кишки в условиях стойкого пареза. Он требовал продолжительных и сложных манипуляций, связанных с вынужденным положением тяжелобольных, частыми контрольными рентгенологическими исследованиями, и, кроме того, требовалось наличие перистальтической активности кишечника. По предложению G.A.Smith (1956) и J.C.Thurner et al. (1958) зонд Миллер-Эббота начали использовать для трансназальной интубации тонкой кишки во время операции.
Интерес к энтеростомии как дренирующей операции возобновился после разработки Richardson (1927) подвесной энтеростомии с заведением в просвет кишки зонда для питания больных, страдающих опухолями желудка, а также предложения Heller (1931) использовать гастростому для лечения паралитической кишечной непроходимости. В это же время F.Rankin (1931) предложил формировать илеостому вне лапаротомной раны. В России впервые подвесную энтеростомию для лечения перитонита и кишечной непроходимости выполнил Б.А.Петров в 1935 году. Но более значительный вклад в разработку и пропаганду этого метода внес С.С.Юдин. Подробное описание наложения подвесной энтеросто-мы он изложил в работе «Как снизить послеоперационную смер-
ГЛАВА 2
 1Гость у раненых в живот», вышедшей в 1943 году. Эта методика нашла широкое распростанение во время Великой Отечественной войны при оказании хирургической помощи раненым в живот.
1Гость у раненых в живот», вышедшей в 1943 году. Эта методика нашла широкое распростанение во время Великой Отечественной войны при оказании хирургической помощи раненым в живот.
По данным А.А.Бочарова (1947) и С.И.Банайтиса (1949), она была сделана не менее чем в 12,8% операций по поводу огнестрельных ранений живота с повреждением кишечника. В послевоенные годы началось постепенное снижение интереса к энтеростомии по С.С.Юдину. Многие авторы ссылались на то, что при параличе кишечника она приводит к разгрузке лишь той части кишки, на которую наложена. Кроме того, формировавшиеся высокие тонкокишечные свищи зачастую приводили к истощению и гибели больных. Отношение к этому вопросу изменилось после того, как J.W.Baxer в 1959 году предложил использовать при наложении подвесной энтеростомии длинные кишечные зонды и проводить интубацию всей тонкой кишки.
В нашей стране методика декомпрессии тонкой кишки через подвесную илеостому с использованием длинных кишечных зондов детально разработана в начале шестидесятых годов профессором И.Д.Житнюком. С тех пор она получила название «ретроградная интубация тонкой кишки по И.Д.Житнюку» и тридцать лет с успехом используется в лечении перитонита и кишечной непроходимости.
J.M.Farris et G.K.Smith в 1956 году впервые дали глубокий анализ и обосновали преимущества дренирования тонкой кишки через гастростому. Среди отечественных хирургов этот метод получил широкое распространение после опубликования Ю.М.Дедерером в 1962 году результатов лечения с помощью гас-троэнтеростомии больных паралитической кишечной непроходимостью.
И.С.Мгалоблишвили в 1959 году предложил использовать для интубации тонкой кишки аппендикостому. Однако более широкое распространение получил метод энтеростомии через цекостому, предложенный в 1965 году G.Scheide.
С появлением новых конструкций назоэнтеральных зондов многие хирурги стали отдавать предпочтение закрытым способам интраоперационного дренирования тонкой кишки. Даже такие сторонники и пионеры открытых способов дренирования, как O.H.Wangensteen и J.W.Baker, начали использовать в лечении перитонита и кишечной непроходимости назоэнтеральное дренирование.
Таким образом, в конце пятидесятых — начале шестидесятых годов хирурги уже имели на вооружении целый ряд способов де-
J
Ftl 0
ГЛАВА 2
 компрессии тонкой кишки, а кишечный зонд, по мнению H.Hamelmann und H.Piechlmair (1961), стал таким же обязательным инструментом в операционном наборе, как скальпель и пинцет
компрессии тонкой кишки, а кишечный зонд, по мнению H.Hamelmann und H.Piechlmair (1961), стал таким же обязательным инструментом в операционном наборе, как скальпель и пинцет
Несмотря на то, что с момента одного из первых сообщений о применении дренирования тонкой кишки при лечении паралитической непроходимости прошло шестьдесят лет, широкое распространение этот метод получил в последние два десятилетия. Это стало возможным благодаря глубокому изучению лечебных возможностей дренирования тонкой кишки и внутрикишечной чрез-зондовой терапии, а также совершенствованию методов и техники интубации, улучшению конструкции энтеростомических зондов и использованию при их изготовлении высококачественных полимерных материалов. Установлено, что лечебный эффект дренирования тонкой кишки не ограничивается устранением внутрикишечной гипертензии и удалением токсичных веществ из кишки. Экспериментально установлено и клинически подтверждено, что длительное дренирование тонкой кишки улучшает микроциркуляцию и кровоснабжение слизистой оболочки, снижает общую интоксикацию и токсемию, способствует устранению дистрофических изменений в стенке кишки, уменьшает транссудацию в ее просвет жидкости, восстанавливает двигательную активность и всасывательную способность, предупреждает рецидивы паралитической и спаечной кишечной непроходимости.
Различают однократное опорожнение тонкой кишки и длительное ее дренирование. Однократное опорожение производится во время операции.
Длительное дренирование может быть выполнено как неоперационным, так и операционным способами. Неоперационные способы включают: дренирование тонкой кишки с помощью зондов типа Миллер-Эббота, назоэнтеральную эндоскопическую интубацию и интубацию толстой и тонкой кишок трансректальным способом. В свою очередь операционные способы дренирования подразделяются на закрытые, которые осуществляются без вскрытия просвета желудочно-кишечного тракта, и открытые, когда дренирование тонкой кишки связано с формированием искусственных свищей желудка или кишечника. Кроме того, дренирование тонкой кишки подразделяется на антеградное и ретроградное. При антеградном дренировании интубация осуществляется со стороны верхних отделов пищеварительного тракта в аборальном (каудаль-ном) направлении, при ретроградном — кишка интубируется снизу вверх. К закрытым операционным способам относятся назоэнте-ральное дренирование и трансректальная интубация тонкой киш-
__________________ 69
операционным — дренирование тонкой кишки, энтеростому и цекостому, В отдельную группу комбинированные способы, которые предусмат-раздельное дренирование верхних и нижних отделов тон- - кшпкиГа также сквозное дренирование всего кишечника. При «бинированном дренировании одновременно может быть вьшол- Ж открытая и закрытая, а также антеградная и ретроградная интубация кишки.
21 НЕОПЕРАЦИОННЫЕ СПОСОБЫ ДРЕНИРОВАНИЯ ТОНКОЙ КИШКИ
| V» |
Неоперационный способ дренирования тонкой кишки с помощью зондов типа Миллер-Эббота. Т.МШег и W.Abbott в 1934 году сообщили об успешном применении в целях декомпрессии тонкой кишки специального зонда, который представляет собой длинную (до 3,5 м) мягкую резиновую трубку диаметром до 1,5 см с одним или несколькими боковыми отверстиями на конце. Концевая часть зонда снабжена манжеткой, которая раздувается по мере продвижения зонда по желудочно-кишечному тракту. Больной заглатывает зонд и укладывается на правый бок. Постоянно отсасывая содержимое желудка и тонкой кишки, зонд постепенно, через каждые 30—40 мин продвигается на 5—7 см. Положение зонда в кишечнике контролируется с помощью рентгенологического исследования. Перистальтические волны, проталкивая раздуваемую манжету в аборальном направлении, обеспечивают продвижение зонда до нужного уровня. Вся процедура дренирования тонкой кишки занимает три-четыре часа. Последующее усовершенствование зонда путем замены резиновой манжеты баллончиком со ртутью (зонд Кантора) способствовало более быстрому его продвижению по кишечнику.
По мнению Ю.М.Дедерера и соавт. (1971), этот метод может оказаться эффективным лишь при наличии перистальтической активности кишечника. Кроме того, он требует продолжительных и сложных манипуляций, связанных с переменой положения тяжелобольных и частыми контрольными рентгенологическими исследованиями, но при этом удачные попытки заведения зонда в тощую кишку не превышают 60%. R.E.Brolin et al. (1987) считают, что применение закрытого метода дренирования с помощью зонда Миллер-Эббота показано при наличии частичной проходимости. При этом различие между непроходимостью и частичной проходимостью основывается на трактовке рентгенограмм живота.

|
 |
ГЛАВА
 Основным рентгенологическим признаком авторы считают определение газа в тонкой и толстое кишках. Полная непроходимость характеризуется наличием газа в тонкой кишке с уровнями жид. кости и отсутствием газа в толстой кишке, тогда как в случаях частичной проходимости наряду с раздутыми петлями тонкой кишки имеется газ в толстой. Эффект лечения после заведения зонда в кишку оценивается в течение первых 6—12 часов. Оперативное вмешательство потребовалось 38 из 193 (19%) больных с частичной проходимостью и 125 из 149 (84%) больных с рентгенологическими признаками полной непроходимости.
Основным рентгенологическим признаком авторы считают определение газа в тонкой и толстое кишках. Полная непроходимость характеризуется наличием газа в тонкой кишке с уровнями жид. кости и отсутствием газа в толстой кишке, тогда как в случаях частичной проходимости наряду с раздутыми петлями тонкой кишки имеется газ в толстой. Эффект лечения после заведения зонда в кишку оценивается в течение первых 6—12 часов. Оперативное вмешательство потребовалось 38 из 193 (19%) больных с частичной проходимостью и 125 из 149 (84%) больных с рентгенологическими признаками полной непроходимости.
Хорошие результаты от неоперационной декомпрессии тонкой кишки получены F.G.Quatromoni et al. (1989) у 41 больного с послеоперационной тонкокишечной непроходимостью. У10 больных, которые были повторно оперированы, диагностирована механическая форма непроходимости, у одного — причиной стойкого пареза являлся абсцесс брюшной полости.
Имеются сообщения об успешном лечении с помощью зондов Миллер-Эббота и Кантора больных со спаечной кишечной непроходимостью (Норенберг-Чарквиани А.Е., 1969; Hofstter S.R., 1981; Wolfson P. et al., 1985).
Заведение ригидного зонда с оливой в двенадцатиперстную и тощую кишки широко применяется для экстренной зондовой энте-рографии при диагностике острой кишечной непроходимости. Зонд в таких случаях снабжается металлическим проводником, конец которого располагается на 10 см проксимальнее начальной части зонда. Продвижение зонда из желудка в двенацатиперстную кишку контролируется рентгеноскопически. Прохождению зонда через привратник способствуют глубокие дыхательные движения, а также положение больного на правом боку с поворотом на живот. Для устранения спазма пилорического жома подкожно вводится 1 мл прозерина. После того, как зонд проходит за связку Трей-ца, металлический проводник извлекается. В просвет кишки вводится от 500 до 1000 мл 20% взвеси бария сульфата. Как правило, 20—30-минутное рентгенологическое исследование дает полную информацию о характере непроходимости (Ерюхин И.А., Зубарев П.Н., 1980). При неясной картине рентгенографическое исследование повторяется через два часа. По данным К.Д.Тоскина и А.Н.Пака (1988), диагностическая эффективность зондовой деком-прессионнои энтерографии составляет 96,5%. Обнаружение следов или скопление бариевой взвеси в слепой кишке, а также изображение рельефа слизистой оболочки толстой кишки на рентгенограммах отвергают острую непроходимость. Зонд в таких случаях вы-
ГЛАВА_£.
 няет декомпрессионную функцию и используется для введения б
няет декомпрессионную функцию и используется для введения б
роср
В связи с широким внедрением фиброскопическои техники в яяическую практику появилась возможность неоперационного азоэнтерального эндоскопического дренирования начальных отделов тонкой кишки. К настоящему времени разработаны два особа заведения зонда в тонкую кишку с помощью фиброскопа: через инструментальный канал аппарата и параллельно с ним под визуальным контролем.
В первом случае заведение зонда осуществляется для энтераль-ного питания и чреззондовой внутрикишечной коррекции метаболических нарушений. Диаметр просвета зонда в этом случае составляет 0,2 см, что вполне достаточно для проведения инфузий. Второй способ предусматривает заведение зонда для декомпрессии начальных отделов тонкой кишки и требует применения зондов диаметром просвета от 0,4 до 0,8 см.
В обоих случаях манипуляции осуществляется врачом-эндоскопистом. По мнению Ю.М.Панцырева и Ю.И.Галлингера (1984), методика введения зонда по инструментальному каналу эндоскопа более эффективна и безопасна по сравнению со способом проведения зонда параллельно с эндоскопом. Из 111 наблюдений ни в одном авторы не наблюдали каких-либо осложнений. Число неудачных попыток не превышает 1,3%.
Показанием для проведения зонда через инструментальный канал эндоскопа являются органические или функциональные нарушения проходимости гастродуоденальной зоны пищеварительного тракта (язвенный или опухолевый стеноз, нарушение пассажа через гастроэнтеро- или гастродуоденальное соустья, атония желудка, послеоперационный панкреатит и др.).
Анестезия слизистой глотки и премедикация осуществляются в объеме, обычном для диагностической гастродуоденоскопии. Вначале проводится осмотр слизистой оболочки желудка и двенадцатиперстной кишки, устанавливается причина нарушения проходимости. При сохраненном дуоденальном пассаже кончиком эндоскопа достигается нижнегоризонтальный отдел двенадцатиперстной кишки, после чего через инструментальный канал вводится кишечный зонд. По мере продвижения зонда в просвет кишки эндоскоп извлекается. У больных с гастроэнтероанастомозом эндоскоп проводится на 40—50 см в отводящую петлю тощей кишки Дистальнее соустья. Если через область сужения эндоскоп провести не удается, то следует попытаться провести зонд через видимое отверстие. Необходимо отметить, что у больных после резекции
fin'
 |
ГЛАВА
 желудка с атонией культи и отеком области анастомоза найти со устье не представляет трудности. При раздувании воздухом оно легко открывается и свободно преодолевается эндоскопом. Така* же ситуация может возникнуть при формировании пилоропласти-ки двухрядным швом и послеоперационном панкреатите. При явлениях анастомозита эндоскоп проводится путем осторожного раздвигания стенок анастомоза. После извлечения эндоскопа свободный конец зонда проводится через носовой ход и фиксируется к коже лица лейкопластырем или подшивается к крылу носа. В желудок дополнительно заводится зонд. Перед введением питательных смесей и инфузионных растворов положение зонда и его проходимость контролируются рентгенологически с использованием жидких рентгеноконтрастных веществ.
желудка с атонией культи и отеком области анастомоза найти со устье не представляет трудности. При раздувании воздухом оно легко открывается и свободно преодолевается эндоскопом. Така* же ситуация может возникнуть при формировании пилоропласти-ки двухрядным швом и послеоперационном панкреатите. При явлениях анастомозита эндоскоп проводится путем осторожного раздвигания стенок анастомоза. После извлечения эндоскопа свободный конец зонда проводится через носовой ход и фиксируется к коже лица лейкопластырем или подшивается к крылу носа. В желудок дополнительно заводится зонд. Перед введением питательных смесей и инфузионных растворов положение зонда и его проходимость контролируются рентгенологически с использованием жидких рентгеноконтрастных веществ.
Эндоскопическое декомпрессионное дренирование начальных отделов тонкой кишки проводится при уверенности в отсутствии. необходимости экстренного оперативного вмешательства. По мнению R.E.Brolin et al. (1987), основным показанием для его выполнения является необходимость срочной дифференциальной диагностики между острой тонкокишечной непроходимостью и другими заболеваниями, которые сопровождаются нарушением пассажа по тонкой кишке. G.F.Gowen et al. (1987) и L.Stilianu et al. (1988) ставят более широкие показания к эндоскопическому дренированию тонкой кишки и рекомендуют проведение декомпрессионного зонда как этап предоперационной подготовки в большинстве случаев кишечной непроходимости. Это позволяет, по мнению авторов, избежать напрасных лапаротомий, обезопасить проведение эндотрахеального наркоза, менее травматично проводить ревизию органов брюшной полости и тем самым сократить продолжительность хирургического вмешательства. Как свидетельствуют данные Т.П.Гурчумелидзе и соавт. (1990), наибольшего успеха с помощью эндоскопической интубации можно добиться при лечении больных с послеоперационным парезом или ранней спаечной тонкокишечной непроходимостью. Авторами у 40 из 54 больных послеоперационная тонкокишечная непроходимость была разрешена эндроскопическим заведением зонда в проксимальные отделы тощей кишки. Остальным больным оперативное вмешательство было выполнено в сроки от 12 до 48 часов ввиду отсутствия положительной динамики.
В то же время следует считать нецелесообразным применение данного метода больным с явной клиникой механической кишечной непроходимости, при подозрении на нарушение кровообращения в стенке кишки, при перитоните.
 "тГя проведения декомпрессионных зондов следует использо-
"тГя проведения декомпрессионных зондов следует использо-
"Ллисие и длинные гастроинтестинальные аппараты (GIF-P3, *SqGIF-QW, GIF-D4 фирмы «Olympus», ТХ-7, ТХ-8 slim фирмы ACM» или их аналоги).
•^ jq в.синев и соавт. (1988) предлагают предварительно встав канал зонда металлическую струну, что позволяет манипу- кончиком зонда. Жесткость зонда уменьшается путем Постепенного извлечения струны. Ю.М.Панцырев и К) И.Галлингер (1984) рекомендуют в начальной части зонд прошивать 5—6 шелковыми лигатурами или накладывать тесемки, которые располагаются на расстоянии 4—5 см друг от друга. Они служат для захвата их биопсийными щипцами. Таким образом можно легко придать нужные направления начальной части зонда, особенно при проведении его из желудка через изгибы двенадцатиперстной кишки.
Перед началом эндоскопического дренирования желудок опорожняется.
В положении на левом боку через носовой ход в кардиальный отдел желудка проводится кишечный зонд диаметром 0,6—0,8 см.
В желудок вводится фиброскоп и под контролем зрения зонд продвигается к привратнику.
Непременным условием успешного проведения зонда вдоль большой кривизны к пилорическому каналу является хорошее расправление воздухом желудка. Наличие фиксированных к зонду лигатур облегчает продвижение зонда в двенадцатиперстную кишку. Для этого используется следующий прием. После обнаружения начального конца зонда биопсийными щипцами захватывается первая лигатура, подтягиванием за нее зонд прижимается к эндоскопу и в таком положении проводится в двенадцатиперстную кишку. После снятия биопсийных щипцов с лигатуры эндоскоп возвращается в желудок, где производится захват следующей лигатуры. Манипуляцию повторяют до тех пор, пока зонд не дойдет до нижнего горизонтального отдела двенадцатиперстной кишки или не пройдет за связку Трейца. При отсутствии фиксированных к зонду лигатур зонд захватывается щипцами за боковые отверстия.
Убедившись, что зонд проведен в тонкую кишку, эндоскоп удаляют. После удаления эндоскопа из зонда извлекается струна. Положение зонда и состояние кишки контролируются с помощью рентгенологического исследования. Для облегчения проведения зонда Ю.М.Панцыревым и Ю.И.Галлингером (1984) разработана эндоскопическая методика интубации по металлическому напра-вителю. Эндоскоп под контролем зрения максимально проводится

 в двенадцатиперстную кишку. Затем через___ г#—«»-«дыай
в двенадцатиперстную кишку. Затем через___ г#—«»-«дыай
нал в просвет кишки вводится длинный и жесткий с закрут ** ным концом металлический спиралевидный зонд — провод ' диаметром 0,2 см. Эндоскоп извлекается, а кишечный зонд наи зывается на металлический проводник и вводится по нему в той кую кишку.
Дренирование с помощью фиброскопа обычно удовлетвори тельно переносится больными и занимает сравнительно непродолжительное время — от 10 до 30 мин. Наибольшие трудности возникают при прохождении зондом области связки Трейца. Облегчить эту манипуляцию позволяет использование зонда с воздушным баллончиком на начальной его части (GowenG.F. etal., 1987). Зонд заводится до нисходящей части двенадцатиперстной кишки. Баллончик раздувается, и дальнейшее продвижение зонда осуществляется за счет перистальтических волн, возникающих по мере опорожнения кишки. Тем не менее, Т. П. Гурчумелидзе и соавт. (1990) считают интубацию завершенной лишь в том случае, когда кончик зонда находится дистальнее связки Трейца или на уровне дуоденоеюнальной складки. Проведенный ими анализ серийных рентгенограмм показал постепенную спонтанную миграцию зонда в диотальном направлении.
Обязательным условием после окончания дренирования является активная декомпрессия кишки. Для этой цели Б.Г.Смольский и соавт. (1980) и Ю.В.Синев и соавт. (1988) предложили использовать зонд, имеющий два канала — перфузионный и аспирацион-ный. Оба канала открываются на разных уровнях в просвете кишки, что дает возможность проводить не только декомпрессию, но и активный кишечный диализ или энтеросорбцию.
При адекватной декомпрессии начальных отделов тонкой кишки в течение первых суток после интубации количество аспираци-онного содержимого при создании отрицательного давления в 30—40 мм вод.ст. составляет-не менее 1500 мл, на вторые сутки — около 1000 мл, на третьи — 800 мл.
Кроме того, двухпросветный зонд позволяет обследовать пищеварительную и всасывающую функцию верхних отделов тонкой кишки и в соответствии с данными обследования осуществлять подбор сред для энтерального питания.
Неоперационная трансректальная декомпрессия толстой и тонкой кишок чаще всего используется для разрешения обтураци-онной толстокишечной непроходимости или с целью устранения заворота сигмовидной кишки.
Полная обтурация кишки опухолью бывает редко, однако при-
«проходимости появляются при сужении просвета до ее део<5х0дИМ0 учитывать, что сужение кишки бывает & *0 не только самой опухолью, но и воспалением окружа-обуСЛ°тканей и отеком слизистой оболочки. Важное значение при г0111* еет функциональное состояние баугиниевой заслонки. В случаев она нормально функционирует даже при далеко за- формах толстокишечной непроходимости, а у 20% боль-^юдается ее функциональная несостоятельность, что ведет * чабросу толстокишечного содержимого в тонкую кишку, механическому ее перерастяжению и развитию пареза. Развившаяся таким образом толсто-тонкокишечная непроходимость усиливает эндогенную интоксикацию и токсемию и может сопровождаться развитием эндотоксинового шока.
Декомпрессию толстой кишки с помощью ректоскопа можно осуществить лишь при низкорасположенных опухолях прямой кишки. После очистительной клизмы больному производится рек-тороманоскопия, и через канал в стенозирующий просвет опухоли проводится обильно смоченный вазелиновым маслом желудочный зонд с двумя-тремя боковыми отверстиями и закругленным концом. При локализации опухоли выше 30 см от анального отверстия для выполнения декомпрессии можно воспользоваться фиброколо-носкопом. Однако промывание кишки через манипуляционный канал эндоскопа, как правило, малоэффективно. Чаще всего с помощью фиброколовоскопа отыскивается и расширяется место сужения и затем под контролем зрения через видимую щель канала проводится энтеростомическая трубка выше места препятствия. При этом можно воспользоваться теми же приемами, что и при эндоскопическом дренировании начальных отделов тонкой кишки. Эндоскоп через стенозйрующую опухоль можно провести в тех случаях, если она имеет экзофитный рост, а просвет деформирован за счет полиповидных разрастаний на поверхности опухоли. Для расширения просвета канала в опухоли предлагается использовать электро- и лазерную фотокоагуляции (Мамиконов И.Л. и Саввин Ю.Н., 1980). Однако необходимо помнить, что чрезмерно насильственные манипуляции могут вызвать повреждение стенки кишки и интенсивное кровотечение из опухоли.
По мере продвижения зонда содержимое толстой кишки эвакуируется шприцем Жане или с помощью вакуумного отсоса. В большинстве случаев без контроля фиброколоноскопа пройти зондом селезеночный или печеночный изгибы ободочной кишки не представляется возможным. Однако для декомпрессии толстой кишки и разрешения непроходимости часто бывает достаточным опорож-

|
 _76__________________________________________ ГЛАВА 2
_76__________________________________________ ГЛАВА 2
нение диетальных ее отделов. Зонд из просвета кишечника извлекается на вторые сутки.
Дренирование тонкой кишки путем проведения зонда через баугиниеву заслонку с помощью фиброколоноскопа пока рассматривается лишь теоретически и в ближайшее время вряд ли найдет широкое клиническое применение. По данным Ю. В. Синева и соавт. (1988)» заведение зонда таким образом в дистальные отделы тонкой кишки становится возможным лишь при тщательном опорожнении толстой кишки от содержимого. При этом через биоп-сийный канал диаметром 0,5 см можно провести эятеростомичес-кий зонд с просветом не более 0,3 см, что недостаточно для полноценной декомпрессии.
2.2. ОПЕРАЦИОННЫЕ СПОСОБЫ ДРЕНИРОВАНИЯ ТОНКОЙ КИШКИ
2.2.1. Однократные способы декомпрессии тонкой кишки
Существуют различные способы однократного опорожнения тонкой кишки во время операции.
В одних случаях декомпрессия тонкой кишки осуществляется без вскрытия ее просвета путем последовательного выдавливания («сдаивания») содержимого ретроградно в желудок или чаще — антеградно в толстую кишку. Несмотря на то, что большинство авторов высказывается против такого метода, считая его травматичным и малоэффективным, существуют и его сторонники. Так, П.Д.Рогаль и А.А.Пляпук (1977) у больных кишечной непроходимостью рекомнедуют применять щадящую методику однократного перемещения содержимого кишечника в нижележащие отделы.

|
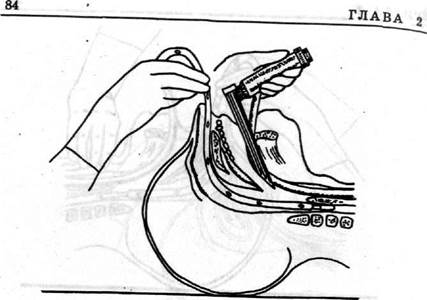
| Рис. 17. Перемещение содержимого кишки методом«сдаивания» |
 ГГ дсостоит в том, что после устранения причины непроходимое -перирующий хирург влажной марлевой салфеткой удерживает 111 лю кишки между первым и остальными пальцами левой кисти, П гякрывая ее просвет, а между вторым и третьим пальцами пра-аой РУ«И протягивает ее, легко сближая стенки (рис.17). Таким пбоазом содержимое кишечника передвигается в нижележащие отделы. В это время ассистент перехватывает освобожденную от содержимого кишку через каждые 15—20 см.
ГГ дсостоит в том, что после устранения причины непроходимое -перирующий хирург влажной марлевой салфеткой удерживает 111 лю кишки между первым и остальными пальцами левой кисти, П гякрывая ее просвет, а между вторым и третьим пальцами пра-аой РУ«И протягивает ее, легко сближая стенки (рис.17). Таким пбоазом содержимое кишечника передвигается в нижележащие отделы. В это время ассистент перехватывает освобожденную от содержимого кишку через каждые 15—20 см.
Б некоторых случаях для освобождения кишки от содержимого ее пунктируют толстой иглой. Однако таким способом не всегда удается освободить даже отдельную петлю кишки от газов и тем более от жидкого содержимого. Для того, чтобы добиться достаточного опорожнения кишечника, его необходимо пунктировать во многих местах, что малоэффективно и опасно в отношении инфицирования брюшной полости. Поэтому этот метод применяется
. '

| Рис, 18. Однократная декомпрессия кишки спомощью специальносконструнро ванн ого троакара(по Ю.М. Дедереру.) |
-
fti ">

|
| ГЛАВд |
L_
Рис 19. Опорожнение тонкой кншкн е помощью электроотсоса,
очень редко. Значительно чаще для этой цели используют специально сконструированный троакар с двумя боковыми отверстиями (Дедерер Ю.М., 1971). Одно из них с широким просветом подсоединяется к электроотсосу, второе меньших размеров, служит для промывания трубки, если она забивается плотным содержимым. Стилетом троакара прокалывается стенка перерастянутой тонкой кишки в центре предварительно наложенного кисетного шва. Стилет поднимается в верхнее положение, а гильза продвигается по просвету кишки (рис.18). Кишечное содержимое эвакуируют с помощью электроотсоса. Для опорожнения близлежащих петель производится либо «сдаивание» кишечного содержимого к месту пункции, либо в кишку вводится зонд через торцевое отверстие троакара. После эвакуации кишечного содержимого троакар извлекается, кисетный шов затягивается, и дополнительно накладываются два-три серозно-мышечных шва.
Многие хирурги для опорожнения тонкой кишки производят энтеротомию. Между двумя нитями-держалками вводят в просвет кишки наконечник электроотсоса и с его помощью сначала освобождают ближайшие участки кишки, а затем на наконечник отсоса нанизывают другие перерастянутые петли кишки (рис.19). N.Balsano и M.Reynolds (1970) для аспирации содержимого из тонкой кишки предложили использовать катетер Фоллея № 22. Бал-

|
■
Рнс. 20. Однократное опорожнение кншкн катетером Фоллея.
лон катетера наполняется 3 мл воды, что обеспечивает его свободное продвижение, препятствует присасыванию слизистой оболочки к отверстию зонда и предотвращает подтекание тонкокишечного содержимого через энтеротомическое отверстие помимо зонда (рис.20). По окончании процедуры отверстие в кишке зашивается в поперечном направлении двухрядным швом.
Опорожнение тонкой кишки через один из концов резецированного ее участка — достаточно распросраненный способ однократной декомпрессии. Удаление содержимого кишки при этом осуществляется с помощью наконечника электроотсоса или путем проведения в просвет кишки зонда. После опорожнения кишки восстанавливается ее непрерывность или проксимальный конец выводится наружу в виде энтеростомы.
Несмотря на кажущуюся простоту перечисленные методы имеют ряд существенных недостатков. Они не асептичны и могут привести к микробному загрязнению операционного поля. Этими способами можно опорожнить только ближайшие петли кишки. Кроме этого, возникает опасность несостоятельности швов, наложенных на измененную стенку кишки. Поэтому вполне оправданы рекомендации производить однократную декомпрессию тонкой кишки закрытыми способами трансназально или трансректально.
ГЛАВА
2.2.2. Назоэнтеральное дренирование
Серийный выпуск стандартных назоэнтеральных зондов, о ствие необходимости специального вскрытия просвета полых o нов и формирования наружных желудочных или кишечных щей позволили рекомендовать назоэнтеральное дренирование» качестве метода выбора для профилактики и лечения энтеральной недостаточности.
С этой целью в настоящее время используются зонды, изготовленные из прочного эластичного материала, устойчивые к воздействию желудочного и кишечного содержимого, обладающие термолабильностью, рентгеноконтрастностыо и не содержащие в своем составе вредных химических примесей. Их диаметр не превышает 1,2 см, просвет канала — 0,8 см. «Рабочая часть» зонда с нанесенными через 6—8 см боковыми отверстиями имеет протяженность 160—170 см при общей длине 250—300 см. Конец зонда оснащен проводником в виде оливы, которая изготовлена из того же материала, имеет такой же диаметр и гантелевидно соединена с основной частью зонда (рис.21). При температуре 37°С и выше зонд становится мягким и не травмирует кишечную стенку. При отсутствии стандартного зонда назоэнтеральное дренирование может быть выполнено с помощью длинной (250—300см) резиновой или силиконовой трубки с просветом 0,4—0,8 см. Для придания зонду упругости в его просвет проводится мандрен из нержавеющей проволоки. Начальная часть зонда закрывается выкроенной из резины или силикона заглушкой, что делает манипуляции безопасными. Конец мандрена целесообразно выполнить в виде оливообразного утолщения, что в значительной степени уменьшает травмирование слизистой оболочки при проведении зонда по просвету пищевода, желудка и двенадцатиперстной кишке. Для свободного скольжения проводника внутренняя поверхность зонда смазывается вазелиновым маслом или глицерином. В качестве проводника могут быть использованы биопсииные щипцы фиброгастродуоденоскопа или фторопластовый катетер диаметром от 0,2 до 0,3 см.
Имеются сообщения о дренировании тонкой кишки с помощью растворимого зонда, созданного из синтетического белка (Jung D. et al.» 1988). Растворение зонда в просвете кишки наступает на 4-й день от момента интубации. Авторы использовали зонд при лечении 52 больных со спаечной кишечной непроходимостью. Осложнений, связанных с пребыванием такого зонда в просвете кишки и желудка, а также рецидивов спаечной непроходимости не наблюдалось.
После принятия решения о назоэнтеральном дренировании хирург

Рис. 21. Одиопросветный назоэнтеральный зонд.
ревизует верхний отдел брюшной полости. Освобождает подпеченочное пространство от спаек и сращений. Палышторно оценивает состояние брюшного отдела пищевода, желудка и двенадцатиперстной кишки. Осматривает область дуоденоеюнального изгиба.
При спаечном процессе тонкая кишка выделяется во всем протяжении. Десерозированные участки ушиваются до начала интубации. При наличии опухоли кардиопищеводной зоны, хронической язвы желудка или двенадцатиперстной кишки, стенозирую-щей опухоли выходного отдела желудка следует отказаться от проведения зонда через желудок и выполнить интубацию тонкой кишки одним из ретроградных способов.
Перед заведением кишечного зонда в пищевод анестезиолог контролирует растяжение манжеты эндотрахеальной трубки. Зон-Дом опорожняется желудок. Достигаются полная релаксация и глубина наркоза. Олива кишечного зонда обильно смазывается вазелиновым маслом, а свободный его конец присоединяется к системе электроотсоса.
Анестезиологом через наружное отверстие носового хода зонд продвигается в пищевод. Можно вводить зонд и через рот. Однако в послеоперационном периоде такое положение зонда может вызвать рвоту и нарушить акт глотания. Поэтому после окончания интубации свободный конец зонда переводится в носовой ход (рис.22).
■

|
| смешением кверху щитоввдвотв хряща. |
| . |

|
Рис. 22. Перевод назоэвтералыогозонда из ротовой полости водин из восовых ходов.
В 80% случаев зонд без особых усилий вводится в пищевод. Но иногда возникают трудности при интубации, обусловленные давлением интубированной трахеи на переднюю стенку пищевода, недостаточной или чрезмерной упругостью зонда, узким носовым ходом, искривлением носовой перегородки,
Для устранения сдавления пищевода интубированной трахеей эффективным может оказаться смещение кверху щитовидного хряща (рис.23). При отсутствии эффекта можно воспользоваться следующим приемом. Указательный палец правой руки заводится в полость рта, нащупывается кончик зонда и прижимается к задней стенке глотки, и зонд проталкивается в пищевод (рис,24).Иногда проведение зонда контролируется с помощью ларингоскопа (рис.25).
Ю.П.Свиргуненко и соавт. (1982) и Б.К.Шуркалин и соавт. (1986) для успешного продвижения зонда по пищеводу предложили интубировать его эндотрахеальной трубкой (рис.26). По мнению авторов, эндотрахеальная трубка, установленная в пищеводе, надежно выполняет роль проводника» облегчает проведение зонда в желудок и предохраняет слизистую носоглотки и пищевода от пов-
 |
|

|
 Рис 25. Проведение назоэнтералиого зонда в пищевод под
Рис 25. Проведение назоэнтералиого зонда в пищевод под
ларингоскопа.
2,
| г |
контролем
| гл. |
 Кроме того, с помощью надувной манжеты дыхатель-^ггИ Защищаются от попадания в них желудочно-кишечного
Кроме того, с помощью надувной манжеты дыхатель-^ггИ Защищаются от попадания в них желудочно-кишечного
| яые |
ыепЖИмого. С такой же целью Е.С.Бабиев (1983) предложил ис-%ивать зонд-проводник длиной до 100 см и диаметром 1,5 см.
' го просвет вводится начальная часть кишечного зонда, после го оба зонда продвигаются в желудок. Зонд-проводник удаляется
осле того* как конец наэоиятестинального зонда с боковыми отверстиями оказывается в двенадцатиперстной кишке. В Г.Дорофееев и соавт. (1986) в качестве зонда-проводника с успехом используют толстый резиновый желудочный'зонд.
В.В.Изосимов и В.А.Борисенко (1984) рекомендуют проводить зонд-проводник по всей длине тонкой кишки. В качестве кишечного зонда используется тонкая полихлорвиниловая трубка. Зонд-проводник удаляется после окончания интубации. П.Ю.Плевокас (1989) в значительной степени усовершенствовал зонд-проводник, снабдив его металлическими кольцами. Кольца создают на стенке зонда выступы, удобные для захвата, удержания и проведения зонда по кишке. Длина зонда-проводника составляет 170—200 см, наружный диаметр —1,2 см. Внутренняя трубка, которая оставляется в просвете кишки для ее декомрессии, имеет длину 300—350 см, а диаметр — 0,5 см.
По мере продвижения зонда хирург со стороны брюшной полости направляет его вдоль большой кривизны желудка и правой рукой фиксирует в области выходного отдела. Левой рукой конец зонда направляется через привратник в луковицу двенадцатиперстной кишки. Нередко спазм пилорического жома мешает продвижению зонда. Причиной этому могут быть травматичные манипуляции и отсутствие согласованных действий хирурга и анестезиолога. В таких случаях помочь манипулировать зондом может следующий прием. Правой рукой через переднюю стенку желудка на границе его тела и антрального отдела зонд захватывается на расстоянии 2—3 см от оливы. Пилорический жом фиксируется двумя пальцами левой руки со стороны двенадцатиперстной кишки. Кольцо пилорического жома под контролем пальцев левой руки «нанизывается» на оливу зонда (рис.27). Как только конец зонда окажется в луковице двенадцатиперстной кишки, хирург правой рукой синхронно с движениями анестезиолога продвигает энтерос-томическую трубку в дистальном направлении. Пальцами же левой руки контролирует и направляет ее конец вниз и кзади до нижнего горизонтального изгиба и далее влево по направлению к связке Трейца.
Форсирование продвижения зонда по кишке при ощущении
 | |||
 |

|
| ________ |
| ГЛАВА 2 |
| " |
Рис. 27. Проведение зонда в двенадцатиперстную кишку.
препятствия недопустимо. В таких случаях двенадцатиперстная кишка мобилизуется по Кохеру (рис.28).
При появлении зонда в начальном отделе тощей кишки он за' хватывается тремя пальцами правой руки и продвигается на 10—15 см. В желудке зонд укладывается по ходу малой кривизны.
Препятствием продвижению зонда в области дуоденоеюнально-го перехода могут быть дополнительные изгибы начального отдела тощей кишки, фиксированные связочным аппаратом брюшины или спайками. В таких случаях следует попытаться захватить оливу зонда и нанизывающими движениями провести ее в дистальном направлении (рис. 29).
Для удобства захвата зонда через стенку кишки рекомендовав ряд приспособлений. Так, А.Л.Прусов и Н.С.Пошшдопуло (1983) предложили через каждые 4 см на «рабочую часть» зонда надевать кольца из красной резины. Интубацию осуществляют через рот. После ее завершения зонд переводят в один из носовых ходов. А.И.Антух (1991) для формирования утолщений использует пищевод желатин. По данным автора, желатиновые муфты под действием кишечных соков на третьи сутки растворяются и не мешают извлечению зонда. С этой же целью было предложено снабжать начальную часть зонда одной или несколькими манжетками из

Рис. 28. Проведение зонда к связке Тренда.
латексной резины (зонд Миллер-Эббота) (Nelson R.L., Nyhys L.M., 1979; Seidmon E.J. et al., 1984). Манжеты раздуваются в желудке и таким образом создаются удобства при проведении зонда через изгибы Двенадцатиперстной кишки.
Для облегчения интубации кишки и профилактики повреждений некоторые авторы раздувают ее кислородом или воздухом (Прусов А.Л.,ПапандопулоН.С, 1983; Веллер Д.Г. с соавт., 1985). С этой целью перед интубацией в просвет зонда проводится тонкая полихлорвиниловая трубка диаметром 2—2,5 мм с несколькими боковыми отверстиями в ее начальной части, через которую во вРемя интубации подается кислород или воздух. С помощью указанного приема Д-Г.Веллеру и соавт. (1985) удалось значительно Уменьшить травму кишки, а саму процедуру дренирования выпол-Вять в течение 30 минут.
Если зонд сворачивается в желудке в виде колец, то расправить 6141 Удается гофрированием начального отдела тонкой кишки с пос-
 Рис. 29. Проведение зоняа в начальный отдел тонкой кишки-
Рис. 29. Проведение зоняа в начальный отдел тонкой кишки-
ледующим подтягиванием зонда в дистальном направлении. Менее выгодным является подтягивание зонда анестезиологом.
При отсутствии пареза кишки (рис.ЗО) зонд продвигается за счет «нанизывания» на него кишечных петель. Сгофрировав 8—10 см кишки, хирург синхронно с анестезиологом проталкивает зовд, расправляя кишку в проксимальном направлении. Интубацию кишки в таких случаях можно ускорить* если хирург будет мани-
Рнс. 30. Проведение назоэнтерального зонда по просвету кишки.
пулировать в области связки Трейца, а ассистент направлять оливу зонда по просвету кишки.
Трансназальную интубацию следует считать завершенной при появлении последнего бокового отверстия зонда в начальном отделе тощей кишки (рис.31).
Дренирование тонкой кишки трансназальным способом осуществляется в большинстве случаев на всем ее протяжении (тотальное назоэнтеральное дренирование). Однако имеются сообщения (Гауенс Я.К. с соавт., 1985; Пашкевич И.Ф., Шестопалов А.Е., 1989; Werner R. et al., 1984) об успешной длительной декомпрессии тонкой кишки путем дренирования только начального ее отдела на протяжении 20—70 см (проксимальное назоэнтеральное Дренирование). В этих целях сотрудниками Московского городского НИИ скорой помощи им. КВ.Склифосовского разработан ^Ухканальный полифункциональный назоэнтеральный зонд с несколькими отверстиями в дистальной его части. Зонд заводится во вРемя операции за связку Трейца на 50—70 см. Аспирация кишечного ^ЭДбржимого осуществляется через один из каналов зонда путем созда-авя вакуума в 20—40 мм вод.ст.
Однако добиться таким образом адекватной декомпрессии **Ппш возможно лишь при умеренном перитоните и сохраненной КВ1печной перистальтике. В условиях стойкого пареза кишечника
 |
| - | ||

Рис. 81. Положение назоэнтеральиого зонда в пищеварительном тракте-
необходима интубация всей тонкой кишки. В связи с этим Н.С.Утешев и соавт. (1985) предложили выполнять вначале тотальную интубацию тонкой кишки, а после ее опорожнения заводить двухпросветный зонд на 50 см за связку Трейца.
Следует отметить также» что даже в случаях тотальной интубации кишки вскоре после восстановления ее моторики происходят смещение начальной части зонда в проксимальном направления.
 91
91
*rvm сутки после операции при наличии перистальтической ео^ти зонд смешается на 15—20 см, а к пятым суткам инту-ВВ ыми остаются 2/3 тонкой кишки. Для удержания зонда в *^ положении M.Regent et al. (1974) и H.W.Waclawiczek ^iS?) считают необходимым проведение его за баугиниеву заслон-слепую кишку. При использовании зонда Миллер-Эббота?Кегп (1980) и L.Nitzche et E.Hutter (1984) его фиксацию осуществляли путем раздувания манжетки в слепой кишке. В таком положении авторы оставляли зонд в течение 7—8 суток.
 Невозможность одновременного раздельного дренирования тонкой кшпки и желудка является основным недостатком стандартных назоэнтеральных зондов. Разница внутрипросветного давления в тонкой кишке и желудке не только нарушает дренажную функцию зонда, но и приводит к застою желудочного и дуоденального содержимого, которое в результате пареза кишки и нарушения запирательной функции пилорического жома скапливается в желудке. Переполнение желудка усиливает рвотный рефлекс и требует дополнительного его опорожнения.
Невозможность одновременного раздельного дренирования тонкой кшпки и желудка является основным недостатком стандартных назоэнтеральных зондов. Разница внутрипросветного давления в тонкой кишке и желудке не только нарушает дренажную функцию зонда, но и приводит к застою желудочного и дуоденального содержимого, которое в результате пареза кишки и нарушения запирательной функции пилорического жома скапливается в желудке. Переполнение желудка усиливает рвотный рефлекс и требует дополнительного его опорожнения.
Так, из 114 наблюдаемых нами больных, которым в процессе трансназальной интубации по тем или иным причинам боковые отверстия зонда были оставлены в просвете желудка, у 67 (58%) дренажная функция зонда была возможна лишь при условии активной аспирации с помощью шприца Жане или вакуумного отсоса. Тем не менее, у 23 больных (20,8%) полноценной декомпрессии получить не удалось, и эвакуация содержимого желудка осуществлялась с помощью дополнительного зонда. Кроме того, этим больным невозможно было произвести полноценную интестиналь-ную терапию. Вводимые энтеросорбенты по пути наименьшего сопротивления через боковые отверстия прежде всего попадают в желудок.
Рвота при дренировании однопросветным зондом отмечена у 36% больных. При этом она возникала с одинаковой частотой как в случаях оставления боковых отверстий зонда в желудке, так и без них. Среди послеоперационных осложнений у этих больных чаще всего наблюдаются пневмония и гнойные трахеобронхиты, Удельный вес которых составляет 21,1% и 12,7%, соответственно (табл.22).
По данным аутопсий, регургитация желудочного содержимого ^Дыхательные пути во время рвоты явилась причиной смерти 5 °°льных, оперированных по поводу кишечной непроходимости.
В связи с этим при проведении назоэнтеральной интубации °Днопросветным зондом необходимо стремиться во время операции




Таблица 22 Частота послеоперационных ннфекциоино-воспалнтельных
осложнений со стороны дыхательных путей при трансназальном дренировании тонкой кишки
| Вид дренирования |
| пневмония |
Осложнени я Число
[наблюдеш
| S. 12,7 14,3 10,0 7,7 8,8 7,0 10,8 |
| 7о | число |
| 22,1 | |
| 21,4 | |
| 23,3 | |
| 12,1 | |
| 14,7 | |
| 10,5 | |
| 18,5 |
| 91 34 57, 249 |
| 35 21 11 5 |
Наэоэнтеральная интубация однопросветным зондом:
С оставлением отверстий
зонда в желудке
Без оставления отверстии
зонда в желудке Раздельное дренирование тонкой кишки и желудка:
Отдельными зондами
Двухпросветным наэогастро-
энтеральным зондом
Всего:
■ i i
Примечание. Зонд в просвете тонкой кишки у представленных групп больных находился не юнее трех суток послеоперационного периода.
заводить дополнительный зонд в желудок. С его помощью легко эвакуируется скапливающееся при интубации в желудке кишечное содержимое. Технически сложнее завести зонд в желудок при выполненной назоэнтеральной интубации. В таких случаях используется прием, при котором зонд продвигается в пищевод указательным пальцем, введенным в полость рта. Для придания зонду упругости в его просвет вводится металлическая струна. Свободные концы обоих зондов помещаются в один носовой ход и раздельно фиксируются к крыльям носа.
В исключительных случаях накладывается разгрузочная гастростома.
Раздельное дренирование тонкой кишки и желудка позволяет не только осуществлять декомпрессию желудочно-кишечного тракта, но и в полном объеме производить чреззондовую интести-вальную терапию. Однако, как показал опыт, дренирование тонкой кишки и желудка отдельными зондами имеет ряд недостатков. Больные тяжелее переносят нахождение двух зондов в глотке и
 При этом возникающее непреодолимое желание яосо»*-^^^ не останавливает даже подшивание их к крыльям яЗВЛвОсобенНО тяжело переносят нахождение двух зондов в иосог-я0СЙ* и пищеводе больные пожилого и старческого возрастов, стра-ЛОТ1п1ие хроническими заболеваниями сердечно-сосудистой и ды-дй!1льной систем. У этих больных большая вероятность возникно-1 пролежней пищевода, а нарушение замыкательной функции ^пдиального жома чаще, чем при дренировании одним зондом, приводит к рефлюкс-эзофагиту и срыгиванию желудочным содержимым. В связи с этим в отечественной и зарубежной литературе предлагались различные виды зондов с раздельным дренированием желудка и тонкой кишки (Гауенс Я.К. с соавт., 1986; Тамазаш-вили Т.Ш., 1986; Schmoz G, et al., 1983; Seidmon E.J. et al., 1984; Xaicala J. et al., 1985). Однако большинство из них имеет сложную техническую конструкцию и рекомендации многоразового использования, что малоприемлемо для стационаров, занимающихся неотложной абдоминальной хирургией. Так, в целях одновременного и раздельного дренирования желудка и тонкой кишки Т.Ш.Тамазашвили (1986) предложил использовать назоэнтераль-ный зонд, который на уровне тела желудка имеет камеру, снабженную шариковым клапаном. Клапан пропускает содержимое желудка и в то же время препятствует одновременному поступлению кишечного. Зонд, предложенный E.J.Seidmon et al. (1984), кроме двух каналов снабжен манжетами, одна из которых с целью предупреждения регургитации кишечного содержимого в желудок раздувается в просвете двенадцатиперстной кишки. Желудок дренируется через дополнительный канал зонда.
При этом возникающее непреодолимое желание яосо»*-^^^ не останавливает даже подшивание их к крыльям яЗВЛвОсобенНО тяжело переносят нахождение двух зондов в иосог-я0СЙ* и пищеводе больные пожилого и старческого возрастов, стра-ЛОТ1п1ие хроническими заболеваниями сердечно-сосудистой и ды-дй!1льной систем. У этих больных большая вероятность возникно-1 пролежней пищевода, а нарушение замыкательной функции ^пдиального жома чаще, чем при дренировании одним зондом, приводит к рефлюкс-эзофагиту и срыгиванию желудочным содержимым. В связи с этим в отечественной и зарубежной литературе предлагались различные виды зондов с раздельным дренированием желудка и тонкой кишки (Гауенс Я.К. с соавт., 1986; Тамазаш-вили Т.Ш., 1986; Schmoz G, et al., 1983; Seidmon E.J. et al., 1984; Xaicala J. et al., 1985). Однако большинство из них имеет сложную техническую конструкцию и рекомендации многоразового использования, что малоприемлемо для стационаров, занимающихся неотложной абдоминальной хирургией. Так, в целях одновременного и раздельного дренирования желудка и тонкой кишки Т.Ш.Тамазашвили (1986) предложил использовать назоэнтераль-ный зонд, который на уровне тела желудка имеет камеру, снабженную шариковым клапаном. Клапан пропускает содержимое желудка и в то же время препятствует одновременному поступлению кишечного. Зонд, предложенный E.J.Seidmon et al. (1984), кроме двух каналов снабжен манжетами, одна из которых с целью предупреждения регургитации кишечного содержимого в желудок раздувается в просвете двенадцатиперстной кишки. Желудок дренируется через дополнительный канал зонда.
Следует подчеркнуть, что основным недостатком предлагаемых многоканальных зондов является малый диаметр каналов, предназначенных для дренирования кишки и желудка. Как показали экспериментальные и клинические исследования, диаметр просвета, позволяющий осуществлять адекватную декомпрессию желудочно-кишечного тракта, должен быть не менее 0,4 см, что в настоящее время технически допустимо при изготовлении лишь двух-просветных зондов. Создание трех и более каналов ведет к увеличе-■**> диаметра зонда, что затрудняет проведение его через носовые *АЦы и пищевод.
В этой связи нами был разработан двухпросветный назогастро-энтеральный зонд для одновременного раздельного дренирования ловкой кишки и желудка (приоритетная справка на изобретение № 4935940 от 12.05.91) (рис.32, рис.33). Зонд представляет собой аластичную термолабильную и рентгеноконтрастную полихлорви-
| $2Ј~~~~~^ f~9 мм. В выходной части (С) каждый из каналов просвета ьнЫЙ> отличающийся друг от друга буквенным обозна-й*|ееТ °'йли цветом просвет. Предложенный двухпросветный назо-чеЯИеМ1ггеоальный зонд был использован при лечении 57 больных га(ГГ^ОЭиятом и кишечной непроходимостью. Зонд прост и удобен в пери1'*' и интубация им малотравматична. Время интубирова-8—15 мин. В послеоперационном периоде такой зонда поз-осуществлять одновременную и раздельную декомпрессию i и тонкой кишки, производить внутрикишечную терапию, видно из представленных в табл.22 данных, число пневмо <лт*п& гпжттептк TTOVXllDOCBeTHbH |
| Ркс 32. Технический рисунок двухпросветногояазогастроэвтерального зонд». |
 Рис. 33. Общий вид наэогастроэвтерального зонда в серийной изготовлении, ниловую трубку с заглушённым рабочим концом и булавовидной направляющей частью (А). Рабочая часть зонда содержит канал (Б) с 40—50 боковыми отверстиями, расположенными на расстоянии 5 см друг от друга, который служит для дренирования тонкой кишки, и канал (В), в начальной части которого имеются 3—4 отверстия для дренирования желудка. Переходная часть (Д) представляет собой цельную трубку длиной 30 см, что соответсвует длине двенадцатиперстной кишки. Она лишена боковых отверстий и является продолжением кишечного канала. Желудочный канал зонда в начальном отделе переходной части закрыт силиконовой втулкой, диаметр которой соответствует 1/2 просвета зонда. Длина рабочей части кишечного канала — от 1,6 м до 2 м. Диаметр
Рис. 33. Общий вид наэогастроэвтерального зонда в серийной изготовлении, ниловую трубку с заглушённым рабочим концом и булавовидной направляющей частью (А). Рабочая часть зонда содержит канал (Б) с 40—50 боковыми отверстиями, расположенными на расстоянии 5 см друг от друга, который служит для дренирования тонкой кишки, и канал (В), в начальной части которого имеются 3—4 отверстия для дренирования желудка. Переходная часть (Д) представляет собой цельную трубку длиной 30 см, что соответсвует длине двенадцатиперстной кишки. Она лишена боковых отверстий и является продолжением кишечного канала. Желудочный канал зонда в начальном отделе переходной части закрыт силиконовой втулкой, диаметр которой соответствует 1/2 просвета зонда. Длина рабочей части кишечного канала — от 1,6 м до 2 м. Диаметр
k видно из представленных в табл.22 дан, яяй у больных с дренированной тонкой кишкой двухпросветным нязогастроэнтеральным зондом снизилось до 10,5% и было достоверно меньше, чем в группах больных, которым осуществлялось дренирование однопросветным зондом или раздельно кишечным и желудочным зондами. Уменьшилось число гнойных трахеоброн-хитов. Это позволило расширить показания к интубации тонкой кишки трансназальным способом больным пожилого и старческого
возрастов.
В большинстве случаев больные плохо переносят длительное нахождение зонда в носоглотке и нередко саомстоятельно извлекают его уже в первые часы после операции. Поэтому необходима надежная фиксация зонда у носового хода. Чаще всего, учитывая важность длительного дренирования кишечника, зонд фиксируется путем подшивания его к крылу носа. Особенно это касается лиц пожилого и старческого возрастов, больных с неустойчивой психикой, а также при тяжелом интоксикационном синдроме и делирии. Г.-А.Ш.Каган (1982), ссылаясь на травматичность этого метода, предложил для фиксации зонда использовать лигатуру, предварительно проведенную вокруг носовой перегородки. Больные в таких случаях, по мнению автора, испытывают меньше неприятных ощущений. E.J.Seidmon et al. (1984) предложили специальную конструкцию, которая предусматривает фиксацию зонда в носовых ходах с помощью раздувания манжеты, изготовленной из мягкой латексной резины. Кроме того, зонд можно фиксировать тесемками бинта, концы которого проводятся и завязываются вокруг головы. Р.Ш.Вахтаигишвили и М.В.Беляев (1983) предлагают использовать зонд с петлей, специально предназначенной для проведения тесемки бинта.
2,2.3. Трансректальная интубация тонкой кишки Трансректальная интубация тонкой кишки с целью ее длительной декомпрессии получила распространение в детской хирургии
1 V *
 | |||
 |
 (Долецкий С.Я. с соавт., 1973; Топузов B.C. с соавт., 1982; Ва^ Г.А., Рошаль Л.М., 1991). Это связано с физиологическими и аш* томо-топографическими особенностями кишечника ребенка, а так же с трудностями ведения послеоперационного периода у этой *■ тегории больных при назознтерал ьном и чрезфистульных метода дренирования. У взрослых заведение зонда через толстую в тонкую кишку представляет собой более травматичную манипуляцию, особенно при проведении зонда через селезеночный угол и баугиниеву заслонку. Кроме того, трубка, имеющая боковые отверстия, в просвете толстой кишки быстро закупоривается калом и перестает дренировать кишечник. Тем не менее имеются сообщения об успешном использовании длительной трансректальной интубации при лечении кишечной непроходимости и перитонита у взрослых (Зайцев В.Т. с соавт., 1977; Любенко ЛА. с соавт., 1987; Griffen W., 1980). По данным этих авторов, удельный вес трансректального дренирования тонкой кишки составляет от 9 до 11%.
(Долецкий С.Я. с соавт., 1973; Топузов B.C. с соавт., 1982; Ва^ Г.А., Рошаль Л.М., 1991). Это связано с физиологическими и аш* томо-топографическими особенностями кишечника ребенка, а так же с трудностями ведения послеоперационного периода у этой *■ тегории больных при назознтерал ьном и чрезфистульных метода дренирования. У взрослых заведение зонда через толстую в тонкую кишку представляет собой более травматичную манипуляцию, особенно при проведении зонда через селезеночный угол и баугиниеву заслонку. Кроме того, трубка, имеющая боковые отверстия, в просвете толстой кишки быстро закупоривается калом и перестает дренировать кишечник. Тем не менее имеются сообщения об успешном использовании длительной трансректальной интубации при лечении кишечной непроходимости и перитонита у взрослых (Зайцев В.Т. с соавт., 1977; Любенко ЛА. с соавт., 1987; Griffen W., 1980). По данным этих авторов, удельный вес трансректального дренирования тонкой кишки составляет от 9 до 11%.
Для трансректальной интубации в зависимости от возраста больного и предполагаемого уровня дренирования используются полихлорвиниловые зонды длиной от 250 до 350 см и диаметром 0,8—1,5 см, снабженные оливой на конце. Предварительно на рабочую часть зонда (150 см) спиралевидно на расстоянии 5—6 мсм друг от друга наносятся боковые отверстия диаметром 0,3 см. Перед началом манипуляции в прямую кишку вводится 30—50 мл глицерина или вазелинового масла, и умеренно растягивается анус. Зонд вводится в прямую кишку и продвигается до ректосиг-моидного отдела. Хирург со






