Спектральные методы исследования находят в настоящее время широкое применение в лабораторной практике. Свет представляет собой совокупность элекромагнитных волн очень высокой частоты. Если на его пути поставить призму, то лучи будут преломляться под разными углами
(дисперсия), и дают спектры. Различают спектры по происхождению (атомные, молекулярные) по способу получения (испускания, поглощения), по виду (сплошной, линейчатый, полосатый).
I .Атомные спектры.
Состояние электрона в атоме характеризуется волновой функцией, которая содержит безразмерные величины-квантовые числа. Квантовые числа могут принимать ряд целочисленных значений. Этими числами задается атомная орбиталь, распределение электронов по атомным орбиталям и определяется электронная конфигурация атома.
Основным состоянием атомной системы является состояние с наименьшей энергией.
Возбужденным состоянием атомной системы называют состояние, в котором полная энергия больше энергии основного состояния. Энергия электронов атома тоже зависит от квантовых чисел и может принимать только строго определенные значения энергии Е, которые называются энергетическими уровнями. Для одноэлектроного атома энергетические уровни атома и электрона совпадают.
Поглощение и испускание энергии атома связано с квантовыми переходами электронов с одного уровня на другой.
Различаются два типа переходов:
I- с излучением или поглощением энергии квантов.
II.-без излучения или поглощения электромагнитной энергии.
Излучаемая атомами энергия составляет спектр излучения, поглощаемая спектр поглощения.
Квантовые переходы не могут происходить между любыми уровнями.
Существуют правила отбора или запрета, формирующие условия, при которых переходы возможны или невозможны (маловероятны).
В атомах в результате взаимодействия электронов между собой картина энергетических уровней усложняются. Энергия атома в целом определяется заданием квантовых чисел: n – главнее квантовое число, определяет уровни энергии электрона и L - орбитальное квантовое число, характеризует орбитальный моменьт электрона относительно ядра. Совокупность квантовых чисел n и L и определяет электронную конфигурацию атома. Как правило, каждой конфигурации принадлежит набор энергетических уровней.
При переходе между уровнями излучается или поглощается квант электромагнитной энергии, частота которого определяется формулой Планка: hv=Е2-Е1
II.Молекулярные спектры 
Молекулярные спектры значительно сложнее атомных. Рассмотрим энергетические уровни простейшей двухатомной молекулы. Каждому электронному состоянию соответствует своя система колебательных уровней Vi одно из которых основное и несколько возбужденных. Каждому колебательному уровню Vi соответствует своя система вращательных подуровней Ii.
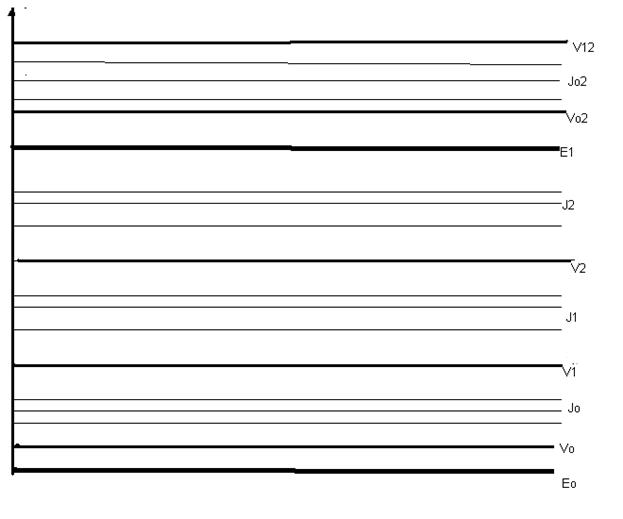
Рис.1 Энергетические уровни молекул
Чисто вращательные молекулярные спектры дают вещества в газообразном состоянии, чисто колебательные, а тем более чисто электронные спектры молекул получить нельзя, т.к. изменяется все три вида движения молекул. Колебательно-вращательные спектры можно получить при любом агрегатном состоянии.
В возбужденном состоянии молекула резко отличается по своим свойствам и строению, по сравнению с основным состоянием.






