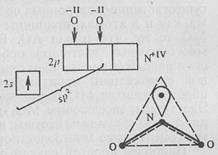
Оказалось, что конфигурация не всех молекул может быть объяснена схемой, приведенной в табл. 2. Так, например, можно представить себе, что в молекуле аммиака NH3 три связи N–H образованы «чистыми» (т.е. негибридизованными) 2р-орбиталями азота.
Молекула должна иметь пирамидальную форму: в вершине пирамиды – атом азота, угол между связями – 90°. Однако экспериментально измеренный угол составляет ~107,8°, что значительно лучше согласуется с тетраэдрической конфигурацией, характерной для sp 3‑гибридизации. Это можно объяснить, если предположить, что в гибридизации принимает участие орбиталь неподеленной (несвязывающей) пары электронов:
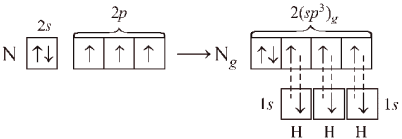
Перекрывание орбиталей в молекуле NH3 показано на рис. 12.
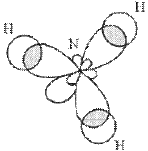
Рисунок 12. Перекрывание орбиталей в молекуле NH3
С этих же позиций участием орбиталей двух неподеленных пар электронов в sp 3‑гибридизации можно объяснить строение молекулы воды, в которой угол между связями О–Н равен ~104,5°:
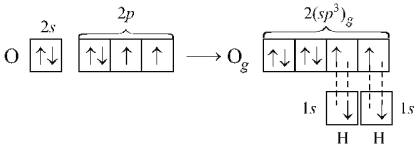
Вследствие более сильного отталкивающего действия неподеленных (несвязывающих) электронных пар валентные углы в молекулах NН3 и Н2О оказываются несколько меньше тетраэдрического.
Таблица 2
Изменение угла между связями Э–Н
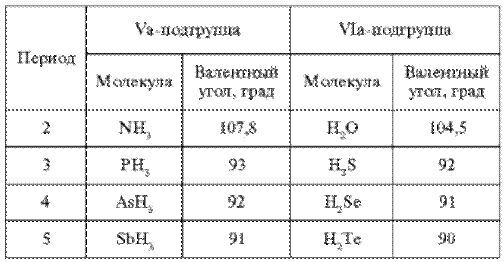
Для третьего и последующих периодов из-за увеличения размеров атомов и уменьшения плотности электронных облаков гибридизация, как реальное явление не наблюдается, связи образуются р-орбиталями. Это иллюстрирует табл. 2
В случае sp, sp 2, sp 3, sp 3 d 2 гибридизации вершины в многограннике, описывающем геометрию химической частицы, равноценны, и поэтому кратные связи и неподеленные пары электронов могут занимать любые из них. Однако, sp 3 d -гибридизации отвечает тригональная бипирамида, в которой валентные углы для атомов, расположенных в основании пирамиды (экваториальной плоскости), равны 120o, а валентные углы с участием атомов, расположенных в вершинах бипирамиды, равны 90o. Эксперимент показывает, что неподеленные электронные пары всегда располагаются в экваториальной плоскости тригональной бипирамиды. На этом основании делается вывод, что они требуют больше свободного пространства, чем пары электронов, участвующие в образовании связи. Примером частицы с таким расположением неподеленной электронной пары является тетрафторид серы. Если центральный атом одновременно имеет неподеленные пары электронов и образует кратные связи (например, в молекуле XeOF2), то в случае sp 3 d -гибридизации именно они располагаются в экваториальной плоскости тригональной бипирамиды.
Механизм образования связи - обменный или донорно-акцепторный - не влияет на тип гибридизации электронных облаков атомов-партнеров. Линейная молекула ВеСl2 может образоваться в газовой фазе как из атомов Ве и Сl, так и из ионов Ве2+ и Сl-. В последнем случае ион Ве2+ (акцептор) предоставляет вакантные 2 s - и 2 p -орбитали, а ионы Сl- (доноры) - неподеленные электронные облака связи. Оба механизма в конечном итоге приводят к одному и тому же sр-гибридному состоянию.
В образовании молекулы CH4 и NH4+ принимают участие электроны 2s- и 2p-орбиталей. Общее число валентных электронов одинаково в обеих частицах. Именно вследствие sp3-гибридизации для них характерна одна и та же структура - правильного тетраэдра, несмотря на различие в механизме их образования.
Наличие π -связей также не влияет на тип гибридизации. Однако наличие дополнительного связывания может привести к изменению валентных углов, поскольку электроны кратных связей сильнее отталкиваются друг от друга. По этой причине, например, валентный угол в молекуле NO2 (sp 2-гибридизация) увеличивается от 120o до 134o.