Электролиз раствора хлорида натрия
Вычисления
Вычисление теоретической массы получаемых веществ проводится по формуле: mтеор = М ∙ I ∙ τ / Z ∙ F
где М – это молярная масса получаемого вещества (г/моль)‚ Z – число принятых или отданных электронов‚ I – это сила тока, при которой осуществлялся процесс (А), τ – время (в секундах или часах), F – постоянная Фарадея, равная 26,8 А ∙ ч, если время было взято в часах‚ или 96500 А∙с/моль, если время было взято в секундах.
Вычисление практической массы газа проводится исходя из практического объема газа, полученного за время проведения эксперимента по формуле:
mпракр = М ∙ V прак. / V m,
где М – это молярная масса полученного вещества, V прак. – объем полученного вещества, V m – молярный объем газа, равный 22.4 л/моль
Вычисление массовой доли выхода вещества от теоретически возможного (в%) проводится по формуле: η = mпракр ∙ 100% / mтеор
Опыт 1. Электролиз раствора хлорида натрия
Реактивы и оборудование: 1,5 л насыщенного раствора хлорида натрия, крахмальный клейстер, кристаллический КI, электролизер, выпрямитель электрического тока, кристаллизатор, пробирки, резиновые шланги.
Ход работы: (А) Собрать прибор по схеме‚ приведённой на рис. 5. Подключить прибор к источнику электрического тока и засечь время до момента полного заполнения пробирки газом с катода. На угольном аноде наблюдаем _______________________________, а на железном катоде происходит________
_________________________________________, наблюдаемые процессы можно описать следующей схемой:
К – :
А +:
Ионное уравнение:____________________________________________________
Общее молекулярное уравнение электролиза раствора NaCl имеет вид:
____
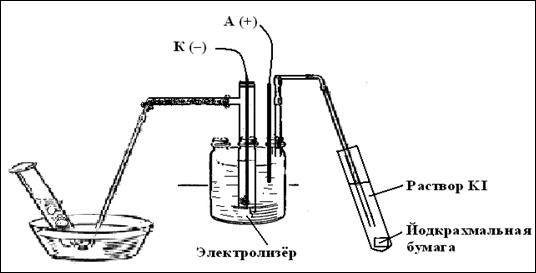
Рис. 5
(Б) Газ (________), выделяющийся на аноде пропускаем в крахмальный клейстер с помещенными в него кристаллами иодида калия, в пробирке наблюдаем ___________________________________.Уравнение реакции данного процесса:
Уравнение электронного баланса этой реакции:
Выделяющийся на аноде газ способен вытеснить из раствора KI свободный йод‚ так как__________________________________________________________.
(В) Газ (______________), выделяющийся на катоде, собираем над водой и подтверждаем его качественный состав, поднося пробирку с газом (строго вертикально и вверх дном, так как _______________________________________) к горящей лучине или спиртовке. Наблюдения: ____________________________, уравнение данной реакции имеет вид:___________________________________, а уравнение электронного баланса можно представить:
Вычисление массовой доли выхода водорода от теоретически возможного
Выводы:
Упражнения для самостоятельного решения
1. Вычислить эквивалент железа, если при прохождении через раствор соли железа тока в 5А в течение 5,36 ч выделилось 27,9∙10 –3 кг железа. (Ответ: 27,9 г).
2. Вычислить объем Н2, выделенного при пропускании тока 5 А в течение часа через раствор H2SO4. (Ответ: 4,2 л.)
3. Раствор NiCl2, содержащий 0,1297 кг соли, подвергался электролизу током в 5 А в течение 5,36 ч. Сколько хлорида никеля осталось в растворе и какой объем хлора выделился? (Ответ: 64,85 г, 11,2 л.)
4. Составить уравнение электролиза раствора нитрата натрия и хлорида меди (II).






