в бесконечно разбавленных растворах при 25 ∞— [8]
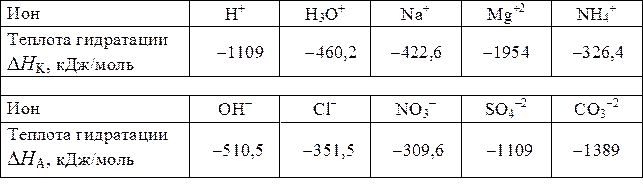
|DHг| ѕример 1. ќпределить теплоту гидратации мол€ NaCl.
–ешение.
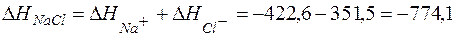 кƒж/моль.
кƒж/моль.
“еплота гидратации NaCl весьма значительна, что говорит о прочности гидратированных ионов, образующихс€ в растворе.
—войства растворов электролитов
—ильные электролиты в растворе диссоциированы (ионизированы) практически полностью. ƒиссоциаци€ слабых электролитов протекает обратимо и устанавливаетс€ равновесие (7.1).
оличественно процесс диссоциации может быть охарактеризован р€дом величин: степенью диссоциации a, изотоническим коэффициентом i, константой электролитической диссоциации K д, эквивалентной электропроводимостью l.
—тепень электролитической диссоциации a Ц это отношение числа молекул, распавшихс€ на ионы, к общему числу молекул растворенного вещества в растворе.
—тепень диссоциации a может измер€тьс€ в дол€х единицы или в процентах (%). ≈сли a = 0, диссоциаци€ отсутствует, вещество раствор€етс€ в молекул€рной форме и €вл€етс€ неэлектролитом. огда a = 1 или a = 100 %, происходит полна€ диссоциаци€ электролита и растворенное вещество находитс€ только в ионной форме.
ƒеление электролитов на слабые и сильные проводитс€ по значению a Ц степени диссоциации дл€ 0,1 н. растворов электролитов при температуре t = 25 ∞—. —ильные электролиты Ц вещества, которые в 0,1 н. растворе хорошо провод€т электрический ток и диссоциируют больше чем на 30 %. сильным электролитам относ€тс€ хорошо растворимые соли, а также сильные кислоты и основани€ (табл. 5).
“аблица 5
ѕримеры электролитов
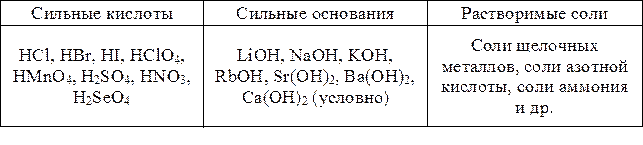
слабым электролитам относ€тс€ кислоты и основани€, которые в 0,1 н. растворе плохо провод€т электрический ток и диссоциируют менее чем на 3¸5 %. “акже к ним относ€т труднорастворимые соли, дл€ которых низка€ электропроводность раствора св€зана с малой концентрацией соли в растворе (хот€ a диссоциации таких солей близка к 1).
Ёлектролиты средней силы характеризуютс€ степенью диссоциации 5¸30 %.
процессу электролитической диссоциации применим принцип Ће Ўателье, позвол€ющий вы€вить вли€ние внешних факторов на состо€ние равновеси€, привод€щее к изменению a. ƒл€ смещени€ равновеси€ в сторону продуктов диссоциации необходимо увеличить массу растворител€.
“еплота гидратации понижаетс€ с повышением температуры (вследствие уменьшени€ координационного числа гидратированных ионов), процесс диссоциации становитьс€ более эндотермичным, поэтому повышение температуры будет смещать равновесие реакции диссоциации (7.1) слева направо. —тепень диссоциации слабого электролита в водном растворе будет увеличиватьс€ с повышением температуры.






