Используя свойства экстенсивности термодинамических потенциалов, математическим следствием которых является соотношение Гиббса-Дюгема, можно показать, что химический потенциал для системы с одним типом частиц есть отношение энергии Гиббса к числу частиц в системе:
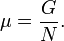
Если система состоит из частиц нескольких сортов 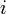 с числом
с числом 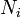 частиц каждого сорта, то соотношения Гиббса-Дюгема приводят к выражению
частиц каждого сорта, то соотношения Гиббса-Дюгема приводят к выражению
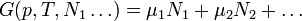
Химический потенциал применяется при анализе систем с переменным числом частиц, а также при изучении фазовых переходов. Так, исходя из соотношений Гиббса-Дюгема и из условий равенства химических потенциалов 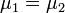 находящихся в равновесии друг с другом фаз, можно получить уравнение Клапейрона-Клаузиуса, определяющее линию сосуществования двух фаз в координатах
находящихся в равновесии друг с другом фаз, можно получить уравнение Клапейрона-Клаузиуса, определяющее линию сосуществования двух фаз в координатах 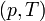 через термодинамические параметры (удельные объёмы) фаз и теплоту перехода между фазами.
через термодинамические параметры (удельные объёмы) фаз и теплоту перехода между фазами.
В химических процессах одновременно действуют два противоположных фактора — энтропийный (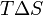 ) и энтальпийный (
) и энтальпийный (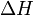 ). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (
). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (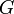 ):
):
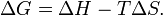
Из этого выражения следует, что 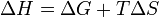 , то есть некоторое количество теплоты расходуется на увеличение энтропии (
, то есть некоторое количество теплоты расходуется на увеличение энтропии (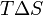 ), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (
), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (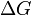 ) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.
) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.
Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При 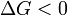 процесс может протекать, при
процесс может протекать, при 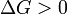 процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же
процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же 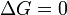 , то система находится в состоянии химического равновесия.
, то система находится в состоянии химического равновесия.
Обратите внимание, что речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенства 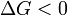 (по кинетическим причинам).
(по кинетическим причинам).
Существует полезное соотношение, связывающее изменение свободной энергии Гиббса 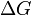 в ходе химической реакции с её константой равновесия
в ходе химической реакции с её константой равновесия 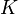 :
:
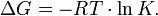
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как
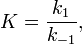
где 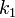 — константа скорости прямой реакции,
— константа скорости прямой реакции, 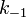 — константа скорости обратной реакции.
— константа скорости обратной реакции.
Историческая справка
Энергия Гиббса названа в честь одного из основателей термодинамики, Джозаи Уилларда Гиббса.
Закон Гесса — основной закон термохимии, который формулируется следующим образом:
§ Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данноехимическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы). Например, окисление глюкозыв организме осуществляется по очень сложному многостадийному механизму, однако суммарный тепловой эффект всех стадий данного процесса равен теплоте сгорания глюкозы.
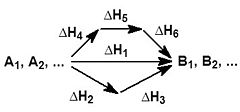

На рисунке приведено схематическое изображение некоторого обобщенного химического процесса превращения исходных веществ А1, А2… в продукты реакции В1, В2…, который может быть осуществлен различными путями в одну, две или три стадии, каждая из которых сопровождается тепловым эффектом ΔHi. Согласно закону Гесса, тепловые эффекты всех этих реакций связаны следующим соотношением:
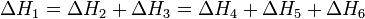
Закон открыт русским химиком Г. И. Гессом в 1840 г.; он является частным случаем первого начала термодинамикиприменительно к химическим реакциям. Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты самых разнообразных химических процессов; для этого обычно используют ряд следствий из него.
[Следствия из закона Гесса
§ Тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции (закон Лавуазье — Лапласа).
§ Тепловой эффект химической реакции равен разности сумм теплот образования (ΔHf) продуктов реакции и исходных веществ, умноженных на стехиометрическиекоэффициенты (ν):
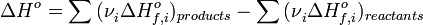
§ Тепловой эффект химической реакции равен разности сумм теплот сгорания (ΔHc) исходных веществ и продуктов реакции, умноженных на стехиометрические коэффициенты (ν):
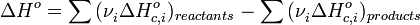
Таким образом, пользуясь табличными значениями теплот образования или сгорания веществ, можно рассчитать теплоту реакции, не прибегая к эксперименту. Табличные величины теплот образования и сгорания веществ обычно относятся к т. н. стандартным условиям. Для расчёта теплоты процесса, протекающего при иных условиях, необходимо использовать и другие законы термохимии, например, закон Кирхгофа, описывающий зависимость теплового эффекта реакции от температуры.
§ Если начальное и конечное состояния химической реакции (реакций) совпадают, то ее (их) тепловой эффект равен нулю.
§ 30. ЭНЕРГЕТИЧЕСКИЕ ЭФФЕКТЫ ХИМИЧЕСКИХ РЕАКЦИЙ
§ Молекулы состоят из атомов. Возможны два вида молекул: содержащие одинаковые атомы и молекулы, содержащие два или более различных атомов. Эти два вида молекул имеют разные названия:
- элемент — состоит из атомов только одного вида;
- соединение, или сложное вещество, — состоит из двух или более различных атомов.
Один моль каждого индивидуального вещества обладает определенным теплосодержанием, равно, как и определенной массой. Теплосодержание является мерой энергии, накапливаемой веществом при его образовании. Тепловой эффект химической реакции равен разности между теплосодержанием ее продуктов реакции и теплосодержанием реагирующих веществ. Если теплосодержание реагирующих веществ больше, чем у продуктов реакции, то при такой химической реакции тепло выделяется и она называется экзотермической. Если же теплосодержание продуктов реакции больше, чем у реагирующих веществ, то при реакции тепло поглощается и такая реакция называется эндотермической.
То, что в каждом индивидуальном веществе заключено определенное количество энергии, служит объяснением тепловых эффектов химических реакций. Теплосодержание иногда называют химической энергией, так как его величина тесно связана с химическим составом вещества.
Каждый атом обладает энергией, часть которой связана с электронами и часть — с ядром. Электроны в атоме обладают кинетической энергией, и поскольку они притягиваются ядром и отталкиваются друг от друга, то и потенциальной энергией. Алгебраическая сумма кинетической и потенциальной энергий и составляют энергию, необходимую для отрыва электрона от атомного ядра. Ядро же каждого атома — колоссальный источник энергии, которая связана с взаимодействием ядерных частиц — нуклонов.
Так как атомные ядра при химических реакциях не испытывают изменений, энергия ядер не изменяется. Поэтому энергия ядер не входит в теплосодержание молекул.
При нагревании твердого вещества увеличивается кинетическая энергия колебательного движения молекул около мест, занимаемых ими в кристаллической решетке. С повышением температуры эти тепловые колебания все больше нарушают упорядоченное строение кристалла. Когда же такое хаотическое тепловое движение молекул становится слишком быстрым, кристаллическая решетка полностью разрушается. При температуре, выше которой кинетическая энергия частиц обусловливает столь быстрое хаотическое движение, что кристаллическая решетка больше не может оставаться устойчивой, происходит фазовый переход — плавление твердого вещества.
В жидкости каждая молекула обладает значительно большей свободой движения, особенно поступательного и вращательного. При нагревании жидкости молекулярное движение усиливается. Кинетическая энергия обуславливает хаотическое движение, приводящее к распределению молекул по возможно большему объему. Поэтому с ростом температуры по мере увеличения энергии движения все большее число молекул может удаляться из жидкой фазы туда, где потенциальная энергия минимальна. При этом происходит другой фазовый переход — испарение жидкости.
Если продолжать нагревать вещество, то наступит момент, когда кинетическая энергия колебательного, вращательного и поступательного движений по величине станет сравнима с энергией химических связей. Тогда молекулы начинают разрушаться. По этой причине на Солнце не обнаружены молекулы, содержащие более чем два атома: только самые простые, двухатомные молекулы. Температура на Солнце настолько высока (6000 К), что более сложные молекулы не могут существовать.
Если дальше продолжать нагревание, то в конце концов достигается температура, при которой кинетическая энергия настолько возрастает, что разрушаются ядра. Тогда начинаются ядерные реакции. Предполагается, что на некоторых звездах существуют условия, благоприятные для быстрых ядерных реакций. Затраты энергии при химических реакциях в 10—100 раз больше, чем при фазовых переходах.
§ В ходе химической реакции происходит превращение веществ, следовательно, разрушаются химические связи, на что затрачивается энергия и образуются другие вещества при этом энергия выделяется. Поэтому любая реакция сопровождается поглощением или выделением энергии.
§ Внутренняя энергия (U) – это общий запас энергии системы, включая энергию поступательного и вращательного движения молекул, энергии внутремолекульных колебаний атомов, внитреядерную энергии, т. е. все виды энергии, кроме кинетической энергии как целого и ее потенциальной энергии. Внутренняя энергия является функцией состояния системы, т. е. U=f(P,V,T,νа,νв,νс)
§ Сумма внутренней энергии и произведение объема системы на внешнее давление называется энтальпия H, Дж – это теплосодержание системы. Энтальпия как и внутренняя энергия является функцией состояния системы.
§ Для того чтобы сравнить между собой теплоты различных реакций необходимо точно указать условия при которых они протекают. В термохимии принято стандартное состояние вещества при – это давление 101 кПа и температура 298 к.
§ Символ ∆H0298 – это изменение энтальпии веществ реакции в стандартном состоянии для исходных веществ и продуктов реакции.
§ Стандартная теплота образования вещества ∆H0f298 – это тепловой эффект образования одного моль вещества из простых веществ при стандартных условиях. Условно принято, что теплота образования простых веществ равна 0. Величина стандартных тепло образования сложных веществ приводится в справочных таблицах.
Закон Гесса — основной закон термохимии, который формулируется следующим образом:
§ Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данноехимическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы). Например, окисление глюкозыв организме осуществляется по очень сложному многостадийному механизму, однако суммарный тепловой эффект всех стадий данного процесса равен теплоте сгорания глюкозы.


На рисунке приведено схематическое изображение некоторого обобщенного химического процесса превращения исходных веществ А1, А2… в продукты реакции В1, В2…, который может быть осуществлен различными путями в одну, две или три стадии, каждая из которых сопровождается тепловым эффектом ΔHi. Согласно закону Гесса, тепловые эффекты всех этих реакций связаны следующим соотношением:
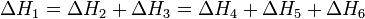
Закон открыт русским химиком Г. И. Гессом в 1840 г.; он является частным случаем первого начала термодинамикиприменительно к химическим реакциям. Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты самых разнообразных химических процессов; для этого обычно используют ряд следствий из него.
]Следствия из закона Гесса
§ Тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции (закон Лавуазье — Лапласа).
§ Тепловой эффект химической реакции равен разности сумм теплот образования (ΔHf) продуктов реакции и исходных веществ, умноженных на стехиометрическиекоэффициенты (ν):
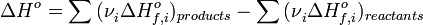
§ Тепловой эффект химической реакции равен разности сумм теплот сгорания (ΔHc) исходных веществ и продуктов реакции, умноженных на стехиометрические коэффициенты (ν):
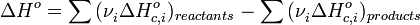
Таким образом, пользуясь табличными значениями теплот образования или сгорания веществ, можно рассчитать теплоту реакции, не прибегая к эксперименту. Табличные величины теплот образования и сгорания веществ обычно относятся к т. н. стандартным условиям. Для расчёта теплоты процесса, протекающего при иных условиях, необходимо использовать и другие законы термохимии, например, закон Кирхгофа, описывающий зависимость теплового эффекта реакции от температуры.
§ Если начальное и конечное состояния химической реакции (реакций) совпадают, то ее (их) тепловой эффект равен нулю.
Рассчет теплового эффекта
§)По термохимическому уравнению С(тв)+ О2(г)=СО2(г)+393,5 кДж расчитайте сколько выделится теплоты при сгорании 1 кг угля?
2)При взаимодействии 1,8 г алюминия с кислородом выделяется 55,65 кДж теплоты.Составьте термохимическое уравнение этой реакции.
Решение:
1)n(С)=83,33моль
1моль с-393,5 кДж
83,33 моль-х; х=32791,67кДж,а у ответах 32,792кДж.Ошибка с переводом единиц?
2)n(Al)=0,067моль
0,067моль Al-55,65 кДж
4 моль-х; х=3322,388кДж, а в ответах 3339кДж.Выходит через массу считали?А нужно только через количество?
Энтальпи́я, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Проще говоря, энтальпия - это та энергия, которая доступна для преобразования в теплоту при определенных температуре и давлении.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня с грузом весом Р = p S, уравновешивающего давление газа р внутри сосуда, то такая система называется расширенной.
Энтальпия или энергия расширенной системы Е равна сумме внутренней энергии газа U и потенциальной энергии поршня с грузом E пот = pSx = pV
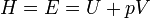
Таким образом, энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объёмом V ввести в окружающую среду, имеющую давление р и находящуюся с телом в равновесном состоянии. Энтальпия системы H — аналогично внутренней энергии и другим термодинамическим потенциалам — имеет вполне определенное значение для каждого состояния, т. е. является функцией состояния. Следовательно, в процессе изменения состояния
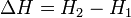
Изменение энтальпии (или Тепловой эффект химической реакции) не зависит от пути процесса, определяясь только начальным и конечным состоянием системы. Если система каким-либо путём возвращается в исходное состояние (круговой процесс), то изменение любого её параметра, являющегося функцией состояния, равно нулю, отсюда 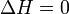 , или же
, или же
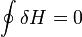
Дифференциал энтальпии, выраженный в собственных переменных — через энтропию S и давление p:
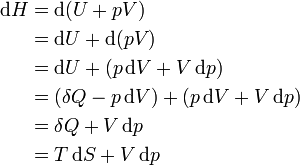
Поскольку в квазиравновесных процессах 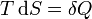 — количество теплоты, подведенной к системе, отсюда вытекает физический смысл введения понятия энтальпии: ее изменение — это тепло, подведенное к системе в изобарическом процессе (при постоянном давлении). Практическое применение этой функции основано на том, что множество химических процессов в реальных или лабораторных условиях реализуются именно при постоянном (атмосферном) давлении, когда резервуар открыт. Так,энтальпия образования — количество энергии, которое выделяется или поглощается при образовании сложного вещества из простых веществ.
— количество теплоты, подведенной к системе, отсюда вытекает физический смысл введения понятия энтальпии: ее изменение — это тепло, подведенное к системе в изобарическом процессе (при постоянном давлении). Практическое применение этой функции основано на том, что множество химических процессов в реальных или лабораторных условиях реализуются именно при постоянном (атмосферном) давлении, когда резервуар открыт. Так,энтальпия образования — количество энергии, которое выделяется или поглощается при образовании сложного вещества из простых веществ.
Все химические реакции сопровождаются выделением (экзотермические) или поглощением (эндотермические) тепла. Мерой теплоты реакции служит изменение энтальпии ΔН, которая соответствует теплообмену при постоянном давлении. В случае экзотермических реакций система теряет тепло и ΔН — величина отрицательная. В случае эндотермических реакций система поглощает тепло и ΔН — величина положительная.
Энтальпией системы удобно пользоваться в тех случаях, когда в качестве независимых переменных, определяющих состояние системы, выбирают давление р и температуру Т
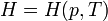
В этом случае изменение энтальпии в изобарическом процессе практически удобно рассчитывать, зная теплоемкость при постоянном давлении 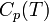 (термохимический закон Кирхгофа):
(термохимический закон Кирхгофа): 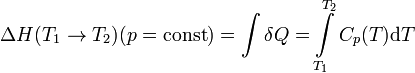
При этом используется эмпирическое разложение теплоёмкости в ряд по степеням Т:
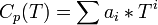
Энтальпия — величина аддитивная (экстенсивная), т. е. для сложной системы равна сумме энтальпий её независимых частей 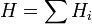 . Подобно другим термодинамическим потенциалам, энтальпия определяется с точностью до постоянного слагаемого, которому в термодинамике часто придают произвольные значения (например, при расчете и построении тепловых диаграмм). При наличии немеханических сил величина энтальпии системы равна
. Подобно другим термодинамическим потенциалам, энтальпия определяется с точностью до постоянного слагаемого, которому в термодинамике часто придают произвольные значения (например, при расчете и построении тепловых диаграмм). При наличии немеханических сил величина энтальпии системы равна
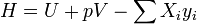
где 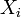 — обобщённая сила;
— обобщённая сила; 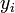 — обобщённая координата.
— обобщённая координата.
]Примеры
| Неорганические соединения (при 25 °C) стандартная энтальпия реакции | |||
| Хим соединение | Фаза (вещества) | Химическая формула | Δ Hf 0 кДж/моль |
| Аммиак | сольватированный | NH3 (NH4OH) | −80.8 |
| Аммиак | газообразный | NH3 | −46.1 |
| Карбонат натрия | твёрдый | Na2CO3 | −1131 |
| Хлорид натрия (соль) | сольватированный | NaCl | −407 |
| Хлорид натрия (соль) | твёрдый | NaCl | −411.12 |
| Хлорид натрия (соль) | жидкий | NaCl | −385.92 |
| Хлорид натрия (соль) | газообразный | NaCl | −181.42 |
| Гидроксид натрия | сольватированный | NaOH | −469.6 |
| Гидроксид натрия | твёрдый | NaOH | −426.7 |
| Нитрат натрия | сольватированный | NaNO3 | −446.2 |
| Нитрат натрия | твёрдый | NaNO3 | −424.8 |
| Диоксид серы | газообразный | SO2 | −297 |
| Серная кислота | жидкий | H2SO4 | −814 |
| Диоксид кремния | твёрдый | SiO2 | −911 |
| Диоксид азота | газообразый | NO2 | +33 |
| Монооксид азота | газообразный | NO | +90 |
| Вода | жидкий | H2O | −286 |
| Вода | газообразный | H2O | −241.8 |
| Диоксид углерода | газообразный | CO2 | −393.5 |
| Водород | газообразный | H2 | |
| Фтор | газообразный | F2 | |
| Хлор | газообразный | Cl2 | |
| Бром | жидкий | Br2 | |
| Бром | газоообразный | Br2 |
31. Превращение энергии при химических реакциях
Химическая реакция – превращение одного или нескольких исходных веществ в другие по химическому составу или строению вещества.
По сравнению с ядерными реакциями общее число атомов и изотопный состав химических элементов при химических реакциях неизменны.
Виды химических реакций:
1) смешение или физический контакт реагентов;
2) нагревание;
3) катализ;
4) фотохимические реакции (с участием света);
5) электродные процессы;
6) механохимические реакции;
7) радиационно-химические реакции;
8) плазмохимические реакции.
Основные типы химических реакций:
1) соединения: 2Cu + O2 = 2CuO;
2) разложения: 2HgO = 2Hg + O2;
3) замещения: Fe + CuSO4 = FeSO4 + Cu;
4) обмена: NaCl + H2SO4 = НСl + NaHSO4.
Химические реакции характеризуются физическими проявлениями:
1) поглощение и выделение энергии;
2) изменение агрегатного состояния реагентов;
3) изменение окраски реакционной смеси и др.
Выделение или поглощение энергии происходит в виде теплоты. Это позволяет судить о наличии в веществах определенного количества некоторой энергии (внутренней энергией реакции).
При химических реакциях происходит освобождение части энергии, содержащейся в веществах, это носит название теплового эффекта реакции, по которому можно судить об изменении количествавнутренней энергии вещества.
У ряда химических реакций можно наблюдать поглощение или выделение лучистой энергии. В этих случаях внутренняя энергия через теплоту превращается в излучение (горение). Существуют также процессы в которых внутренняя энергия сразу превращается в лучистую (лю-минисценция).
В химических реакциях, протекающих с взрывом, внутренняя энергия превращается в механическую, причем частично сразу, частично переходя изначально в теплоту.
Во время химических реакций происходит взаимное превращение энергий – внутренней энергии веществ в тепловую, лучистую, электрическую и механическую, и наоборот.
Экзотермические химические реакции характеризуются выделением энергии во внешнюю среду. Эндотермические – поглощением энергии.
В физических процессах вещества не изменяют своих свойств, может измениться внешняя форма или агрегатное состояние. В химических процессах образуются новые вещества с другими свойствами. При ядерных реакциях в атомах обязательно происходят трансформации электронной оболочки.
Зако́н сохране́ния эне́ргии — фундаментальный закон природы, установленный эмпирически и заключающийся в том, что для изолированной физической системы может быть введена скалярная физическая величина, являющаяся функцией параметров системы и называемая энергией, которая сохраняется с течением времени. Поскольку закон сохранения энергии относится не к конкретным величинам и явлениям, а отражает общую, применимую везде и всегда, закономерность, то его можно именовать не законом, а принципом сохранения энергии.
С фундаментальной точки зрения, согласно теореме Нётер, закон сохранения энергии является следствием однородности времени, то есть независимостью законов физики от момента времени, в который рассматривается система. В этом смысле закон сохранения энергии является универсальным, то есть присущим системам самой разной физической природы. При этом выполнение этого закона сохранения в каждой конкретно взятой системе обосновывается подчинением этой системы своим специфическим законам динамики, вообще говоря различающимся для разных систем.
В различных разделах физики по историческим причинам закон сохранения энергии формулировался независимо, в связи с чем были введены различные виды энергии. Говорят, что возможен переход энергии одного типа в другой, но полная энергия системы, равная сумме отдельных видов энергий, сохраняется. Ввиду условности деления энергии на различные виды, такое деление не всегда может быть произведено однозначно.
Для каждого вида энергии закон сохранения может иметь свою, отличающуюся от универсальной, формулировку. Например, в классической механике был сформулирован закон сохранения механической энергии, в термодинамике — первое начало термодинамики, а в электродинамике — теорема Пойнтинга.
С математической точки зрения закон сохранения энергии эквивалентен утверждению, что система дифференциальных уравнений, описывающая динамику данной физической системы, обладает первым интегралом движения, связанным с симметричностью уравнений относительно сдвига во времени.
]Фундаментальный смысл закона
| Симметрия в физике | ||
| Преобразование | Соответствующая инвариантность | Соответствующий закон сохранения |
| ↕ Трансляции времени | Однородность времени | …энергии |
| ↔ Обращение времени | Изотропность времени | …энтропии |
| ↔ Трансляции пространства | Однородность пространства | …импульса |
| ○ Вращения пространства | Изотропность пространства | …момента импульса |
| × Группа Лоренца | Относительность Лоренц-инвариантность | …4-импульса |
Фундаментальный смысл закона сохранения энергии раскрывается теоремой Нётер. Согласно этой теореме каждый закон сохранения однозначно соответствует той или иной симметрииуравнений, описывающих физическую систему. В частности, закон сохранения энергии эквивалентен однородности времени, то есть независимости всех законов, описывающих систему, от момента времени, в который система рассматривается.
Вывод этого утверждения может быть произведён, например, на основе лагранжева формализма[1]. Если время однородно, то функция Лагранжа, описывающая систему, не зависит явно от времени, поэтому полная её производная по времени имеет вид:
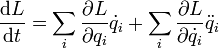
Здесь 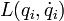 — функция Лагранжа,
— функция Лагранжа, 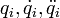 — обобщённые координаты и их первые и вторые производные по времени соответственно. Воспользовавшись уравнениями Лагранжа, заменим производные
— обобщённые координаты и их первые и вторые производные по времени соответственно. Воспользовавшись уравнениями Лагранжа, заменим производные 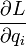 на выражение
на выражение 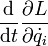 :
:
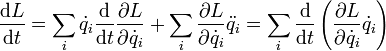
Перепишем последнее выражение в виде
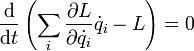
Сумма, стоящая в скобках, по определению называется энергией системы и в силу равенства нулю полной производной от неё по времени она является интегралом движения (то есть сохраняется).
Термодинамическая система — это некая физическая система, состоящая из большого количества частиц, способная обмениваться с окружающей средой энергией и веществом. Также обычно полагается, что такая система подчиняется статистическим закономерностям. Для термодинамических систем справедливы законы термодинамики.
]Описание
Для описания термодинамической системы вводят так называемые термодинамические величины — набор физических величин, значения которых определяют термодинамическое состояние системы. Примерами термодинамических величин являются:
§ температура
§ давление
§ объем
§ внутренняя энергия
§ энтропия
§ энтальпия
§ свободная энергия Гельмгольца
§ энергия Гиббса
Если термодинамическое состояние системы не меняется со временем, то говорят, что система находится в состоянии равновесия. Строго говоря, термодинамические величины, приведённые выше, могут быть определены только в состоянии термодинамического равновесия.
[Классификация
Термодинамические системы подразделяются на однородные по составу (например, газ в сосуде) и неоднородные (вода и пар или смесь газов в сосуде).
Выделяют также изолированные системы, то есть системы, которые не обмениваются с окружающей средой ни энергией, ни веществом, и закрытые системы, которые обмениваются со средой только энергией, но не обмениваются веществом. Если же в системе происходят обменные процессы с окружающей средой, то её называютоткрытой.
Функции состояния
Функции состояния зависят только от текущего состояния системы и не зависят от пути, по которому система пришла в это состояние.
Функции состояния в термодинамике включают:
§ температуру,
§ давление,
§ объём,
§ энтропию,
а также термодинамические потенциалы.
В зависимости от выбранной модели некоторые из этих величин, строго говоря, могут быть не функциями, а независимыми переменными.
Эти величины не являются независимыми. Связь между термодинамическими параметрами для конкретной системы называетсяуравнением состояния.
В случае, если известно каноническое уравнение состояния, задание любой пары параметров из следующих:
§ энтропия и объём,
§ энтропия и давление,
§ температура и объём,
§ температура и давление,
позволяет вычислить остальные два параметра.
Первый закон термохимии: при разложении соединения на простые вещества происходит изменение энтальпии, равное (но с противоположным знаком) изменению энтальпии при образовании этого соединения из тех же простых веществ
Первый закон тeрмохимии открыт в конце XVIII в. французскими учеными Лавуазье и Лапласом, второе название этого закона - закон Лавуазье-Лапласа. Фактически этот закон вытекает из закона сохранения энергии; именно на этом законе основана формула для расчета энтальпии реакции по энтальпии образования участвующих в ней веществ.
Энтальпию образования определить экспериментально можно не для всех веществ из-за сложности проведения или практической неосуществимости многих реакций. Табличные значения ΔH°298 для многих веществ получены расчетным способом, основанном на втором законе термохимии, открытом в 1840 г. русским химиком Г.И. Гессом, закон Гесса
32. ободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции; это термодинамический потенциал следующего вида:
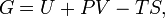
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста ее энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж)
Определение
Классическим определением энергии Гиббса является выражение
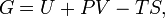
где 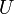 — внутренняя энергия,
— внутренняя энергия, 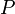 — давление,
— давление, 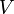 — объем,
— объем, 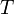 — абсолютная температура,
— абсолютная температура, 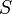 — энтропия.
— энтропия.
Дифференциал энергии Гиббса для системы с постоянным числом частиц, выраженный в собственных переменных — через давление p и температуру T:
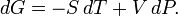
Для системы с переменным числом частиц этот дифференциал записывается так:
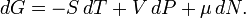
Здесь 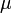 — химический потенциал, который можно определить как энергию, которую необходимо затратить, чтобы добавить в систему ещё одну частицу.
— химический потенциал, который можно определить как энергию, которую необходимо затратить, чтобы добавить в систему ещё одну частицу.






