Кафедрой технологии продуктов питания и экспертизы товаров установлены требования к выполнению контрольных работ. Студенту следует внимательно ознакомиться с ними и учесть, что невыполнение одного из требований может быть причиной возвращения преподавателем студенту контрольной работы без ее рецензирования.
Требование к выполнению контрольных работ:
Контрольная работа должна показывать степень усвоения студентом разделов программы, способность к анализу изучаемого материала, умение выделять основные положения и обобщать данные учебной литературы.
Контрольная работа должна иметь объем не менее объема ученической тетради (12 листов), допускается написание работы на скрепленных листах формата А-4.
Контрольную работу следует писать разборчивым почерком, с интервалами между строками (если тетрадь в линейку – писать следует на каждой строке, если в клеточку – через строку).
Страницы тетради надо пронумеровать.
На каждой странице необходимо оставлять поля.
В тексте контрольной работы не допускаются сокращения слов, кроме наименований единиц измерений (только после цифровых данных), а также научных символов.
При описании ответов на вопросы работы обязательно надо представлять схемы, таблицы, диаграммы, химические формулы и другой иллюстрационный материал.
На первой странице тетради указываются номер варианта работы и полное наименование трех вопросов работы.
Обязательным требованием является наличие списка литературы, использованной при выполнении работы.
Литература указывается по установленной форме:
Для книг указывается:
Фамилия и инициалы автора (авторов). Название книги. Место издания: Издательство. Год издания. Количество страниц.
Для статей указывается:
Фамилия и инициалы автора (авторов). Название статьи. // Название журнала или сборника. – Год издания. – Номер журнала, номер выпуска, номера страниц, на которых напечатана статья.
Контрольную работу после списка литературы студент подписывает и указывает дату ее выполнения.
На обложке контрольной работы студент указывает фамилию, имя, отчество, шифр, номер варианта, дисциплину, домашний адрес.
Выполненная работа в сроки, предусмотренные графиком, представляется в деканат для регистрации и рецензирования.
Проверенная работа возвращается студенту. При наличии замечаний рецензента, студенту следует выполнить все его указания и доработать вопросы работы в тетради после основного текста и после замечаний рецензента. Не рекомендуется доработку вопросов проводить на полях тетради.
Если работа выполнена в соответствии с указанными требованиями, преподаватель допускает ее к собеседованию. Для зачета по контрольной работе студенту необходимо иметь выполненную контрольную работу с отметкой преподавателя «Допущен к собеседованию».
Собеседование по работе проводит преподаватель, индивидуально беседуя с каждым студентом по вопросам работы.
По дисциплине «Биохимия» студент заочной полной формы обучения выполняет две контрольные работы, студент заочной сокращенной формы обучения – одну контрольную работу №1.
В контрольную работу №1 входят три теоретических вопроса и три задачи. В контрольную работу №2 – три теоретических вопроса и четыре задачи.
Студенты выполняют первое контрольное задание согласно своемушифру (двух последних цифр) до номера 50, если в номере шифра две последние цифры больше 50, следует из них вычесть 50 и оставшиеся две цифры являются вариантами контрольного задания.
Так, например, студент с шифром 538 выполняет вариант 38, а с шифром 295 - выполняет вариант 45 (295-50=245).
Вариант второй контрольной работы выполняется студентом в соответствии со специальностью и соответствует последней цифре шифра.
Вариант решения контрольной работы.
1. Напишите уравнения реакций, происходящих при нагревании аланина.
Решение:
α-Аминокислоты при нагревании образуют соответствующие им дикетопиперазины и воду:

2. Напишите формулы следующих дипептидов: а) аланилаланина, б) аланилглицина.
Решение:

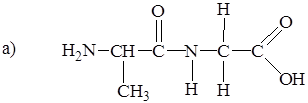
3. Напишите уравнения реакций синтеза глициллейцина.
Решение:
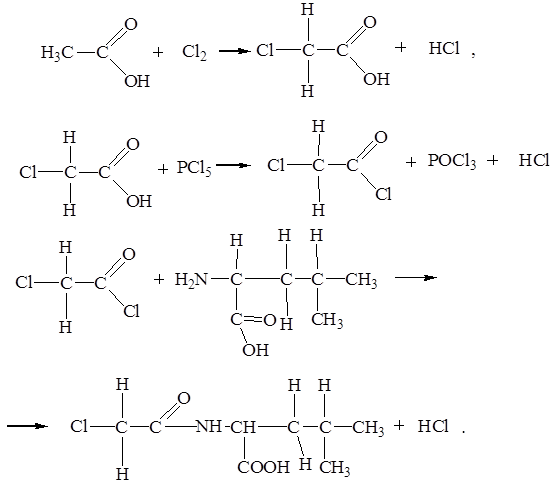
Для замещения хлора действуют далее аммиаком:

4. При действии надмуравьиной кислоты на полипептиды расщепляются дисульфидные мостики, а по месту каждого атома серы образуются сульфогруппы.
Напишите уравнения реакций окисления цистина с помощью надмуравьиной кислоты.
Решение:
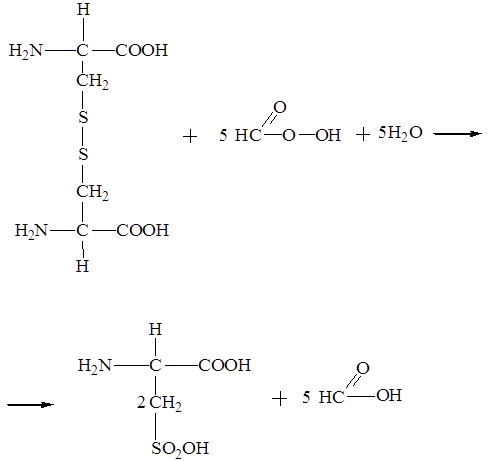
5. Нуклеозиды и основания, входящие в состав мононуклеотидов, подвергаются гидролизу при воздействии на них соответствующих ферментов. При этом выделяется аммиак.
Напишите уравнения реакций гидролиза оснований в соответствии со схемами:


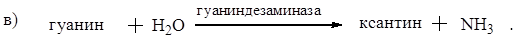
Решение:
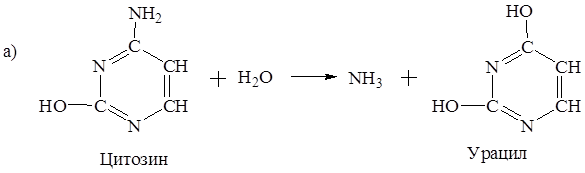
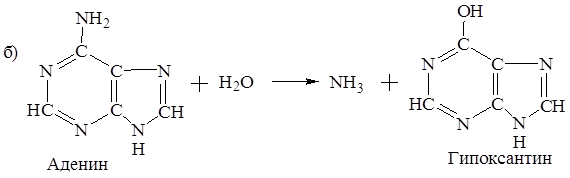

6. b-Оксибутиратдегидрогеназа окисляет D-b-оксимасляную кислоту (перенося водород на кофермент НАД) в ацетоуксусную кислоту.
Напишите уравнение этой реакции.
Решение:

7. Напишите уравнение реакции неконкурентного торможения при взаимодействии парахлормеркурбензоата с цистеином.
Решение:

8. L-аланин-2-оксоглутаратаминотрансфераза переносит аминогруппу:
L-аланин + a-кетоглутаровая кислота ® пировиноградная + a-глутаминовая кислота.
Напишите уравнение этой реакции.
Решение:
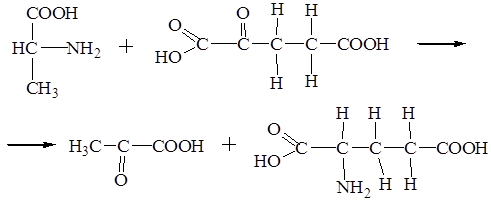
Контрольные задания.
Контрольная работа №1
Теоретические вопросы
Вариант 1
1. Классификация белков. Общая характеристика протеинов.
2. Лактоза и мальтоза. Химическое строение, свойства.
3. Специфические свойства ферментов, отличающие их от небиологических катализаторов.
Вариант 2
1. Молекулярная масса белков, методы ее определения (вискозиметрия, диффузия, ультрацентрифугирование).
2. Сахароза. Химическое строение и свойства. Ферментативный гидролиз сахарозы.
3. Витамины РР, химическое строение, свойства. Участие в построении коферментов.
Вариант 3
1. Современные представления о структуре белка. Типы связей, сохраняющие пространственную конфигурацию белков молекулы.
2. Строение и химические свойства трегалозы, целлобилозы. Какие промежуточные и конечные продукты образуются при гидролизе клетчатки?
3. Классификация ферментов. Характеристика гидролаз.
Вариант 4
1. Написать формулы следующих трипептидов:
а) аланил-лизил-цистеин,
в) глутамил-гистидил-триптофан,
в) фенилаланил-лейцил-аргинин. Укажите пептидные связи.
2. Химическое строение, свойства и биологическая роль крахмала и клетчатки.
3. Общая характеристика оксидоредуктаз. Анаэробные и аэробные дегидрогеназы. Химическое строение коферментов.
Вариант 5
1. Первичная структура белковой молекулы. Типы связей, формирующие первичную структуру белка.
2. Строение и свойства дисахаридов.
3. Написать формулы коферментов, в состав которых входит адениловая кислота.
Вариант 6
1. Химический состав белков.
2. Фосфолипиды, их формулы, свойства и применение в пищевой промышленности.
3. Витамины, входящие в состав ферментов. Привести примеры.
Вариант 7
1. Фракционирование белков (электрофорез, хроматография, высаливание). Осаждение белков. Нативные и денатурированные белки.
2. Моносахариды – гексозы и их производные: гексозамины и гексофорные эфиры.
3. Витамины, входящие в состав ферментов. Привести примеры.
Вариант 8
1. Третичная и четвертичная структура белка. Связи, формирующие пространственную конфигурацию белковой молекулы.
2. Физико-химические свойства моносахаридов, изображение гексоз с помощью перспективных формул.
3. Классификация ферментов. Характеристика изомераз.
Вариант 9
1. Классификация и характеристика аминокислот. Написать формулы незаменимых аминокислот.
2. Строение и химические свойства глюкозы, маннозы, галактозы и фруктозы. D- и L- ряды моносахаридов.
3. Рибофлавин (витамин В2), особенности структуры, обусловливающие его биологические свойства. Конферменты, содержащие рибофлавин.
Вариант 10
1. Физические и химические свойства белков. Полноценный белок.
2. Проектирование вещества, структура, свойства, использование в пищевой промышленности.
3. Общая характеристика и классификация липидов. Жиров: строение, свойства, распространение в природе.
Вариант 11
1. Пептиды и полипептиды. Получить два тетрапептида из следующих аминокислот: серина, метионина, лецина, фенилаланина.
2. Общая характеристика и классификация углеводов. Образование углеводов в растениях.
3. Одно- и двухкомпонентные ферменты. Простетические группы ферментов. Химическое строение важнейших коферментов.
Вариант 12
1. Белки как амфотерные электролиты. Изоэлектрическая точка белков.
2. Сахароза и мальтоза. Строение, свойства. Объяснить, почему сахароза не дает реакции на карбонильную группу.
3. Принцип классификации ферментов. Характеристика классов.
Вариант 13
1. Денатурация белков, обратимая и необратимая. Причины, вызывающие денатурацию белков.
2. Написать формулы важнейших моносахаридов – гексоз в ациклической и циклической форме и указать их химические свойства.
3. Современные данные о химической природе ферментов. Конферменты, их связь с витаминами. Привести примеры.
Вариант 14
1.Классификация и характеристика сложных белков. Строение простетической группы нуклеидов.
2. Витамины В1 и В2, их строение, роль в обмене веществ. Пищевые источники этих витаминов. Какие ферменты содержат эти витамины?
3.Липиды, общие свойства и особенности структуры. Отличие простых липидов от сложных. Привести примеры.
Вариант 15
1. Аминокислоты, строение, свойства, классификация. Написать формулы всех белковых аминокислот.
2. Строение трегалозы и сахарозы. Чем характеризуется трегалозный тип связи? Инверсия сахарозы и ее использование в пищевой промышленности.
3. Понятие о ферментах как о белковых веществах, обладающих каталитическими функциями. Активный центр ферментов. Основные положения ферментативного катализатора.
Вариант 16
1. Какими свойствами характеризуется белки?
2. Что такое гликозиды? Как определить принадлежность гликозида к D- или L-ряду? Написать перспективные формулы метал-α-D-глюкопиранозы и этил-β-D-фруктофуранозы.
3. Классификация липидов. Строение и свойства жиров, стероидов, воска.. Написать их формулы.
Вариант 17
1. Полноценные и неполноценные белки. Незаменимые аминокислоты, их биологическая роль и химическое строение (дать формулы).
2. Что такое мутаротация моносахаридов? Какими процессами обусловлено это заявление? Какими процессами обусловлено это явление?
3. Ингибиторы и активаторы ферментов.
Вариант 18
1. Классификация белков. Простые белки: альбумины, глобулины, протамины, гистоны, протеиноиды.
2. Трисахариды, тетрасахариды. Строение, свойства, продукты гидролиза.
3. Написать формулы витаминов С и Р. Указать характер связи между ними в обмене веществ и их биологическую роль. Их пищевые источники.
Вариант 19
1. Написать формулы всех встречающихся в белках аминокислот.
2. Полисахариды. Крахмал: строение, свойства, распространение в природе.
3. Провитамины и витамины. Образование витаминов D из эргостерола.
Вариант 20
1. Качественные реакции на белки. Приведите формулы циклических аминокислот.
2. Классификация углеводов, их биологическое значение, строение и свойства олигосахаридов.
3. Витамины группы А. Строение, биологическая роль, провитамины. Как идет преобразование провитамина в витамин?
Вариант 21
1. Написать структурные формулы и назвать дипептиды, получаемые из следующих аминокислот: а) гистидина и цистина, б) триптофана и лизина, в) изолейцина и цистеина, г) серина и глутамина.
2. Химические и физические свойства крахмала, гликогена и целлюлозы. Указать черты сходства и различия в их строении и свойствах.
3. Витамины, классификация. Провитамины, антивитамины и антогонисты витаминов.
Вариант 22
1. Классификация белков. Сложные белки: хромопептиды, гликопептиды, липопептиды, металлопептиды, нуклеопротеиды. Строение простетических групп нуклеотидов.
2. Крахмал, перспективная формула фрагмента молекулы амилопектина.
3. Классификация липидов. Химическое строение жиров и стеридов.
Вариант 23
1. Вторичная структура белков: α-спираль, β-складка. Какие связи формируют вторичную структуру белка?
2. Написать ациклическую и циклическую формулы α-D-глюкозы.
3. Химическое строение фосфолипидов. Их биологическое значение.
Вариант 24
1. Охарактеризуйте белки как амфотерные электролипиды. Что такое изоэлектрическая точка белка?
2. Сахароза и лактоза. Строение и свойства. Почему лактоза восстанавливает реактив Фелинга, а сахароза нет?
3. Что такое коферменты? Роль витаминов в построении коферментов. Привести формулы важнейших коферментов: НАД, НАДФ, ФАД, фосфопиридоксаля (ФП).
Вариант 25
1. Продукты неполного гидролиза белков. Номенклатура и строение ди-, три-, тетрапептидов. Привести примеры. Что такое полипептиды? Качественные реакции на пептидную связь.
2. Моносахариды - гексозы. Химическое строение, стереоизомерия моноз. Написать проекционные формулы моноз, эпимерных D-глюкозе.
3. Назовите и напишите формулу коферментной системы, в состав которой входит пантотеновая кислота. Роль КоА в обмене веществ.
Вариант 26
1. Физические и химические свойства белков.
2. Напишите уравнение гидролиза сахарозы, объясните, почему эту реакцию называют инверсией?
3. Принцип классификации ферментов.
Вариант 27
1. Какие типы связей формируют структуру белка?
2. Строение и свойства крахмала. Опишите различия в структуре амилопектина и крахмала.
3. Характеристика ферментов класса лиаз. Приведите примеры реакции.
Вариант 28
1. Вторичная структура белка, типы связей, обеспечивающих ее стабильность. Какие формы этой структуры наиболее распространены в нативных белках?
2. Напишите схему превращений D-глюкопиранозы и D-маннопиранозы при мутаротации.
3. Характеристика ферментов класса оксидоредуктаз.
Вариант 29
1. Строение нуклеотидов и нуклеозидов. Приведите примеры.
2. Растительные масла: строение, физические и химические свойства.
3. Ферменты класса оксидоредуктаз. Цитохромная система.
Вариант 30
1. Структурные элементы нуклеиновых кислот: азотистое основание, углевод, фосфорная кислота. Изобразите химическое строение.
2. Высшие жирные кислоты, участвующие в образовании природных жиров. Приведите примеры простого и сложного триглицерида. Назовите их.
3. Особенности ферментов как биологических катализаторов.
Вариант 31
1. Полинуклеотиды. Поясните структурные элементы, приведите примеры.
2. Углеводы. Характеристика моносахаридов и дисахаридов.
3. Антивитамины. Приведите примеры.
Вариант 32
1. ДНК. Первичная структура ДНК.
2. На примере глюкозы и фруктозы покажите строение их пиранозных и фуранозных форм.
3. Дегидрогеназы. Общие характеристики. Строение. Участие витаминов в образовании коферментов.
Вариант 33
1. ДНК. Вторичная и третичная структура ДНК. Типы связей.
2. Моносахариды. Образование циклической формы гексоз.
3. Ферменты класса оксидоредуктаз. Анаэробные дегидрогеназы.
Вариант 34
1. РНК. Структура РНК.
2. Липиды. Строение сложных липидов.
3. Ферменты класса оксидоредуктаз. Характеристика оксидаз.
Вариант 35
1. Два типа нуклеиновых кислот. Строение и химические свойства.
2. Крахмал, строение, свойства. Приведите фрагменты формул. Использование крахмала в пищевой промышленности.
3. Ферменты класса трансфераз.
Вариант 36
1. Соединения с макроэргическими связями. АТФ. Структура, функции. Приведите уравнения биохимических реакций с участием АТФ.
2. Структурные составляющие крахмала: амилоза и амилопектин. Приведите фрагменты формул, опишите их свойства.
3. Ферменты класса изомеров. Приведите уравнения биохимических реакций с участием изомера.
Вариант 37
1. Различие в строении ДНК и РНК. Локализация в органеллах клетки.
2. Аскорбиновая кислота. Строение, биологическая роль.
3. Сходство и различия биологических и химических катализаторов.
Вариант 38
1. Нуклеиновые кислоты. Их строение и роль в жизнедеятельности организма.
2. Сахара. Строение, физические и химические свойства.
3.Ферменты класса лиаз.
Вариант 39
1. Соединения с макроэргическими связями. Их строение, биологическая роль.
2. Витамины группы В. Структура, биологическая роль.
3. Ферменты класса гидролаз. Протеолитические ферменты.
Вариант 40
1. Нуклеиновые кислоты. Охарактеризуйте пуриновые и пиримидиновые основания, входящие в состав нуклеиновых кислот.
2. Каротины и каротиноиды. Строение и биологическая роль, содержание в растворах.
3. Ферменты класса оксидоредуктаз. Оксидазы, полифенолоксидазы.
Вариант 41
1. Протеиды. Их классификация. Важнейшие представители каждой группы.
2. Пектиновые вещества, строение, свойства, применение в пищевой промышленности.
3. Витамины группы К, их строение, свойства, биороль, пищевые источники.
Вариант 42
1. Протеиды. Хромопротеиды. Опишите структуру гема, приведите формулу, укажите, в состав каких ферментов входит гем?
2. Пентозы и пентозаны. Строение, свойства, содержание в растениях.
3. Ферменты, их активаторы и ингибиторы. Приведите примеры.
Вариант 43
1. Ферментативный гидролиз белков. Продукты полного и неполного гидролиза. Аминокислотный состав растительных белков. Незаменимые аминокислоты.
2. Дисахариды. Их строение, свойства, применение в пищевой промышленности.
3. Различия в свойствах и строении растительного масла и жира.
Вариант 44
1. Денатурация белков. Причины ее вызывающие. Использование в пищевой промышленности.
2. Жирорастворимые витамины А и D. Строение, биологическая роль, пищевые источники.
3. Химическая природа ферментов. Роль активного центра в катализе.
Вариант 45
1. Глутатион. Строение, химические свойства, биологическая роль.
2. Витамин PP. Химическое строение, биологическая роль, приведите примеры
коферментных систем, в образовании которых участвует витамин РР, напишите формулы. Укажите пищевые источники витамина PP.
3. Фосфорные группы глюкозы, фруктозы. Образование их при дыхании растений. Приведите уравнения биологических реакций, укажите ферменты, охарактеризуйте роль АТФ.
Вариант 46
1. Напишите структурные формулы АМФ (адениловой кислоты) и уридин-5-фосфата. Как может идти образование динуклеотидов? Укажите тип связей.
2. Липиды. Строение растительных масел и животных жиров. Отличие в обмене веществ.
3. Классификация витаминов. Провитамины.
Вариант 47






