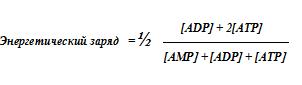Окисление, сопряженное с синтезом АТР, называется сопряженным окислением, которое может осуществляться двумя путями: на уровне субстрата и на уровне электронтранспортной цепи.
В ходе реакций окисления электроны, находящиеся на высокоэнергетическом уровне в молекуле восстановителя (водорода), переходят на низкоэнергетическую орбиталь в молекуле окислителя, где они сильнее притягиваются ядрами атомов. Способность молекулы принимать электроны оценивается по величине окислительно-восстановительного потенциала (Е). Отрицательная величина Е обозначает низкое сродство, положительная – высокое сродство. В биологии используется стандартный Е′0 (нормальный потенциал), определяемый при параметрах 25°С, 1 моль/л, 1 атм, рН=7,0. В процессе окисления перенос электронов происходит по направлению от более отрицательного к более положительному потенциалу (Рис.26.1).
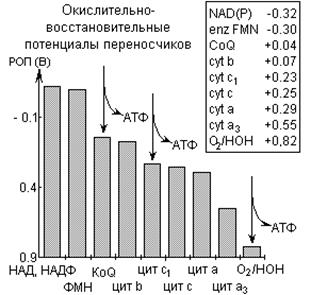
Рис.26.1. Окислительно-восстановительные потенциалы электронтранспортной цепи
Электроны при отрицательном значении потенциала являются «высокоэнергетическими» и при переходе к системе с более высоким значением потенциала они теряют часть своей энергии и способны произвести работу.
Примером сопряженного окисления на уровне субстрата могут служить реакции окисления 3-фосфоглицеринового альдегида в 1,3-дифосфоглицерат, 2-фосфоглицерата – в 2-фосфоенолпируват (реакции гликолиза). С возникающих в ходе этих реакций соединений фосфат, связанный макроэргической связью, легко передается на ADP. Однако посредством реакций субстратного фосфорилирования образуется сравнительно небольшое количество АТР.
Наиболее прост механизм образования АТР при окислении 2-фосфоглицерата. Эта реакция, катализируемая енолазой, представляет собой внутримолекулярное окисление, в результате которого образуется богатое энергией фосфорное соединение – фосфоенолпируват:
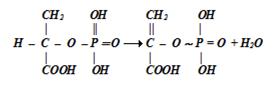
Окисление ведет к уменьшению плотности электронов на атоме фосфора в молекуле фосфоенолпирувата. Это придает фосфорильному остатку способность взаимодействовать с молекулой ADP, что приводит к синтезу АТР:
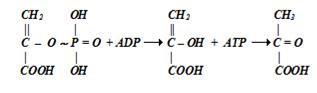
В соответствии со схемой химического сопряжения в этой реакции функции донора электронов, акцептора электронов и акцептора энергии окисления выполняют различные атомарные группировки в молекуле одного и того же вещества – 2-фосфоглицерата. В роли первичного макроэргического соединения, аккумулирующего энергию окисления, выступает один из продуктов реакции – фосфоенолпируват.
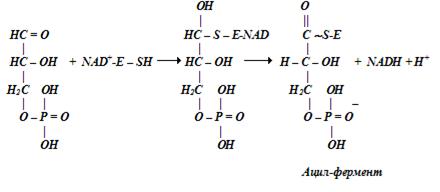
Фосфорилирование при анаэробном окислении глицеральдегид-3-фосфата происходит более сложным путем. Окисление субстрата является результатом взаимодействия с комплексом фермент-NAD. Вначале альдегид-ферментный комплекс окисляется до ацилфермента, а затем под действием неорганического фосфата тиоловый эфир расщепляется с образованием мак-роэргического соединения ‒ 1,3-дифосфоглицерата:
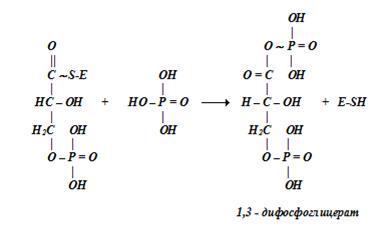
В последующем под действием фермента фосфоглицераткиназы макроэргическая фосфатная группа этого соединения переносится на ADP с образованием АТР:
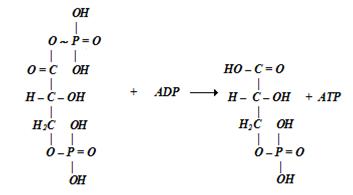
В роли донора электронов в этой реакции выступает глицеральдегид-3-фосфат, вступающий в соединение с ферментом. Роль акцептора электронов выполняет NAD+, в качестве компонента сопряжения выступает SH-группа фермента, первичное высокоэнергетическое соединение представлено ацил-ферментом.
Энергетическое состояние клетки можно оценить с помощью энергетического заряда. Согласно Аткинсону, энергетическое состояние клетки лучше всего может быть охарактеризовано степенью «заполнения» системы АТР-ADP-АМР высокоэнергетическими фосфатными связями. Если все содержащиеся в клетке аденозинфосфаты находятся в форме АТР, это означает, что система энергетически заполнена до предела, т.е. ее энергетический заряд равен 1,0. Другому предельному состоянию соответствует случай, когда все содержащиеся в клетке аденозинфосфаты находятся в форме АМР. В этом случае система не содержит высокоэнергетических связей, т.е. она энергетически «пуста» и ее энергетический заряд равен 0. Если все аденозинфосфаты находятся в форме ADP или эквимолярной смеси АТР и АМР, это значит, что система заполнена высокоэнергетическими связями наполовину, т.е. ее энергетический заряд равен 0,5. Энергетический заряд системы АТР, ADP, АМР можно легко вычислить для любого соотношения концентраций АТР, ADP и АМР при помощи уравнения