В промышленной теплотехнике и теплоэнергетике водяной пар может встречаться либо как греющий теплоноситель в теплоиспользующих установках, либо как рабочее тело в паровых двигателях, либо как компонент в парогазовых смесях.
В последнем случае пар обычно имеет невысокое парциальное давление и его можно рассматривать как достаточно разреженный газ, приближающийся по своим свойствам к идеальному газу. Поэтому для водяного пара как компонента влажного воздуха или продуктов сгорания топлива применимо уравнение состояния идеального газа: pv = RT.
Однако гораздо чаще водяной пар используется в различных установках и двигателях при сравнительно высоком давлении или в состояниях, близких к границе фазового перехода из газа в жидкость. В этом случае уже нельзя пренебрегать собственным объемом молекул и силами сцепления между ними, т. е. модель идеального газа и уравнение его состояния не подходят для водяного пара.
Наиболее простое уравнение состояния реального газа, предложенное Ван дер Ваальсом в 1873 г., имеет вид:
 , (4.1)
, (4.1)
где a и b – постоянные величины, зависящие от природы газа.
Структура уравнения (4.1) говорит о том, что в основе его лежит уравнение состояния идеального газа, в которое внесены поправки. Одна из них учитывает силы взаимодействия между молекулами реального газа и называется внутренним давлением. Величина его обратно пропорциональна квадрату удельного объема газа: а / v2. Другая поправка учитывает объем недоступности для перемещения молекул b, который составляет примерно учетверенный объем самих молекул.
Уравнение Ван дер Ваальса (4.1) получило качественное подтверждение в опытах по изотермическому сжатию углекислого газа, проведенных английским физиком Т. Эндрюсом. Однако с количественной стороны оно является весьма приближенным, так как не учитывает явления ассоциации молекул.
Дальнейшие попытки усовершенствования уравнения состояния реальных газов привели к созданию разными авторами достаточно точных зависимостей, однако их громоздкость и сложность не позволяют широко использовать эти уравнения в практических расчетах. Поэтому термодинамические свойства и процессы изменения состояния применяемых в теплотехнике паров и жидкостей изучаются и анализируются с помощью специальных таблиц или диаграмм состояния.
Рассмотрим принцип построения р, v-диаграммы воды и водяного пара. Проследим за процессом парообразования и изменением объема воды, если к ней подводить тепло при постоянном давлении р1. Точка a1, лежащая на изобаре p1 = const, характеризует состояние воды при 0 °С. Участок a1 – b1 (рис. 4.1) соответствует подогреву воды до температуры кипения.
 Процесс парообразования b1 – с1 происходит при постоянной температуре насыщения, пока не выкипит вся вода (точка с1). Далее идет перегрев пара с1 – d1. Повысив давление до р2, а затем до р3 и т. д., можно получить аналогичные характерные точки. Линия, соединяющая точки а1 а2, а3, …, характеризует состояние воды при 0 °С. В силу малой сжимаемости жидкости она практически вертикальна. Левая ветвь кривой, соединяющая точки b1, b2, b3, …, отражает состояние воды в момент начала кипения. Она разделяет области жидкости и влажного пара и называется нижней пограничной кривой. Правая ветвь, проходящая через точки с1, с2, с3, …, является линией сухого насыщенного пара, которая отделяет области влажного и перегретого пара. Она называется верхней пограничной кривой. С ростом давления пограничные кривые сближаются, а затем сходятся в точке К, называемой критической. В этой точке исчезает видимое различие между жидкостью и паром. Критические параметры для каждого вещества имеют вполне определенные значения. Для воды ркр = 221,15 бар; tкр = 374,12 °С; vкр = 0,003147 м3/кг. Влажный пар, занимающий на диаграмме область между пограничными кривыми, представляет собой механическую смесь пара и капелек воды. Содержание пара в этой смеси оценивается степенью сухости
Процесс парообразования b1 – с1 происходит при постоянной температуре насыщения, пока не выкипит вся вода (точка с1). Далее идет перегрев пара с1 – d1. Повысив давление до р2, а затем до р3 и т. д., можно получить аналогичные характерные точки. Линия, соединяющая точки а1 а2, а3, …, характеризует состояние воды при 0 °С. В силу малой сжимаемости жидкости она практически вертикальна. Левая ветвь кривой, соединяющая точки b1, b2, b3, …, отражает состояние воды в момент начала кипения. Она разделяет области жидкости и влажного пара и называется нижней пограничной кривой. Правая ветвь, проходящая через точки с1, с2, с3, …, является линией сухого насыщенного пара, которая отделяет области влажного и перегретого пара. Она называется верхней пограничной кривой. С ростом давления пограничные кривые сближаются, а затем сходятся в точке К, называемой критической. В этой точке исчезает видимое различие между жидкостью и паром. Критические параметры для каждого вещества имеют вполне определенные значения. Для воды ркр = 221,15 бар; tкр = 374,12 °С; vкр = 0,003147 м3/кг. Влажный пар, занимающий на диаграмме область между пограничными кривыми, представляет собой механическую смесь пара и капелек воды. Содержание пара в этой смеси оценивается степенью сухости
 , (4.2)
, (4.2)
где Мп и Мв – масса пара и воды в смеси. В начале кипения x = 0, в конце парообразования х = 1.
Основные параметры кипящей воды v', h', s' и сухого насыщенного пара v", h", s" приведены в таблице работы [4] в зависимости от температуры насыщения tн или давления насыщения рн. Для перегретого пара также существуют таблицы, пользуясь которыми можно по двум известным параметрам – температуре и давлению – найти для данного состояния удельный объем, энтальпию и энтропию пара.
В области же влажного пара при 0 < х < 1 параметры определяются расчетом. Так, удельный объем влажного пара складывается из удельных объемов воды (1 – x)v' и пара хv", т. е.
 . (4.3)
. (4.3)
Заметим, что первое слагаемое существенно меньше второго, поэтому им часто пренебрегают, считая v ≈ xv".
Аналогично рассуждая, можно получить формулу энтальпии влажного пара:
 (4.4)
(4.4)
или
 . (4.5)
. (4.5)
Разность энтальпий h" – h' представляет собой количество тепла, необходимое для превращения 1 кг воды в пар при некотором давлении р = const. Оно называется теплотой парообразования: r = h" – h'. Тогда выражение (4.5) можно записать в виде:
 . (4.6)
. (4.6)
Формула для определения энтропии влажного пара по аналогии с уравнением (4.5) имеет вид:
 . (4.7)
. (4.7)
Внутренняя энергия пара определяется из выражения:
 , (4.8)
, (4.8)
которое справедливо для любого состояния воды и водяного пара.
За начало отсчета внутренней энергии и энтропии принята тройная точка воды, т. е. такое состояние, в котором Н2О находится одновременно в трех фазах. Энтальпию воды в этой точке тоже можно принимать равной нулю. Остальные параметры тройной точки: р = 0,0061 бар; v = 0,001 м3/кг; t = 0,01 °C.
Рассмотрим характер и расположение изобар воды и водяного пара в Т, s-диаграмме. Если подводить тепло при р = const, то элементарное изменение энтропии можно записать в виде:
 . (4.9)
. (4.9)
Интегрируя уравнение (4.9) в пределах от T0 = 273,15 K до Т и учитывая, что при температуре Т0 энтропия равна нулю, получаем
 . (4.10)
. (4.10)
Полученное уравнение отражает логарифмический характер изобары нагревания воды в Т, s-координатах. Начало этой изобары независимо от величины давления находится в точке а (рис. 4.2), отстоящей от начала координат на величину T0 = 273,15 K. Температура кипения увеличивается с ростом давления, поэтому точки b1 b2, b3, …, характеризующие начало парообразования при соответствующих давлениях, находятся на различных температурных уровнях. В области влажного пара изобара совпадает с изотермой и располагается горизонтально. Характер изобары в области перегретого пара можно проанализировать, переписав выражение (4.9) в виде:
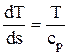 . (4.11)
. (4.11)
Ошибка! Ошибка связи. 
Рис. 4.2 Рис. 4.3
Наклон кривой p = const, характеризуемый производной dT / ds, определяется температурой перегрева и теплоемкостью перегретого пара. Вблизи состояния насыщения сp имеет большие значения, затем уменьшается и при высокой температуре зависимость ср от Т становится незначительной. Изобары вблизи точек с1 c2, с3 идут сравнительно полого, затем крутизна их увеличивается, характер кривой приближается к экспоненциальной. Таким образом, линия изобарного процесса нагрева воды, парообразования и перегрева пара имеет ломаный ступенчатый характер с горизонтальным участком в области влажного пара.
Поскольку площадь под любым процессом в Т, s-диаграмме характеризует количество подведенного пли отведенного тепла, то площадь под участком кривой ab1 (см. рис. 4.2) отражает количество тепла, пошедшего на нагревание воды от Т0 до температуры кипения.
При изобарном нагревании воды qa–b1 = hb1 – ha. Так как ha = 0, то энтальпия h' точки b1 численно равна площади под изобарой ab1. Точно так же площадь под процессом кипения b1c1 равна теплоте парообразования r = h" – h', а энтальпия точки с1 h" = h' + r. Тепло, затраченное на перегрев пара, равно площади под процессом с1d1.
Тепловая диаграмма T, s полезна при анализе термодинамических процессов и циклов. Однако для расчетов более удобна диаграмма состояния h, s, позволяющая определять энтальпии точек не в виде площадей, а в виде отрезков. Построение диаграммы производится следующим образом. По табличным значениям h', s', h", s" строят пограничные кривые x = 0 и х = 1 (рис. 4.3).
Точки равных давлений соединяют прямыми линиями, которые в области влажного пара образуют веерообразный пучок прямых, исходящих из начала координат. Одновременно эти прямые являются изотермами. Из уравнения
Tds = dh – vdp при p = const имеем:
 . (4.12)
. (4.12)
Поскольку в области влажного пара T = const, то наклон изобары в h, s-диаграмме постоянен, причем он растет с увеличением Т.
Уравнение (4.12) дает объяснение и положению критической точки К, которая в h, s-диаграмме не лежит в вершине пограничной кривой. Действительно, тангенс угла наклона касательной в точке К будет равен Tкр, в то время как в Т, s-диаграмме  . В области перегретого пара температура его растет, поэтому изобары становятся нелинейными с увеличивающейся кривизной. Изотермы расходятся с изобарами и по мере удаления от пограничной кривой x = l становятся почти горизонтальными.
. В области перегретого пара температура его растет, поэтому изобары становятся нелинейными с увеличивающейся кривизной. Изотермы расходятся с изобарами и по мере удаления от пограничной кривой x = l становятся почти горизонтальными.
Часто в h, s-диаграмме наносятся и изохоры, которые проходят несколько круче изобар. В области влажного пара строятся линии постоянной сухости
x = const. Нижняя часть диаграммы в теплотехнических расчетах обычно не используется. Это позволяет выполнить рабочую часть диаграммы в более крупном масштабе. Покажем изображение некоторых процессов в h, s-диаграмме и их расчет.
Расчет того или иного процесса обычно сводится к определению недостающих параметров начала и конца процесса, вычислению тепла q1–2, изменения внутренней энергии Du1–2 и работы l1–2.
Изохорный процесс v = const подвода тепла располагается в h, s-диаграмме (рис. 4.4) круче изобар. Точка 1 может быть задана давлением pl (или температурой t1) и степенью сухости x1. Состояние точки 2 в области перегретого пара обычно задается давлением р2 или температурой t2.






