Поверхневі явища і адсорбція
На поверхні твердого або рідкого тіла можуть поглинатись газоподібні або розчинені речовини. Такий процес називається адсорбцією. Речовину, яка адсорбується на поверхні твердого або рідкого тіла, називають адсорбтивом, а речовину, що адсорбує, – адсорбентом.
Кількість речовини, адсорбованої одиницею поверхні адсорбента, називають поверхневою концентрацією або питомою адсорбцією (г/см2 або кг/м2).
Кількісну характеристику здатності речовини адсорбуватися на поверхні поділу двох фаз залежно від поверхневих сил описано рівнянням Гіббса:
 ,
,
де Г і С – адсорбція (поверхневий надлишок речовини) і концентрація речовини в розчині; R - універсальна газова стала; Т – температура, оК; s – поверхневий натяг.
При  >> 0, Г < 0, тобто адсорбція негативна, а якщо
>> 0, Г < 0, тобто адсорбція негативна, а якщо  <0, Г >0, тобто адсорбція позитивна. Поряд з адсорбцією завжди відбувається і зворотній процес – десорбція, коли молекули покидають поверхню поділу. Ці протележні процеси протікають паралельно. Рівновага має динамічний характер. Кількісно адсорбційна речовина описується рівнянням Фрейндліха,
<0, Г >0, тобто адсорбція позитивна. Поряд з адсорбцією завжди відбувається і зворотній процес – десорбція, коли молекули покидають поверхню поділу. Ці протележні процеси протікають паралельно. Рівновага має динамічний характер. Кількісно адсорбційна речовина описується рівнянням Фрейндліха, 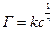 , де Г – адсорбція; с – концентрація, k та
, де Г – адсорбція; с – концентрація, k та 
 – константи. Якщо побудувати графік у координатах
– константи. Якщо побудувати графік у координатах  ; то можна знайти значення констант, де х – кількість адсорбованої речовини; m – кількість адсорбенту; tga = 1/n.
; то можна знайти значення констант, де х – кількість адсорбованої речовини; m – кількість адсорбенту; tga = 1/n.
 |
Lg
Lg K Lg C
a
Ізотерма Фрейндліха в координатах: Lg  - Lg C.
- Lg C.
Адсорбцію на поверхні твердого тіла вимірюють так: визначають концентрацію речовини, що адсорбується в розчині після встановлення адсорбційної рівноваги, а також концентрацію речовини, до контакту з адсорбентом, за різницею між вихідною концентрацією і концентрацією, що встановлюється при адсорбційній рівновазі, визначають кількість адсорбованої речовини.
Кількість адсорбованої речовини розраховують за формулою:
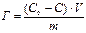 ,
,
де Со – вихідна концентрація;
С - рівноважна концентрація;
V - об’єм розчину в колбі;
m - наважка вугілля.
Хроматографія
Хроматографічний метод аналізу є універсальним методом розділення складних сумішей речовин на окремі компоненти. Метод заснований на різниці в розподілі компонентів суміші між двома фазами. Одна з фаз – нерухомий шар твердої речовини або рідини з великою поверхнею (нерухома фаза), друга фаза (рухома фаза) - потік рідини або газу, що фільтрується через нерухомий шар. Процес складається з повторення великої кількості елементарних актів сорбції (поглинання) – десорбції (виділення), в результаті чого і відбувається розділення суміші на окремі компоненти.






