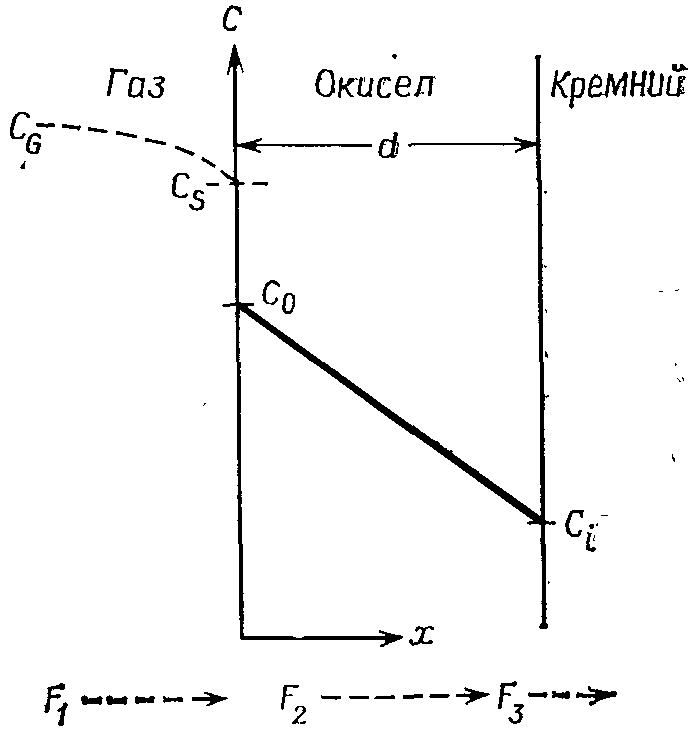
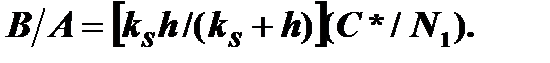 Окисляющие элементы диффундируют из объёма газовой среды на границу раздела газ – окисел (поток F1), переносятся через уже образованный окисел по направлению к кремнию (поток F2)
Окисляющие элементы диффундируют из объёма газовой среды на границу раздела газ – окисел (поток F1), переносятся через уже образованный окисел по направлению к кремнию (поток F2)
и реагируют на границе раздела фаз Si-SiO2 с кремнием (поток F3). CG – концентрация окислителя в объёме газовой фазы; СS – вблизи поверхности окисла; С0 – равновесная концентрация в окисле на внешней стороне; Сi – вблизи границы раздела фаз.
Уравнение для потока F1
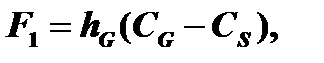 Поток F1 пропорционален разности концентраций окислителя:
Поток F1 пропорционален разности концентраций окислителя:
где hG – коэффициент массопереноса в газовой фазе.
Согласно закону Генри:

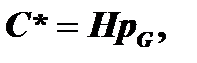
где С*-равновесная объёмная концентрация в окисле, pS –парциальное давление в газовой фазе вблизи поверхности окисла, pG – парциальное давление в объёме газовой фазы, Н – постоянная Генри.

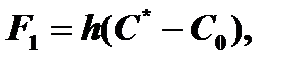
 При использовании закона Генри совместно с законом идеальных газов:
При использовании закона Генри совместно с законом идеальных газов:
где h – коэффициент массопереноса в газовой фазе, определяемый как:
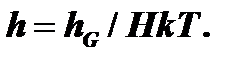
Уравнение для потока F2
 Поток частиц окислителя через окисел для любой точки d описывается законом Фика:
Поток частиц окислителя через окисел для любой точки d описывается законом Фика:
где D – коэффициент диффузии, dC/dd – градиент концентрации частиц окислителя в окисле.
 При установившемся процессе поток F2 одинаков для любой точки окисла (dF2/dd=0):
При установившемся процессе поток F2 одинаков для любой точки окисла (dF2/dd=0):
где d0 – толщина окисла.
Уравнение для потока F3
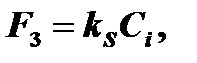
Поток, соответствующий реакции, пропорционален Ci:
где kS – константа скорости химической реакции окисления кремния.
Решение уравнений для Сi и С0

 Для установившегося потока соблюдается условие F1=F2=F3. Тогда совместное решение уравнений
Для установившегося потока соблюдается условие F1=F2=F3. Тогда совместное решение уравнений
даёт следующие выражения для Сi и С0:
Предельные случаи уравнений для Сi и С0
1. Если D слишком мал, то Сi→0, C0→C*,
т.е. реакция идет при диффузионном контроле.
2. Если D слишком велик, то реакция идет при кинетическом контроле: Сi=C0→C*/(1+kSh).
Определение числа молекул окислителя, входящих в состав SiO2
Окисел содержит 2,2×1022 молекул SiO2 в 1 см3. На создание одной молекулы SiO2 требуется одна молекула O2 или 2 молекулы H2O.
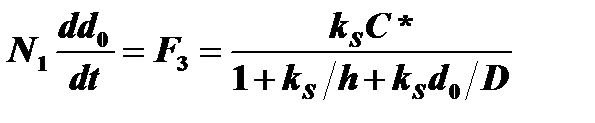 Таким образом число молекул окислителя,входящих в 1 см3 окисла (N1) составляет:-,4×1022 для окисления в парах воды. 2,2×1022 для окисления в сухом кислороде
Таким образом число молекул окислителя,входящих в 1 см3 окисла (N1) составляет:-,4×1022 для окисления в парах воды. 2,2×1022 для окисления в сухом кислороде
Тогд4а:
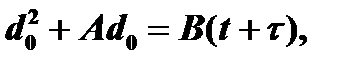 Зависимость толщины отвремени процесса
Зависимость толщины отвремени процесса
(*)
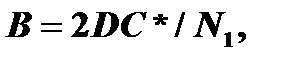

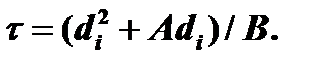 где:
где:
 Величина τ соответствует сдвигу по временной оси, учитывающему наличие первоначального слоя окисла толщиной di.
Величина τ соответствует сдвигу по временной оси, учитывающему наличие первоначального слоя окисла толщиной di.
Тогда решение (*) имеет вид:
Предельные случаи решения уравнения для толщины окисла
1.  Большое время окисления (t>>τ):
Большое время окисления (t>>τ):
 Уравнение представляет собой параболический закон, В – параболическая константа скорости окисления.
Уравнение представляет собой параболический закон, В – параболическая константа скорости окисления.
2. Малое время окисления (t+τ)<<A2/4B:
Уравнение представляет собой линейный закон,
В/А – линейная константа скорости окисления: