Вирусология — учение о вирусах. Им присущ строгий внутриклеточный паразитизм, осуществляемый на молекулярно-генетическом уровне. Многие вирусные болезни животных (ящур, чума крупного рогатого скота, классическая и африканская чума свиней, оспа овец, ньюкаслская болезнь и ряд других) представляют большую опасность и приносят значительный экономический ущерб. (Классификацию вирусов см. в главе 1 раздела I).
Вирусы обладают свойствами, отличающими их от других микроорганизмов: они очень малы, способны проходить через бактериальные фильтры, не культивируются на искусственных питательных средах. Для вирусов характерны две формы существования: внеклеточная, или покоящаяся, внутриклеточная, или размножающаяся (комплекс вирус — клетка).
Вирусы имеют корпускулярную структуру и определенную для каждого вида морфологию. Величина их варьирует в широких пределах: возбудитель ящура размером до 30 нм, вирус коровьей оспы около 200 нм. Величину вируса определяют фильтрацией через фильтры с известной величиной пор, центрифугированием в скоростных центрифугах, что позволяет по скорости оседания судить о величине частиц, и, наконец, исследованием в электронном микроскопе.
Инфекционные единицы вирусов называют вирионами. Каждый вирион состоит из нуклеиновой кислоты (ДНК или РНК), окруженной оболочками. Белковую оболочку называют капсидом. Структура, состоящая из нуклеиновой кислоты и окружающего ее капсида, именуется нуклеокапсидом. Различают два типа симметрии строения капсида: кубический и спиральный. У некоторых вирусов капсиды окружены второй липо- или гликопротеидной оболочкой.
Нуклеиновая кислота несет в себе наследственные признаки, она непосредственно участвует в синтезе белка и, кроме того, является фактором инфекционности вируса, а белок обеспечивает антигенную специфичность и стимулирует образование антител.
При ряде вирусных болезней (оспа, бешенство) обнаруживают внутриклеточные тельца-включения (элементарные тельца), что имеет диагностическое значение. По составу они разнообразны, но в большинстве своем состоят из вирусных частиц.
Очистка и концентрация вирусов. Достигаются путем фильтрации через специальные фильтры с использованием синтетических смол и полимерных материалов, а также путем ультраскоростного центрифугирования. Эти методы позволяют также выделить отдельные компоненты (фракции) вирусов.
Устойчивость вирусов. К воздействию факторов внешней среды и разного рода физических факторов и химических веществ устойчивость вирусов различна и зависит от их строения и химического состава, наличия защитных оболочек, среды, в которой находится вирус. Степень устойчивости соответствует механизму передачи вируса. Наиболее устойчивы вирусы, которые передаются алиментарным путем (классическая чума свиней, ящур) или через наружные покровы (контагиозный пустулезный дерматит овец и коз). Менее устойчивы вирусы, передающиеся воздушно-капельным (респираторным) или трансмиссивным путем.
Культивирование вирусов. Для размножения вирусов необходимо наличие живых чувствительных к нему клеток. Поэтому культивирование вирусов осуществляют в организме восприимчивых животных, в клетках куриных эмбрионов и клетках культур тканей.
В клетку проникает нуклеиновая кислота вируса. В соответствии с заложенной в ней генетической информацией живая клетка начинает производить ферментные системы, а затем белковые компоненты и нуклеиновую кислоту возбудителя. После этого происходит «сборка» составных частей вируса из белковых молекул и нуклеиновой кислоты. Накопление вирусных частиц приводит, как правило, к разрушению клетки и выделению вирионов во внешнюю среду.
Различают два типа клеточных культур: 1) клетки культур переживающих тканей (первично трипсинизированные) получают путем механического (измельчение) и ферментативного (трипсинизация) расщепления тканей из почек животных, плаценты, сердца, куриных эмбрионов (фибробласты куриного эмбриона); 2) клетки культур растущих тканей (перевиваемые) получают чаще всего из злокачественных опухолей. Используют также культуры диплоидных клеток, которые не опасны в канцерогенном отношении.
Выращивание культур клеток чаще производят в однослойных (монослойных) культурах. В этом случае клетки, внесенные в стеклянный сосуд, прикрепляются к одной из его стенок, образуя слой толщиной в одну клетку. Модификации этого метода — выращивание культур клеток во вращающихся сосудах (роллерный метод), на пластинках, помещенных в сосуд, на микроносителе (гранулы полимерных материалов, на поверхности которых образуется монослой клеток). Большинство вирусов по мере роста в однослойных культурах вызывают дегенерацию и гибель клеток, что называют цитопатогенным действием (ЦПД). Таким свойством обладают вирусы ящура, ньюкаслской болезни. Специфичность ЦПД устанавливают с помощью реакции нейтрализации со специфической сывороткой. Однако имеются вирусы, которые размножаются без проявления ЦПД (вирус классической чумы свиней). Существует также метод глубинного выращивания вирусов, при котором клетки находятся во взвешенном состоянии (в перемешиваемых суспензиях). Рост культур клеток и размножение вирусов происходят в питательных средах, содержащих аминокислоты, витамины, соли, глюкозу, сыворотку и другие вещества.
Патогенное действие вирусов. Действие вирусов на организм животного сопровождается поражением чувствительных клеток, местными и общими реакциями. На месте размножения вируса наблюдают распад клеток (например, слущивание эпителия), что зачастую сопровождается внедрением бактериальной флоры и накоплением различных токсических веществ, всасывание которых приводит к повышению температуры тела, нарушению обмена веществ. Специфичность действия вирусов связана с избирательным поражением определенных органов и тканей — тропизмом. Вирус ящура, например, поражает в основном эпителиальные ткани, а бешенства — нервную ткань.
Общие реакции проявляются, прежде всего, повышением температуры тела, угнетением, отказом от корма. Отмечают также изменение форменных элементов крови и ее состава, образование антител, нарушение деятельности сердечно-сосудистой, дыхательной, пищеварительной систем, возникновение патологоанатомических изменений (воспалительные процессы лимфоидной ткани и др.).
Установлена возможность длительного вирусоносительства. Примером может служить вирус герпеса, патогенное действие которого проявляется лишь на фоне ослабления резистентности организма. Некоторые вирусы (вирус классической чумы свиней) могут также длительно находиться в организме переболевшего животного.
(Иммунитет при вирусных болезнях см. в главе 2 раздела II.)
Вирусологическое исследование. Это комплекс лабораторных исследований, направленных на распознавание этиологии болезни, выделение и изучение вируса-возбудителя, а также на обнаружение в крови больных и переболевших животных специфических антител.
Выделение вируса зависит от правильности взятия и хранения материала. Вирус выделяют путем заражения лабораторных животных, развивающихся куриных эмбрионов или культуры тканей. С целью дальнейшего изучения вирусы культивируют на чувствительных объектах. Изучают биологические свойства выделенного вируса: устойчивость к воздействию разных температур, красителей, лучистой энергии, рН среды, течение болезни у лабораторных животных. В реакциях связывания комплемента, нейтрализации, иммунофлюоресценции, гемагглютинации и задержки гемагглютинации, преципитации и др. определяют антигенные свойства выделенного вируса. Некоторые из этих реакций используют и для определения наличия антител в крови животных по заведомо известному вирусному антигену. По комплексу признаков, присущих выделенному вирусу, производят его идентификацию, т.е. устанавливают принадлежность к определенному виду. Совокупность данных эпизоотологических, клинических, патологоморфологических, вирусологических и серологических исследований позволяет поставить диагноз при возникновении болезни вирусной этиологии.
Лабораторная работа.
Техника заражения куриных эмбрионов и культуры фибробластов
Заражение куриных эмбрионов. Проводят с диагностической целью для обнаружения и идентификации вирусов, а в биологической промышленности — для изготовления вакцин и антигенов. Берут свежие оплодотворенные инкубированные при 38 °С яйца, овоскопируют (просвечивают) их в темной комнате, чтобы выявить неоплодотворенные яйца и отличить живые эмбрионы от погибших. Неоплодотворенные яйца прозрачны. В оплодотворенных инкубированных яйцах обнаруживают движение эмбрионов и наполнение кровью сосудов хорион-аллантоисной оболочки.
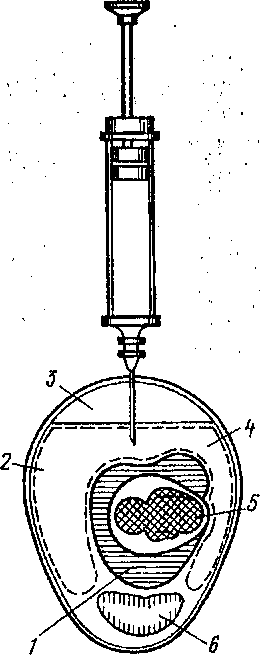
| Рис. 10. Заражение куриных эмбрионов в аллантоисную полость: 1 — желточный мешок; 2 и 4 — хорион-аллантоисная полость; 3 — воздушная камера; 5 — зародыш; 6 — белок |
Зараженные эмбрионы инкубируют при 36-37,5 °С. Сюда же ставят кювету с водой для поддержания влажности. Сроки инкубирования зависят от характера вируса. Изменения можно обнаружить уже через 48-96 ч. Эмбрионы ежедневно осматривают, овоскопируют, поворачивают каждый раз другой стороной; погибшие вскрывают или сохраняют при 4 °С.
 Вскрытие погибших эмбрионов. Скорлупу дезинфицируют спиртом и настойкой йода и срезают ножницами по границе пуги. Разрезают скорлуповую и хорион-аллантоисную оболочки; стерильной пастеровской пипеткой отсасывают в пробирку аллантоисную жидкость; содержимое яйца выливают в чашку Петри и изучают изменения. Чаще обнаруживают в хорион-аллантоисной оболочке воспалительные очаги и кровоизлияния в теле эмбриона.
Вскрытие погибших эмбрионов. Скорлупу дезинфицируют спиртом и настойкой йода и срезают ножницами по границе пуги. Разрезают скорлуповую и хорион-аллантоисную оболочки; стерильной пастеровской пипеткой отсасывают в пробирку аллантоисную жидкость; содержимое яйца выливают в чашку Петри и изучают изменения. Чаще обнаруживают в хорион-аллантоисной оболочке воспалительные очаги и кровоизлияния в теле эмбриона.
Культивирование клеток куриных фибробластов (КФ) и техника их заражения. Культуру КФ готовят на основе ферментативного гидролизата мышц (ФГМС) или на другом гидролизате. Берут 9-10-дневный куриный эмбрион, тупой конец яйца протирают спиртом и прожигают. Верхнюю часть скорлупы по окружности вскрывают ножницами и пинцетом извлекают эмбрион на чашку Петри. Голову и лапки удаляют, тушку переносят в мерный стаканчик, разрезают ножницами на кусочки 2-3 мм величиной, промывают дважды раствором Хенкса (1:20), встряхивая при этом содержимое. Надосадочную жидкость сливают. Ткань заливают в соотношении 1:10 подогретым до 35 °С раствором трипсина и переливают в коническую колбу, куда опускают простерилизованный кипячением цилиндрический магнитик (входит в комплект магнитной мешалки), и 25-30 мин перемешивают содержимое с такой скоростью, чтобы на поверхности жидкости образовывалось воронкообразное углубление. Клеточную взвесь, состоящую уже из одиночных клеток, фильтруют через марлю и разводят в 2 раза свежеприготовленной ростовой средой: 0,25%-ный раствор ФГМС на растворе Эрла — 90% и сыворотка крупного рогатого скота — 10%. Определяют концентрацию клеток в 1 мл взвеси, пользуясь камерой Горяева. Исходя из расчета, суспензию разводят ростовой средой до концентрации 700-800 тыс. клеток в 1 мл и высевают по 1 мл в пробирки с резиновыми пробками. Их размещают в наклонном положении в термостате при 37 °С. Через 24-48 ч в пробирках формируется плотный слой (монослой), состоящий из прозрачных фибробластоподобных клеток, толщиной в одну клетку.
Заражают культуру КФ суспензией патологического материала в растворе Хенкса (1:10) с добавлением пенициллина и стрептомицина по 1000 ЕД на 1 мл. Из приготовленных пробирок с культурами клеток сливают ростовую среду, вносят в них по 1 мл тканевой суспензии.. Чтобы вирус адсорбировался на клетках, пробирки ставят в термостат на 30 мин, затем исследуемый материал сливают, культуры в пробирках ополаскивают раствором Хенкса в объеме 1 мл, затем заливают таким же объемом свежей ростовой среды и вновь помещают в термостат. Просматривают культуры под микроскопом через каждые 24 ч., сравнивая с незараженными культурами. По мере необходимости меняют питательную среду на свежую. ЦПД проявляется в зависимости от характера вируса на 1-3-и сутки, иногда и в более поздние сроки.
Контрольные вопросы. 1. Чем отличаются вирусы от бактерий? 2. Как культивируют вирусы? 3. Каковы методы выделения и идентификации вирусов? 4. Что вы знаете о технике заражения куриных эмбрионов вируссодержащим материалом?






