В последние годы убедительное подтверждение получило выявление наряду с обычными («дикими») штаммами вируса мутантных вариантов. Первой была установлена мутация в зоне pre-S/S генома ВГВ, кодирующим синтез HBsAg. В результате новый штамм HBV с измененной структурой HBsAg стал недосягаемым для вакцинных анти-HBs. Как оказалось, вакцинация спровоцировала образование мутантного штамма, «убегающего» от действия вакцины.
Вторая группа мутаций связана с участком рге-С генома ВГВ, кодирующим HBeAg, что приводит к невозможности его экспрессии, хотя организм продуцирует анти-НВе. При этом образование HBcAg не нарушается, а значит, сохраняется репликация вируса. Считают, что подобные варианты HBV селекционировались в процессе естественной эволюции, в частности в процессе лечения интерфероном.
Все антигены вируса и соответствующие им антитела могут служить индикаторами различных стадий инфекционного процесса.
HBsAg является маркером, свидетельствующим об инфицировании человека ВГВ. Он обнаруживается в сыворотке крови спустя 4—6 нед. после заражения, еще в инкубационном периоде (за 25—30 дней до появления клинических признаков), а также в преджелтушном и на протяжении всего острого периода гепатита. У большинства больных он исчезает в периоде реконвалесценции, однако у отдельных пациентов HBsAg продолжает обнаруживаться в крови месяцы и даже годы после начала заболевания.
Антитела к поверхностному антигену (анти-HBs) большей частью начинают обнаруживаться в крови только в отдаленном периоде, спустя длительное время после исчезновения HBsAg. Продолжительность фазы «окна» чаще составляет 3—4 мес. Выявление анти-HBs рассматривают как один из критериев развития постинфекционного протективного иммунитета и выздоровления после острого ГВ.
HBcAg выявляется только в биоптатах печени, что ограничивает возможности внедрения этого теста диагностики в практику. Антитела к сердцевинному антигену (анти-НВс IgM) появляются при остром ГВ еще до желтухи или в первые дни разгара болезни. Они циркулируют в крови до 3—5 месяцев. Обнаружение анти-НВс IgM является для клиницистов наиболее важным подтверждением наличия у больного острого ГВ. Анти-НВс IgG обычно обнаруживаются практически в те же сроки или несколько позже, но сохраняются продолжительное время.
HBeAg появляется у больного ГВ почти одновременно с HBsAg и свидетельствует о высокой ДНК-полимеразной активности. Наличие в сыворотке крови HBeAg, ДНК HBV является показателем активной репродукции (репликации) вируса. Антитела к антигену инфекционности (анти-НВе) начинают появляться при исчезновении HBeAg. Значительное снижение HBeAg, ДНК HBV и появление анти-НВе указывают на вероятность доброкачественного течения патологического процесса. Длительная циркуляция в крови HBeAg и HBsAg, высокое содержание ДНК HBV свидетельствуют о затяжном течении инфекционного процесса и угрозе хронизации заболевания.
Эпидемиология. ГВ является одной из самых распространенных инфекций человека. По данным ВОЗ, в мире ежегодно от различных клинических форм этой инфекции умирает свыше 1 млн человек. К территориям с низкой частотой выявления HBV-инфекции относятся Северная, Западная и Центральная Европа, Северная Америка; со средней — Южная и Восточная Европа, Южная и Центральная Америка; с высокой — страны Азии и Африки.
Источником инфекции являются больные как манифестными, так и бессимптомными формами острого и хронического ГВ. Больной манифестной формой острого ГВ может быть заразен уже за 2—8 нед. до появления признаков заболевания. У большинства таких больных вирусемия прекращается с наступлением клинического выздоровления. Однако у части заразившихся возбудитель может присутствовать в крови в течение нескольких лет. Наибольшую эпидемическую опасность представляют больные бессимптомным ГВ, особенно в фазе активной вирусной репликации. Число выявляемых таких лиц ежегодно в несколько раз превышает число больных манифестным ГВ. В свою очередь, больные хроническим ГВ могут сохранять эпидемическое значение и течение всей жизни. Длительное сохранение возбудителя в организме инфицированных обеспечивает существование вируса как биологического вида.
Механизмы передачи возбудителя при ГВ — контактный и, редко, вертикальный. Выделяют естественные пути передачи ВГВ (от матери к ребенку — трансплацентарный и перинатальный; при половых контактах с инфицированным человеком — половой; при других контактах с инфицированным человеком — горизонтальный) и искусственные (при нарушении целостности кожных покровов и слизистых оболочек).
Дети, рожденные от HBsAg-позитивных матерей, оказываются инфицированными в 10% случаев. Примерно у 15% из них развивается хронический гепатит. При обнаружении у матери HBeAg вероятность перинатального инфицирования ребенка возрастает до 70—90%. При этом почти 90% из числа этих перинатально инфицированных детей впоследствии становятся больными хроническим ГВ. Необходимо отметить, что около 95% случаев перинатальной передачи происходит во время родов, и примерно 5% новорожденных заражаются ВГВ еще в утробе матери.
Общепризнана роль сексуальных контактов в распространении ГВ. Передача вируса происходит в результате контакта слизистых оболочек с семенной жидкостью, вагинальным секретом или менструальной кровью инфицированных ВГВ.
Горизонтальная передача чаще всего наблюдается среди детей, в семьях больных хроническим ГВ, в организованных коллективах при пользовани общими бритвенными приборами, зубными щетками, расческами, мочалками и пр. В перемещении вируса вследствие его высокой устойчивости во внешней среде могут участвовать также обезличенные полотенца, носовые платки, постельное белье и др. ГВ является одной из самых опасных профессиональных инфекций для работников медицинских учреждений, а также для тех служащих, которые но роду своей профессиональной деятельности имеют контакт с кровью или другими контаминированиыми биологическими жидкостями. Заболеваемость ГВ медицинских работников в 3-5 раз превышает показатели заболеваемости взрослого населения.
Реализация искусственных путей передачи чаще всего происходит при разнообразных лечебно-диагностических манипуляциях в случаях использования недостаточно очищенного от крови и плохо простерилизованного медицинского или лабораторного инструментария, приборов, аппаратов. Наиболее трудоемка стерилизация эндоскопических инструментов. Растет число лиц, инфицирующихся при внутривенном введении наркотиков.
ГВ наблюдается преимущественно в виде спорадических случаев независимо от сезонов года. Ежегодно регистрируются групповые заболевания в лечебных учреждениях. Удельный вес ГВ в структуре внутрибольничных инфекций составляет около 10%. Основной причиной заражения в лечебных учреждениях является неудовлетворительное материально-техническое обеспечение и грубые нарушения санитарно-противоэпидемического режима.
У лиц, перенесших инфекционный процесс, вырабатывается специфическая невосприимчивость к повторным заражениям.
Патогенез и патологическая анатомия. Патогенез ГВ имеет ряд принципиальных отличий. Парентеральный путь передачи возбудителя обеспечивает его гематогенный занос в печень. Вирусу не свойственно прямое повреждающее действие на гепатоциты. Их цитолиз осуществляется иммуноопосре-дованно, главным образом, за счет реакции со стороны клеточного звена иммунитета через цитотоксические Т-лимфоциты.
Установлено, что при ГВ усиливается продукция гамма-интерферона, который активизирует систему HLA. В результате происходит экспрессия молекул гистосовместимости 1-го класса в совокупности с пептидными антигенами на мембране гепатоцитов, которые распознаются нативными цитотоксическими Т-лимфоцитами. Последние пролиферируют и образуют клоны антиген-специфических киллеров, поражающих вирусинфицированные гепатоциты. В меньшей степени происходит экспрессия молекул гистосовместимости 2-го класса с последующей пролиферацией Т-хелперов 1-го типа, которые активируют бактерицидность и цитотоксичность макрофагов. Последние, в свою очередь, поглощают остатки некротизированных интралобулярных и перипортальных гепатоцитов.
Реакция со стороны гуморального звена менее значима в иммунопатогенезе и заключается в продукции специфических антител к антигенам ВГВ, их связывании с образованием иммунных комплексов и прекращении циркуляции в крови в свободном виде. Однако значимость гуморального ответа повышается при развитии аутоиммунных процессов, которые принимают участие в генезе хронического гепатита.
Иммунопатогенез ГВ схематично может быть представлен следующим образом. У взрослых заболевание протекает как с клиническими симптомами (30—40%), так и латентно (60—70%), но заканчивается, как правило, выздоровлением, что свидетельствует об адекватном иммунном ответе. Хронический гепатит развивается у 6—10% взрослых, перенесших острую инфекцию, причем либо латентно, либо в легкой форме, что связано с неполноценным иммунным ответом. Педиатры реже видят острый ГВ, так как имеется прямая корреляция между возрастом человека и наличием клинических проявлений в острой стадии болезни. У детей иммунная система еще «недостаточно зрелая» для распознавания ВГВ как «чужого» и не проявляет достаточной активности для избавления организма от возбудителя. Вот почему острый ГВ у большинства детей обычно протекает бессимптомно (90-95%), но очень часто приводит к развитию хронического «носительства» HBV (70—90%), а следовательно, и хронического гепатита (30—50%).
Таким образом, адекватному иммунному ответу, обеспечивающему купирование инфекционного процесса, соответствует острый ГВ циклического течения с полным выздоровлением. Следует заметить, что, хотя иммунному ответу и принадлежит доминирующая роль в патогенезе ГВ, не всегда конечный исход инфекционного процесса определяется состоянием иммунной системы макроорганизма. Необходимо учитывать и биологический цикл развития самого возбудителя, в частности активность вирусной репликации. Например, при высокой репликативной активности и адекватном ей иммунном ответе развивается типичный клинически манифестный острый ГВ. В свою очередь, низкая активность вирусной репликации обусловливает слабую защитную реакцию организма, что приводит к легкому или бессимптомному течению ГВ с быстрым купированием инфекционного процесса и выздоровлением. При этом относительно слабо выраженные проявления Т-клеточной цитотоксичности могут рассматриваться как адекватные.
В разгар ВГ поражение печени характеризуется цитолизом (повреждением гепатоцитов, нарушением структурно-функциональной целости мембран, разрушением органелл клетки), холестазом и мезенхимально-воспалительной реакцией (повреждением стромы и клеток ретикулогистиоцитарной системы). В основе цитолиза лежит нарушение внутриклеточных метаболических процессов, активация прооксидантных и угнетение антиоксидантных систем клеток. В результате на мембранах гепатоцитов происходит накопление свободных радикалов, усиливается перекисное окисление липидов, что приводит к повышению их проницаемости, выходу из гепатоцитов внутриклеточных ферментов (аминотрансфераз и др.), ионов калия. Последние заменяются натрием и кальцием, что ведет к задержке жидкости и набуханию клеток, изменению их рН, нарушению окислительного фосфорилирования со снижением биоэнергетического потенциала гепатоцитов. В результате нарушаются их весьма разнообразные функции, в том числе детоксицирующая, синтетическая, ухудшаются утилизация глюкозы, эстерификация холестерина, процессы переаминирова-ния и дезаминирования аминокислот. Наиболее ранним проявлением цитоли-тического синдрома является повышение активности в сыворотке крови таких внутриклеточных ферментов, как аланин-, аспартат-аминотрансфераза (АлАТ, АсАТ) и др. Клинически значимым отражением нарушения пигментного обмена, детоксицирующей и секреторной функции печени является гипербилирубинемия, обусловленная снижением процессов захвата свободного билирубина гепатоцитами, его глюкуронидирования и экскреции в желчные пути. Угнетение синтетической функции печеночных клеток приводит к гипоальбумине-мии, уменьшению практически всех факторов свертывания крови, особенно протромбина, ингибиторов коагуляции и фибринолиза. При критическом падении коагуляционного потенциала появляются кровоизлияния, а в тяжелых случаях - массивные кровотечения (геморрагический синдром).
Холестаз отражает нарушение оттока желчи, как правило, в результате снижения секреторной функции печеночных клеток (гепатоцеллюлярный холестаз), и причем в сочетании с цитолизом. В крови накапливаются не только различные фракции билирубина, но и желчные кислоты, холестерин, экскреторные ферменты (щелочная фосфатаза, гамма-глутамилтранспептидаза — ГГТП и др.) и некоторые микроэлементы, в частности медь.
Возникновение фульминантного гепатита большинство клиницистов связывает с развитием чрезмерного гуморального гипериммунного ответа, следствием чего является массивный некроз печени. При этом регенерация печеночной ткани не наступает или развивается медленно. Чрезмерный иммунный ответ может быть детерминирован иммуногенетически. Некоторые исследователи допускают, что определенную роль в генезе фульминантного течения гепатита могут иметь мутантные штаммы ВГВ (в частности, HBVe-штамм), а также ускоренный апоптоз гепатоцитов, индуцированный HBV.
В случаях тяжелого цитолитического синдрома развивается гипокалиеми-ческий алкалоз, а процесс дезинтеграции мембран распространяется на внутриклеточные органеллы. В результате нарушения целостности лизосомных мембран происходит массивный выход протеолитических ферментов-гидролаз, что ведет к саморазрушению клеток, которое может приобрести характер своеобразной цепной реакции с развитием массивного некроза печени и острой печеночной недостаточности. В этот период отмечаются изменения многих жизненно важных органов и систем (центральной нервной системы, сердца, почек, надпочечников, поджелудочной железы), проявляющиеся их полнокровием, кровоизлияниями и некрозом клеток. С развитием острой печеночной недостаточности интоксикация приобретает черты специфических нарушений функций центральной нервной системы, проявляющихся в так называемых инфекционно-токсической или печеночной энцефалопатии. В основе патогенеза поражения нервной системы при острой печеночной недостаточности лежат глубокие обменные нарушения, обусловленные, с одной стороны, выпадением антитоксической барьерной функции печени. Ряд веществ, образующихся в результате извращенного обмена, оказывают церебротоксическое действие. Определенное значение имеет повышение в крови концентрации аммиака, фенола, некоторых аминокислот. Нарастает концентрация пировиноградной и молочной кислот, низкомолекулярных жирных кислот. С другой стороны, токсическим воздействием обладают и продукты распада самой печеночной ткани. Под влиянием церебротоксических веществ происходит «дезорганизация» обмена нервных клеток, прежде всего в коре головного мозга. Извращается цикл превращений трикарбоновых кислот, следствием чего является нарушение процессов биологического окисления и энергообразования, сопровождающихся развитием внутриклеточного ацидоза. Функция центральной нервной системы при этом нарушается вплоть до развития коматозного состояния.
При благоприятном течении гепатита последней стадией патогенеза является освобождение организма от вирусов и формирование иммунитета.
Симптомы и течение. Инкубационный период продолжается от 42 до 180 дней, в среднем 60—120 дней.
Начальный (преджелтушный) период. Заболевание в 50—55% случаев начинается с признаков смешанного варианта преджелтушного периода, обычно без значительного повышения температуры тела. Симптомы интоксикации и диспепсические проявления выражены умеренно. У 30—35% больных наблюдается артралгический вариант начального периода, особенностью которого является усиление болей в крупных суставах по ночам и в утренние часы. У 10—12% больных могут появляться уртикарные высыпания на коже, сохраняющиеся 1-2 дня и сопровождающиеся эозинофилией в периферической крови. В 5—7% случаев признаки интоксикации полностью отсутствуют, а ик-теричность склер и кожи, потемнение цвета мочи могут быть первыми клиническими проявлениями заболевания. Начальный период болезни длится 7—14 дней и более, однако при заражениях, связанных с переливанием крови, он может быть короче.
Желтушный период обычно продолжается 3—4 нед. и характеризуется выраженностью и стойкостью клинических проявлений. Отмечаются более выраженная и продолжительная болезненность, а иногда и довольно резкие боли в правом подреберье. Сохраняется слабость, снижение аппетита доходит до анорексии. Нередки тошнота и даже рвота. Часто (почти в 20% случаев) отмечается зуд кожи. Печень всегда увеличена, при пальпации гладкая, с несколько уплотненной консистенцией. Как правило, отмечается увеличение селезенки. Могут быть положительными желчепузырные симптомы.
В периферической крови чаще выявляется лейкопения с лимфо- и моноци-тозом, иногда — с плазматической реакцией. СОЭ снижена до 2—4 мм/ч, в периоде реконвалесценции может ускоряться до 18—24 мм/ч с последующей нормализацией при отсутствии осложнений.
Гипербилирубинемия — более выраженная и стойкая, чем при ГА, особенно на 2—3-й неделе желтушного периода. Как правило, наблюдается достаточно манифестированное повышение активности аминотрансфераз в сыворотке крови при снижении сулемового теста и протромбинового индекса. При серологическом исследовании крови обнаруживаются HBsAg, анти-НВс IgM.
При тяжелом течении очень важны своевременное выявление и комплексная оценка признаков нарастания печеночной недостаточности и прогрессиро-вания некротических процессов в печени: усиление общей мышечной слабости, головокружение, апатия, анорексия, тошнота, учащение рвоты, появление немотивированного возбуждения, нарушения памяти; прогрессирующее увеличение желтушной окраски кожи; уменьшение размеров печени, усиление болезненности ее края; появление геморрагического синдрома (петехиальная сыпь на коже, носовые кровотечения, кровоизлияния в местах инъекций, «дегтеобразный» стул, рвота с примесью крови); появление отечно-асцитического синдрома (отеки на стопах и нижней трети голеней, асцит); возникновение лихорадки, тахикардии, нейтрофильного лейкоцитоза; увеличение содержания общего билирубина в сыворотке крови при нарастании его непрямой фракции; уменьшение содержания холестерина ниже 2,6 ммоль/л, коэффициента эстери-фикации ниже 0,2, сулемового титра менее 1,2. Особенно информативны выраженные изменения коагулограммы — удлинение времени рекальцификации и времени образования сгустка крови, снижение толерантности плазмы к гепарину, снижение протромбинового индекса ниже 50%, количества тромбоцитов - ниже 100 х 109/л.
Желтушный период ГВ характеризуется длительностью и стойкостью симптомов болезни. Нормализация активности аминотрансфераз, как правило, при легкой форме происходит к 30—35-му дню болезни, при среднетяжелой — к 40-50-му, при тяжелой форме — 60—65-му дню.
При ГВ с холестатическим синдромом на фоне интенсивного цитолиза гепа-тоцитов (высокая активность аминотрансфераз, диспротеинемия, положительная тимоловая проба, низкие цифры протромбинового индекса) в разгаре жел-
тушного периода появляются признаки холестаза (зуд кожи, выраженная гипербилирубинемия, повышение активности щелочной фосфатазы, ГГ'ГМ, увеличение в крови желчных кислот, фосфолипидов, бета-липопротеидов, холестерина). В редких случаях (как правило, у больных пожилого возраста) при ГВ развивается холестатическая форма, для которой характерен выраженный синдром холестаза при отсутствии или слабой выраженности цитолитического синдрома.
Острая пегеногная недостаточность. Усиление дистрофических и воспалительных изменений в печени могут привести к ее острому или подострому некрозу с острой печеночной недостаточностью, которая клинически выражается синдромом острой печеночной энцефалопатии (ОПЭ). Выделяют три стадии острой печеночной недостаточности: первую и вторую, относящиеся к преко-ме, третью — кому.
Первая стадия (ОПЭ-I) характеризуется относительно незначительными нарушениями психики и сознания. Нарастают астения и адинамия. Настроение неустойчивое, апатия сменяется эйфорией. Поведение больных становится неадекватным, часто агрессивным. Они бурно реагируют на болевые раздражения (в том числе и на инъекции), а затем погружаются в дремоту. Больных беспокоят чувство тоски, тревоги, головокружения даже в горизонтальном положении. Изо рта улавливается «печеночный запах». Наблюдается зевота, повторная рвота. Важным признаком прекомы I является нарастающая сонливость днем. Эти признаки выявляются на фоне усиления желтушности кожи, сокращения размеров печени, геморрагического синдрома, ухудшения лабораторных показателей.
Чрезвычайно важно у больных тяжелыми формами вирусного гепатита своевременно выявлять снижение протромбинового индекса и еще нерезко выраженные нарушения психической деятельности, которые могут быть первыми предвестниками надвигающейся энцефалопатии. Для этой цели используются такие простые тесты, как «проба письма» и «проба счета». При первом учитываются изменения почерка больного при попытке написать что-нибудь или невозможность правильно нарисовать какую-либо геометрическую фигуру (круг. звезду, квадрат и т. п.). «Пробы счета» выявляют ошибки при последовательном вычитании, например, от 300 какой-нибудь однозначной цифры (7, 8, У).
Во второй стадии (ОПЭ-П) периоды возбуждения становятся менее продолжительными и все чаще сменяются сопорозным состоянием, из которых больных еще можно вывести окриком или болевым раздражением. Сознание спутано, больной дезориентирован во времени и пространстве, глотательный и роговичный рефлексы сохранены. Появляются мышечные подергивания и характерный «хлопающий» тремор кистей, напоминающий ритмичные взмахи крыльев птицы. Брадикардия сменяется тахикардией. Нередко повышается температура тела. Нарастает кровоточивость, у некоторых больных появляются рвота «кофейной гущей», а также черный «дегтеобразный» стул. Сопорозное состояние постепенно углубляется, переходя в кому. На электроэнцефалограмме (ЭЭГ) регистрируются тета-волны на фоне замедления альфа-ритма.
Третья стадия (ОПЭ-Ш) отличается от предыдущей нарушением словесного контакта, утратой адекватной реакции на боль. Выявляются патологические рефлексы (Бабинского, клонус стопы и др.), симптомы орального автоматизма (хоботковый, Маринеску—Радовичи и др.). Дефекация и мочеиспускание становятся непроизвольными.
С углублением комы (ОПЭ-IV) наступает полная потеря реакции на все виды раздражителей, в т. ч. и на болевые. Арефлексия. Появляется симптом «плавающих глазных яблок», исчезает «хлопающий тремор». В терминальной стадии зрачки расширены и не реагируют на свет. Нарушения биохимических показателей крови и, особенно, коагулограммы весьма отчетливы, но они лишь дополняют яркую клиническую симптоматику, которая сама по себе достаточна для проведения градации ОПЭ.
Условно выделяется ранняя и поздняя печеночная кома. Ранняя развивается в первые 10—14 дней болезни, поздняя — позже 14-го дня.
При затяжных формах ГВ клинико-биохимические проявления разгара заболевания и особенно периода обратного его развития длительные — от 3 до 6 месяцев. Эти формы могут быть предстадией хронического гепатита. Установлено, что гематогенная циркуляция в стабильно высокой концентрации ДНК HBV более 3 нед., HBeAg более 1 мес, HBsAg более 3 мес, анти-НВс IgM характеризует прогредиентное течение ГВ, а, соответственно, более 5 нед., 2 и 6 мес. прогонозирует вероятность хронизации.
Диагноз и дифференциальный диагноз. ГВ подозревают в случае, если заболевшему за 45—180 дней до начала болезни переливали кровь, плазму, эритроцитарную, лейкоцитарную, тромбоцитарную взвесь, проводили оперативные вмешательства, эндоскопические исследования, многочисленные инъекции (в том числе наркотиков) или, что случается гораздо реже, если больной имел половой или тесный контакт с больным ГВ. Для клинически манифестного острого ГВ характерно постепенное начало болезни, длительный преджел- 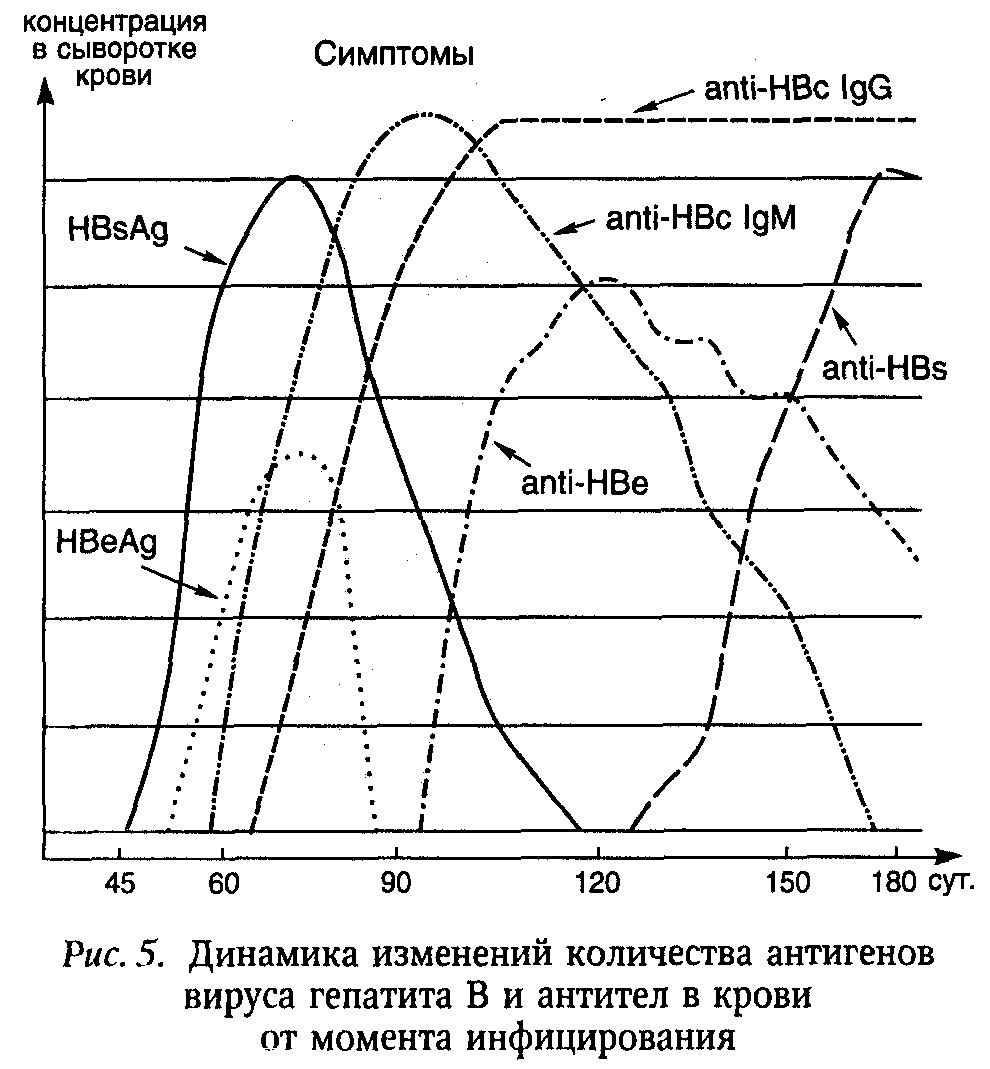 тушный период с полиартралгией и возможными аллергическими высыпаниями на коже, отсутствие улучшения самочувствия или его ухудшение с появлением желтухи, длительный желтушный период с медленным исчезновением симптомов заболевания в периоде реконвалесценции. Критерием раннего подтверждения диагноза служит обнаружение в крови HBsAg, HBeAg, анти-НВс IgM, а также ДНК HBV (рис. 5). Благоприятному циклическому течению гепатита соответствует быстрое исчезновение сначала HBeAg с появлением анти-НВе, ДНК HBV, затем и HBsAg с появлением анти-HBs. На смену ранним анти-НВс IgM появляются поздние анти-НВс IgG. Длительная циркуляция (более 3 мес.) в крови HBeAg, ДНК HBV, а также анти-НВс IgM и HBsAg в стабильно высоком титре свидетельствует о затяжном течении инфекционного процесса и высокой вероятности хронизации, О возможном развитии хронического гепатита также следует думать при выявлении HBsAg в стабильном титре на протяжении 6 мес. и более от начала заболевания даже при отсутствии маркеров активной вирусной репликации (HBeAg, анти-НВс IgM, ДНК HBV), клинической симптоматики и при нормальных биохимических показателях. В данном случае только результаты анализов пункционных биоптатов печени помогают установить правильный диагноз.
тушный период с полиартралгией и возможными аллергическими высыпаниями на коже, отсутствие улучшения самочувствия или его ухудшение с появлением желтухи, длительный желтушный период с медленным исчезновением симптомов заболевания в периоде реконвалесценции. Критерием раннего подтверждения диагноза служит обнаружение в крови HBsAg, HBeAg, анти-НВс IgM, а также ДНК HBV (рис. 5). Благоприятному циклическому течению гепатита соответствует быстрое исчезновение сначала HBeAg с появлением анти-НВе, ДНК HBV, затем и HBsAg с появлением анти-HBs. На смену ранним анти-НВс IgM появляются поздние анти-НВс IgG. Длительная циркуляция (более 3 мес.) в крови HBeAg, ДНК HBV, а также анти-НВс IgM и HBsAg в стабильно высоком титре свидетельствует о затяжном течении инфекционного процесса и высокой вероятности хронизации, О возможном развитии хронического гепатита также следует думать при выявлении HBsAg в стабильном титре на протяжении 6 мес. и более от начала заболевания даже при отсутствии маркеров активной вирусной репликации (HBeAg, анти-НВс IgM, ДНК HBV), клинической симптоматики и при нормальных биохимических показателях. В данном случае только результаты анализов пункционных биоптатов печени помогают установить правильный диагноз.
Дифференциальный диагноз проводится с теми же заболеваниями, что и при ГА. Кроме того, может возникнуть необходимость в исключении хронического ГВ. Острый процесс отличается от хронического достоверно меньшей степенью активности патологического процесса в печени и отсутствием фиброза при исследовании гепатобиоптатов, а также более частым выявлением анти-НВс IgM. Вот почему только комплексное обследование, включая биопсию печени, позволяет достоверно диагностировать данные клинические формы и адекватно назначать соответствующую терапию. При этом даже по результатам комплексного обследования больных точно установить характер течения болезни возможно приблизительно в 70% случаев. Это связано с тем, что отсутствие фиброза и выявление анти-НВс IgM не исключают наличие хронического гепатита.
Лечение. Терапевтические мероприятия такие же, как и при ГА. В случаях циклического течения ГВ назначение противовирусных средств не показано. Их целесообразно использовать при затяжном (прогредиентном) течении. На сегодняшний день в мире основным противовирусным средством для лечения ВГ является альфа-интерферон, в частности его рекомбинантные (интрон А, роферон А, реальдирон) и нативные (вэллферон, человеческий лейкоцитарный интерферон) препараты. Большинство исследователей рекомендуют назначать альфа-интерферон по 3—5 млн ME 3 раза в неделю (возможно, и через день) подкожно или внутримышечно в течение 1—3 мес. При таком способе терапии процент хронизации уменьшается приблизительно в 5 раз.
Также для этиотропного лечения могут применяться некоторые химиопрепараты, принимаемые ежедневно на протяжении 1—3 мес. К ним относятся синтетические нуклеозиды: фамцикловир (фамвир) — 750 мг/сут., ламивудин (эпивир) — 150—300 мг/сут., зидовудин (ретровир, азидотимидин, тимозид) 500—600 мг/сут., диданозин (видекс) — 300 мг/сут., зальцитабин (хивид) -2,25 мг/сут., рибавирин 1000—1200 мг/сут.; а также ингибиторы протеазы: сак-винавир (инвираза) по 600 мг 3 раза в сутки), индинавир (криксиван) по 800 мг 3 раза в сутки. Кроме того, могут быть рекомендованы индукторы интерферона: неовир (циклоферон) по 250—500 мг внутримышечно через день, амиксин по 125 мг после еды первые два дня 2 раза в сутки и далее через день; иммуномодуляторы: лейкинферон по 1 ампуле внутримышечно через день, интерлейкин-1 (беталейкин) по 15 нг/кг внутривенно капельно ежедневно в течение 5 сут., интерлейкин-2 (ронколейкин) по 0,5—2 мг внутривенно капельно через 2—3 дня, препараты тимуса (тималин, тимоген, т-активин) по 1 мл внутримышечно ежедневно в течение 5—10 дней.
В последнее время появилась группа препаратов (наиболее изучен глутоксим) нового класса веществ — тиопоэтинов, являющихся аналогами ключевого клеточного метаболита и запускающих каскадный механизм биохимических реакций регуляции метаболизма, пролиферации и дифференцировки клеток, что формирует широкий спектр иммуномодулирующих и системных цитопротекторных эффектов препаратов. Первые исследования показали высокую эффективность глутоксима в терапии острых ВГ. В частности, при прогредиентном (затяжном) течении острого ГВ с наличием активной репликации возбудителя назначение глутоксима по 1 мл парентерально ежедневно в течение 1 мес. способствовало выздоровлению в 85% случаев.
Вышеуказанные интерфероны и химиопрепараты показаны также при тяжелом течении ГВ (при наличии маркеров активной вирусной репликации) с угрозой развития острой печеночной недостаточности, особенно при появлении признаков печеночной энцефалопатии. В этих случаях суточную дозу альфа-интерферона увеличивают до 10 млн ME ежедневно. Возможно, предпочтительнее использовать химиопрепараты в связи с опасностью стимуляции интерферонами иммунопатологических процессов, лежащих в основе патогенеза острой печеночной недостаточности.
Больные с тяжелой формой ГВ в сочетании с факторами риска, осложняющими течение болезни, а также при появлении у них признаков острой печеночной недостаточности подлежат интенсивной терапии. В случаях нарушения сознания особое значение приобретают наблюдение и уход за больными, исключающие осложнения, связанные с энцефалопатией. Купирование психомоторного возбуждения осуществляется оксибутиратом натрия (20% раствор по 10—20 мл внутривенно, медленно), который можно сочетать с внутримышечным введением седуксена (0,5% раствор — 2 мл). Оксибутират нария должен применяться с осторожностью в случаях гипокалиемии и всегда сочетаться с ее коррекцией (внутривенное капельное введение препаратов калия до 6 г в сутки при отсутствии энтерального его поступления с пищей). Необходимы промывания желудка (через назогастральный зонд) и высокие или сифонные клизмы для уменьшения аутоинтоксикации. Этой же цели служит пероральное применение плоховсасывающихся антибиотиков (канамицин по 0,5 г 4 раза в сутки), энтеросорбентов. Назначают достаточное дробное энтеральное питание в сочетании с парентеральным энергообеспечением. Больным с угнетением сознания (сопор, кома) энтеральное питание проводят через назогастральный зонд. При этом можно применять обезжиренные безбелковые энпиты, детское питание.






