Содержание растворенного кислорода необходимо знать при оценке и контроле работы станций биологической очистки, оценке качества очищенных сточных вод, а также при исследовании коррозионных свойств воды.
Для определения растворенного кислород используется иодометрический метод. Он основан на реакции растворенного кислорода с гидратом закиси марганца и на иодометрическом определении образовавшихся высших по степени окисления соединений марганца.
Этим методом пользуются при содержании в воде не выше 0,1 мг / л азота нитритов и не более 10 м г/ л окисного железа. Другие окислители или восстановители должны отсутствовать.
Пробу очищенной воды отбирают в склянку вместимостью 1 л с притертой пробкой и снабженную специальной насадкой.
При удаленности места отбора проб от лабораторий пробы рекомендуется «заряжать» на месте, т. е. добавлять раствор сернокислого марганца и щелочной раствор иодида, слегка погружая концы пипеток в пробу. После этого осторожно закрывают склянку, тщательно перемешивают и отправляют в лабораторию в темном ящике.
Аппаратура.
1. Кислородные склянки вместимостью 100-300 мл с косо срезанной притертой пробкой, калиброванные с точностью до 0, 1 мл. Калибруют склянки следующим образом: на технических весах взвешивают пустую склянку с пробкой с точностью до 0,01 г, заполняют ее доверху дистиллированной водой, закрывают, следят за тем, чтобы не оставались пузырьки воздуха, осушают горлышко бумагой или полотенцем и снова взвешивают.
Склянки и вода должны приобрести до начала определения температуру комнаты (20 °С).
2. Бутылки для отбора проб вместимостью 1 л, снабженные притертыми пробками.
3. Насадка для отбора проб.
4. Пипетки для прибавления реактивов - цилиндрические пипетки без оттянутого носика.
5. Сифон.
Реактивы.
1. Сульфат марганца (II), раствор. 400 г MnSO 4 × 2 H 2 O (или 480 г Мп SO 4 × 4 Н 2 O, или 364 г MnSO 4 × H 2 O) растворяют в дистиллированной воде и доводят объем до 1 л. Фильтруют через бумажный фильтр. Если имеются сомнения о количестве кристаллизационной воды в препарате, раствор доводят до плотности 1,270г/см3при т емпературе 20 °С. Вместо сульфата марганца можно применять хлорид марганца (II) той же концентрации (425 г MnCl 2 × 4 H 2 O ч. д. а. растворяют в дистиллированной воде и доводят объем до 1 л). Реактив должен быть проверен на чистоту (содержание в нем трехвалентного железа). Для этого к порции реактива прибавляют 1 мл раствора иодида калия, 0,5 мл разбавленной серной кислоты и 1 мл раствора крахмала. Если раствор посинеет, то реактив следует очистить от железа (III), для чего на каждые 100 мл раствора прибавляют по 0,5 г карбоната натрия х. ч., дают постоять в течение суток и отфильтровывают выпавший осадок.
2. Е д кое кали с азидом, раствор. 700 г КОН (или 500 г Na ОН) растворяют в 700 мл дистиллированной воды; отдельно 10 г азида натрия растворяют в 40 мл дистиллированной воды, оба раствора смешивают и доводят до 1 л. Если раствор не прозрачен, ему дают отстояться и сливают при помощи сифона.
3. Едкое кали с иодидом и азидом натрия. Растворяют 700 г K ОН (или 500 г Na ОН) и 150 г KI в 700 мл дистиллированной воды; 10 г NaN 3растворяют в 40 мл дистиллированной воды; оба раствора смешивают и доводят до 1 л. Если раствор не прозрачен, ему дают отстояться и сливают при помощи сифона.
Проверку качества реактива (на отсутствие иодата) проводят следующим образом. Помещают в колбу, содержащую 100 мл дистиллированной воды и 10 мл разбавленной (1:4) серной кислоты, 2 мл раствора реактива, после прибавления 5 мл раствора крахмала не должна появляться синяя окраска.
4. Серная кислота, ч. д. а., разбавленная (1:4).
5. Иодид калия, 15 % - ный раствор: 15 г К I ч. д. а. растворяют в дистиллированной воде, прибавляют 1 мл 1 н. раствора N аОН и доводят до 100 мл. Отсутствие иодата проверяют, как описано выше.
6. Тиосульфат натрия,0,05 н. титрованный раствор.
12,4 г Na 2 S 2 O 3 × 5 Н 2 O ч. д. а. и 0,2 г Na 2 CO 3ч. д. а, растворяют в дистиллированной воде и доводят до 1 л. Установка титра: в колбу Эрленмейера, снабженную притертой пробкой, приливают примерно 100 мл дистиллированной воды, прибавляют 10 мл 15 %- ного раствора иодида калия, 5 мл разбавленной (1:4) серной кислоты и 20 мл 0,05 н. раствора бихромата калия. После перемешивания раствор оставляют на 5 мин в темноте и затем титруют титрованным раствором тиосульфата с 1-2 мл раствора крахмала в качестве индикатора. Титр проверяют при каждом определения. Раствор консервируют прибавлением небольшого количества хлороформа или другого консервирующего вещества.
7. Бихромат калия,0,05 н. раствор. Растворяют 2,4518 г К 2 С r 2 O 7, высушенного при 105 ° C, в дистиллированной воде и доводят объем до 1 л при 20 °С (применяют для установления титра тиосульфата).
8. Крахмал, 0,5 % - ный раствор: 5 г растворимого крахмала ч. д. а. смешивают с 50 мл дистиллированной воды и доводят раствор до 950 мл кипящей дис т иллированной водой. Раствор консервируют прибавлением небольшого количества (1,25 г на 1 л) салициловой кислоты.
Ход определения.
В кислородную склянку, заполненную доверху пробой, добавляют 2 мл раствора сульфата марганца. Для этого наполненную пипетку погружают до самого дна кислородной склянки, затем открывают верхний конец и пипетку медленно вынимают. Другой пипеткой прибавляют к пробе 2 мл раствора едкого кали с азидом. Кончик пипетки опускают только под уровень пробы в горлышке кислородной склянки.
Склянку осторожно закрывают так, чтобы под пробкой не образовались пузырьки воздуха. Горлышко ополаскивают водой и содержимое хорошо перемешивают (переворачиванием склянки) до образования хлопьевидного осадка.
О садку дают собраться на дне склянки. Прозрачный раствор над осадком можно слить сифоном или же присоединить сифон к водоструйному насосу и отсосать. Отсасывание должно продолжаться 15-20 сек (более быстрое отсасывание может увлечь осадок). Сразу после отсасывания или сифонирования прозрачной жидкости над осадком в кислородную склянку по стенке приливают 5 мл разбавленной (1:4) серной кислоты и перемешивают. Затем прибавляют 2 мл раствора иодида калия и содержимое вновь перемешивают.
По истечении 5 мин выделившийся иод титруют непосредственно в кислородной склянке титрованным раствором 0,05 н. тиосульфата до светло - желтой окраски. Затем прибавляют раствор крахмала и продолжают титровать до обесцвечивания. Индикатор обычно прибавляют в количестве 1-2 мл в зависимости от качества применяемого крахмала.
Определение можно вести и следующим приемом. В кислородную склянку, заполненную доверху пробой, приливают, как указывалось выше, 2 мл раствора сульфата марганца и 2 мл раствора едкого кали с иодидом калия и азидом. После выпадения осадка гидроокисей марганца кислородную склянку открывают и пипеткой с широким концом, опущенным под уровень пробы, добавляют 1 мл серной кислоты (плотностью 1,84 г / см 3) или 5 мл разбавленной (1:4) серной кислоты. Кислородную склянку вновь закрывают и перевертыванием перемешивают ее содержимое. Затем содержимое кислородной склянки переливают в колбу для титрования, склянку ополаскивают дистиллированной водой, сливая ее в ту же колбу. Выделившийся иод титруют раствором тиосульфата, как указывалось выше.
Если в анализируемой воде содержатся нитриты более 0,1 мг / л, то используют следующий прием.
В кислородную склянку, заполненную доверху пробой, добавляют 2 мл раствора сульфата марганца и 2 мл КОН, содержащего иодид и азид. Склянку закрывают пробкой и перемешивают до образования хорошо выпадающего осадка. Осадку дают отстояться и затем жидкость над осадком сливают при помощи сифона, а к осадку добавляют 5 мл разбавленной (1:4) серной кислоты. Раствор переливают в колбу, склянку ополаскивают три раза небольшими порциями дистиллированной воды и затем в колбу добавляют 0,3 мл раствора (40 % - ного) сульфаминовой кислоты или 0,3 мл 40 %- ного раствора мочевины и после этого 2 мл 15 %- ного раствора К I. Через 5 мин в присутствии крахмала проводится титрование 0,05 н. раствором тиосульфата.
Расчет.
Содержание растворенного кислорода (в мг / л) вычисляют по формуле
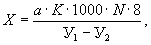 (9.23)
(9.23)
а - объем раствора тиосульфата натрия, израсходованного на титрование, в мл;
К - поправочный коэффициент к нормальности титрованного раствора тиосульфата натрия;
N - нормальность раствора тиосульфата натрия;
У 1- вместимость кислородной склянки, в мл;
У 2- общий объем реактивов, прибавленных в кислородную склянку при фиксации кислорода, а в некоторых случаях и при предварительной подготовке пробы, в мл;
8 - грамм - эквивалент кислорода.
Насыщение растворенным кислородом (в %) вычисляют по формуле:
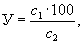 (9.24)
(9.24)
где с1 - найденная концентрация кислорода (в мг / л);
с 2- равновесная концентрация кислорода (в мг / л), найденная по табл. 9.4 для температуры воды, измеренной при отборе пробы, с возможной поправкой на атмосферное давление и на содержание растворенных солей.
Результаты округляются до 0,1 мг или до целых процентов. Приведенные равновесные концентрации кислорода даны для атмосферного давления 760 мм рт. ст. Для других атмосферных давлений равновесные концентрации вычисляются по формуле:
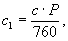 (9.25)
(9.25)
где с1 - искомая величина равновесной концентрации кислорода (в мг / л) при давлении Р;
с - равновесная концентрация кислорода, найденная по табл. 9. 4;
Р - атмосферное давление в мм рт. ст.
Таблица 9.4






