Переход из одного состояния вещества в другое называется фазовым переходом. Испарение и конденсация являются примерами фазовых переходов.
Все реальные газы (кислород, азот, водород и т. п.) при определенных условиях способны превращаться в жидкости. Однако такое превращение может происходить только при температурах ниже определенной, так называемой критической температуры T кр. Например, для воды критическая температура равна 647,3 K, для азота 126 K, для кислорода 154,3 K. При комнатной температуре (≈ 300 K) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов.
Испарением называется фазовый переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости (если нет подвода энергии от окружающих тел).
Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т. е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Число молекул, вылетающих с единицы площади поверхности жидкости за одну секунду, зависит от температуры жидкости. Число молекул, возвращающихся из пара в жидкость, зависит от концентрации молекул пара и от средней скорости их теплового движения, которая определяется температурой пара. Отсюда следует, что для данного вещества концентрация молекул пара при равновесии жидкости и ее пара определяется их равновесной температурой. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p 0данного вещества зависит только от его температуры и не зависит от объема. Поэтому изотермы реальных газов на плоскости (p, V) содержат горизонтальные участки, соответствующие двухфазной системе.
При повышении температуры давление насыщенного пара и его плотность возрастают, а плотность жидкости уменьшается из-за теплового расширения. При температуре, равной критической температуре T кр для данного вещества, плотности пара и жидкости становятся одинаковыми. При T > T кр исчезают физические различия между жидкостью и ее насыщенным паром.
№31. Второе начало термодинамики
Второе начало термодинамики — физический принцип, накладывающий ограничение на направление процессов передачи тепла между телами.
Формулировки:
1.невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому
2.невозможно превратить теплоту в работу, не производя никакого другого действия
3.вечный двигатель второго рода невозможен
Оно было создано на основе обобщения опытных фактов и получило многочисленные экспериментальные подтверждения.
2 начало ТД можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
№32. Прямой и обратный циклы Карно
Цикл Карно — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов. Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропия адиабатически изолированной (без теплообмена с окружающей средой) системы не меняется.
Пусть тепловая машина состоит из нагревателя с температурой TH, холодильника с температурой TX и рабочего тела. Цикл Карно состоит из четырёх стадий:
- Изотермическое расширение. В начале процесса рабочее тело имеет температуру TH, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты QH. При этом объём рабочего тела увеличивается.
- Адиабатическое (изоэнтропическое) расширение. Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника.
- Изотермическое сжатие. Рабочее тело, имеющее к тому времени температуру TX, приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты QX.
- Адиабатическое (изоэнтропическое) сжатие. Рабочее тело отсоединяется от холодильника и сжимается без теплообмена с окружающей средой. При этом его температура увеличивается до температуры нагревателя.
При изотермических процессах температура остаётся постоянной, при адиабатических отсутствует теплообмен, а значит, сохраняется энтропия:
 при δQ = 0
при δQ = 0
№33. Теорема Клаузиуса. Понятие об энтропии.
Теорема Клаузиуса: Энтропия замкнутой системы стремится к максимуму.
Энтропия (S) – термодинамическая функция состояния, которая служит мерой беспорядка (неупорядоченности) системы. Возможность протекания эндотермических процессов обусловлена изменением энтропии, ибо в изолированных системах энтропия самопроизвольно протекающего процесса увеличивается ΔS > 0 (второй закон термодинамики).
Энтропия есть параметр состояния, характеризующий свойства макроскопической системы в условиях равновесия. Энтропия системы может изменяться, но переходить из тела в тело она не в состоянии. Переходит только теплота. Таким образом, энтропия приобретает смысл удобного расчетного параметра, который получается, если количество тепла разделить на температуру.
Формула для нахождения энтропии:
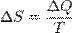
№34. Основное уравнение термодинамики.
1. Основное ур-ние ТД (для равновесных процессов)
dE = TdS – PdV
2. для необратимых процессов - основное термодинамическое неравенство
TdS=TdE + PdV
Основное уравнение термодинамики позволяет ввести характеристические функции (термодинамические потенциалы), изменение которых при изменении состояния системы является полным дифференциалом, т.е. не зависит от способа (пути) перехода от одного состояния к другому.
№35. Изменение энтропии в адиабатных процессах, при теплообмене и расширении газа в пустоту.
Адиабатический процесс – процесс, при котором система не обменивается энергией.
Согласно второму началу термодинамики, при обратимом адиабатическом процессе энтропия постоянна, dS=dQ/T=0, а при необратимом - возрастает. Адиабатический процесс называют изоэнтропийным процессом, т.к.  .
.
Если расширению в пустоту подвергнуть неидеальный газ, температура такого (реального) газа при расширении уменьшается. Дело в том, что в реальных газах заметную роль играет притяжение между молекулами и связанная с этим притяжением потенциальная энергия взаимодействия между молекулами газа. При расширении среднее расстояние между молекулами увеличивается, силы притяжения совершают отрицательную работу, я потенциальная энергия увеличивается. А поскольку полная внутренняя энергия остается постоянной, кинетическая энергия молекул, а значит, и температура газа, уменьшаются.
№36. Свойства энтропии
Энтропия есть параметр состояния, характеризующий свойства макроскопической системы в условиях равновесия. Энтропия системы может изменяться, но переходить из тела в тело она не в состоянии. Переходит только теплота. Таким образом, энтропия приобретает смысл удобного расчетного параметра, который получается, если количество тепла разделить на температуру. Энтропия- величина аддитивная: энтропия макросистемы равна сумме энтропий ее отдельных частей. Одно из важнейших свойств энтропии заключается в том, что энтропия замкнутой (т.е. теплоизолированной) макросистемы не уменьшается - она либо возрастает, либо остается постоянной. Если же система не замкнута, то ее энтропия может как увеличиваться, так и уменьшаться.






