Как было показано в разделе термодинамики, теплоёмкость при постоянном объёме определяется формулой
 . (3.27)
. (3.27)
Используя выражение (3.26) для внутренней энергии одного моля идеального газа получим следующее выражение для молярной теплоёмкости при постоянном объёме.
 . (3.28)
. (3.28)
Из уравнения Майера следует, что молярная теплоёмкость при постоянном давлении равна
 . (3.29)
. (3.29)
С помощью формул (3.28) и (3.29) можно получить следующее выражение для адиабатической постоянной g
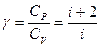 . (3.30)
. (3.30)
Сравнение классической теории теплоёмкости с опытными данными показывают, что при определённых условиях теплоёмкости, вычисленные по формулам (3.29) и (3.30) близки к экспериментальным результатам. Для атомарного газа i=3,  ,
, 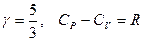 . Для сравнения в таблице №1 приведен экспериментальный результат для различных газов.
. Для сравнения в таблице №1 приведен экспериментальный результат для различных газов.
| Газ | 
| 
| 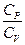
|
| Гелий | 1,519 | 1,001 | 1,659 |
| Неон | - | - | 1,64 |
| Аргон | 1,5 | 1,008 | 1,67 |
| Криптон | - | - | 1,68 |
| Ксенон | - | - | 1,66 |
 Из таблицы следует, что теория достаточно точно определяет теплоёмкость идеального газа.
Из таблицы следует, что теория достаточно точно определяет теплоёмкость идеального газа.
Из классической теории теплоёмкости (3.28) и (3.29) следует, что теплоёмкость идеального газа является постоянной величиной, не зависящей от температуры. В действительности, как показывает опыт, теплоёмкость газа зависит от температуры. На рисунке приведён график зависимости молярной теплоёмкости газообразного водорода от температуры. Как видим из рисунка, теплоёмкость CV газообразного водорода совпадает со значением 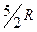 , вытекающим из классической теории только в области температур T3-T4. В области температур T1-T2 теплоёмкость газообразного водорода принимает значение
, вытекающим из классической теории только в области температур T3-T4. В области температур T1-T2 теплоёмкость газообразного водорода принимает значение 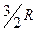 , свойственное теплоёмкости атомарного газа. Это говорит о том, что классическая теория теплоёмкости справедлива только в ограниченной области температур. По-видимому, это связано с тем, что эффективный вклад в теплоёмкость вносит не все, а только некоторые степени свободы. При понижении температуры некоторые степени свободы становятся малоэффективными, их вклад исчезает. Про такие степени свободы говорят, что они «заморожены». Наоборот, при повышении температуры начинает проявляться всё новые степени свободы, которые ранее были либо малоэффективны, либо совсем заморожены. Это значит, что классический закон равномерного распределения энергии по степеням свободы не справедлив и требует уточнения.
, свойственное теплоёмкости атомарного газа. Это говорит о том, что классическая теория теплоёмкости справедлива только в ограниченной области температур. По-видимому, это связано с тем, что эффективный вклад в теплоёмкость вносит не все, а только некоторые степени свободы. При понижении температуры некоторые степени свободы становятся малоэффективными, их вклад исчезает. Про такие степени свободы говорят, что они «заморожены». Наоборот, при повышении температуры начинает проявляться всё новые степени свободы, которые ранее были либо малоэффективны, либо совсем заморожены. Это значит, что классический закон равномерного распределения энергии по степеням свободы не справедлив и требует уточнения.
Эти трудности были преодолены после того, как теория теплоёмкости была построена на основе квантовой теории. Согласно квантовой теории, в отличие от классической, внутренняя энергия атомных систем может принимать лишь дискретные значения. Двухатомную молекулу, когда речь идёт о малых колебаниях её атомов относительно друг друга, можно рассматривать как гармонический осциллятор. Согласно квантовой теории возможные значения колебательной энергии такой системы представляются формулой
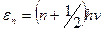 ,
,
где n – частота осциллятора, n – целое число, которое может принять значения 0,1,2,3,…, h - универсальная постоянная, называемая постоянной Планка.
Таким образом, энергетический спектр гармонического осциллятора состоит из бесконечного множества равностоящих уровней. Расстояние между соседними уровнями равно hn. Самому низкому уровню соответствует энергия  . Воздействуя на осциллятор его можно возбудить, т.е. перевести на один из возможных более высоких уровней энергии. Ближайшим является энергетический уровень с n=1 и энергией
. Воздействуя на осциллятор его можно возбудить, т.е. перевести на один из возможных более высоких уровней энергии. Ближайшим является энергетический уровень с n=1 и энергией  .
.
Пусть имеем газ, состоящий из двухатомных молекул, т. е. из гармонических осцилляторов. Предположим, что температура газа настолько низка, что kБТ£hn. Тогда средняя энергия теплового движения молекул будет порядка kБТ и такая энергия недостаточна, чтобы возбудить осциллятор, т.е. перевести его с нулевого уровня на ближайший первый уровень. Возбуждение может происходить только при столкновениях с молекулами, энергия которых равно или больше порции энергии hn. Однако таких молекул относительно мало, так что практически все молекулы останутся на нижнем энергетическом уровне. Моделью жёсткой двухатомной молекулы в теории теплоёмкости можно пользоваться лишь при соблюдении условия kБТ<hn. При повышении температуры, когда величина kБТ становиться сравнимой с hn начинает возбуждаться первый, а затем более высокий колебательные уровни двухатомной молекулы.
Совершенно аналогично влияет на теплоёмкость газов и вращение молекул. Энергия вращения также принимает дискретные значения. Её возможные значения по квантовой механике определяется формулой
 ,
,
где I –момент инерции молекулы, l – целое число, которое может принимать значения 0,1,2,3 …. Расстояния между уровнями энергии не постоянны, а возрастают в арифметической прогрессии. В состоянии с наименьшей энергией при l=0 вращения не возбуждены. В состоянии с l =1 энергия вращения равна
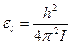 .
.
Если kБТ <e1, то средней тепловой энергии молекулы недостаточно для возбуждения вращений. В этом случае при вычислении теплоемкости вращение молекул можно не учитывать. В противоположном случае, когда  >>e1, возбуждается много вращательных уровней и необходимо учитывать вращение молекул.
>>e1, возбуждается много вращательных уровней и необходимо учитывать вращение молекул.
На основе приведённых данных объясним ход графика, приведённого на рисунке.
В области T1-T2 тепловая энергия молекул kБT намного меньше 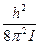 , соответственно и kБT <hn, в результате чего и вращательные и колебательные степени свободы заморожены. Теплоёмкость водорода в этой области температур равна
, соответственно и kБT <hn, в результате чего и вращательные и колебательные степени свободы заморожены. Теплоёмкость водорода в этой области температур равна 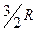 , которая совпадает с теплоёмкостью атомарного газа, в котором атомы совершают только поступательные движения. В области температур T2-T3 теплоёмкость газа возрастает, это связано с тем, что у некоторых молекул начинает возбуждаться вращательные степени свободы, причём, чем выше температура, тем больше таких молекул. При температуре T3 оказывается возбуждёнными вращательные степени свободы всех молекул и теплоёмкость газа становиться равной
, которая совпадает с теплоёмкостью атомарного газа, в котором атомы совершают только поступательные движения. В области температур T2-T3 теплоёмкость газа возрастает, это связано с тем, что у некоторых молекул начинает возбуждаться вращательные степени свободы, причём, чем выше температура, тем больше таких молекул. При температуре T3 оказывается возбуждёнными вращательные степени свободы всех молекул и теплоёмкость газа становиться равной  , что совпадает с классическим значением теплоёмкости двухатомного газа. При дальнейшем увеличении температуры с T4, и выше теплоёмкость водорода начинает расти. Это объясняется тем, что в этой области температур, тепловая энергия молекул становиться достаточной для возбуждения колебательных степеней свободы.
, что совпадает с классическим значением теплоёмкости двухатомного газа. При дальнейшем увеличении температуры с T4, и выше теплоёмкость водорода начинает расти. Это объясняется тем, что в этой области температур, тепловая энергия молекул становиться достаточной для возбуждения колебательных степеней свободы.
Барометрическая формула
Хаотические молекулярные движения приводят к тому, что молекулы газа равномерно распределяются по объёму сосуда, что концентрация частиц во всех частях сосуда становится одинаковой. В равновесном состоянии давление и температура газа также одинакова во всём объёме. Но это возможно только тогда, когда на молекулы не действуют внешние силы. При наличии таких сил, молекулярные движения приводят к особому поведению газов. Рассмотрим газ, находящийся в поле силы тяжести. Если бы отсутствовало тепловое движение молекул, то все молекулы под действием силы тяжести упали бы на поверхность земли, и весь воздух собрался бы тончайшем слое. Если бы отсутствовала сила тяжести, но существовало бы молекулярное движение, молекулы разлетелись бы по всему мировому пространству. Одновременное наличие силы тяжести и теплового движения молекул воздуха приводит к образованию воздушного слоя вокруг земли – атмосферы. При этом в атмосфере устанавливается вполне определённое распределение молекул по высоте. В соответствии с этим устанавливается и определённый закон изменения давления газа с высотой. Определим закон распределения давления с высотой.
 Рассмотрим вертикальный столб воздуха (рис.4). Пусть у поверхности земли, где h=0, давление равно P0, а на высоте h равно P.
Рассмотрим вертикальный столб воздуха (рис.4). Пусть у поверхности земли, где h=0, давление равно P0, а на высоте h равно P.
Так как давление определяется весом вертикального столба воздуха, находящиеся под площадкой 1м2 на этой высоте, с увеличением высоты на dh, давление уменьшится на величину dP, причём dP будет определяться весом столба воздуха высотой dh и площадью основания 1м2:
 , (3.31)
, (3.31)
где r - плотность воздуха, g – ускорение свободного падения. Знак (-) показывает, что с ростом высоты давление уменьшается. Учитывая, что
r=mn,
где m – масса молекулы газа, n – концентрация, а из кинетической теории n=P/kБT, (3.31) перепишем в виде
 . (3.32)
. (3.32)
Получили дифференциальное уравнение, описывающее изменение давление с высотой.
В дальнейшем сделаем допущение, что температура и ускорение свободного падения не зависит от высоты, что, вообще говоря, неверно. Разделив в (3.32) переменные, получим
 .
.
Интегрируя обе стороны данного уравнения, имеем
 , (3.33)
, (3.33)
где c – постоянная интегрирования.
Потенцирование выражения (3.33) даёт
 . (3.34)
. (3.34)
Постоянную с определим из условия, что при h=0, P=P0. Поставив в уравнение (3.34) эти значения h и P, получим
с=P0.
Таким образом, зависимость давления от высоты над поверхностью земли определяется следующим выражением
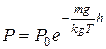 . (3.35)
. (3.35)
Учитывая, что m=m/NA, R=kБNA, имеем
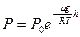 . (3.36)
. (3.36)
Уравнение (3.35) и (3.36) называются барометрическими формулами. Из этого уравнения видно, что давление газа убывает с высотой по экспоненциальному закону. Этим законом пользуются для определения высоты над землёй путём измерения давления на данной высоте. Приборы, служащие для измерения высоты горных вершин, высоту полёта самолёта представляют собой специальные барометры, шкала которых проградуирована в метрах.
Так как давление газа P=n kБT, то из формулы (3.36) можно получить следующий закон убывания концентрации с высотой
 , (3.37)
, (3.37)
где n и n0 – концентрация молекул в точках, между которыми разность высот равна h.
Закон Больцмана
Формула (3.37) является барометрической формулой, которая относиться к случаю, когда газ находиться над действием силы тяжести. Величины mgh в (3.37) представляет потенциальную энергию молекулы на высоте h. Можно поэтому сказать, что формула (3.35) даёт число частиц n, энергия которых U=mgh, если число частиц с энергией, равной нулю, равно n0. Очевидно, поведение газа существенно не измениться, если вместо силы тяжести на него будет действовать какая – либо другая сила, а выражение для энергии будет иметь другой вид.
Если газ находиться в каком-нибудь силовом поле, так что частица обладает потенциальной энергией U, то число частиц с такой энергией определится формулой
 . (3.38)
. (3.38)
Формула (3.38) называется формулой Больцмана. Она позволяет определить долю частиц, которые в условиях теплового равновесия обладают энергией U.

Из формулы (3.38) видно, что доля  частиц с данной энергией U кроме величины этой энергии, зависит только от температуры.
частиц с данной энергией U кроме величины этой энергии, зависит только от температуры.
При данной температуре, доля молекул обладающих той и иной энергией U, зависит от значения U и быстро уменьшается с ростом U. Это означает доля молекул, обладающих большой энергией всегда очень мала.






