Непредельные галогенпроизводные делятся на 3 типа:
1) галогенпроизводные винилового типа: атом углрода находится у непредельного атома углерода.
СН2=СНСl хлористый винил
СН2=ССl2 хлористый винилиден
2) галогенпроизводные аллильного типа:
СН2=СН-СН2-Сl хлористый аллил
СН3-СН=СН-СН2Сl хлористый кротил
3) галогенпроизводные с изолированным расположением двойной связи и галогена:
СН2=СН-СН2-СН2-Сl 4-хлор-1-бутен
АРОМАТИЧЕСКИЕ ГАЛОГЕНПРОИЗВОДНЫЕ
Делятся на две группы:
1. Соединения, содержащие галоген в боковой цепи:

2. Соединения, содержащие галоген в ароматическом ядре:
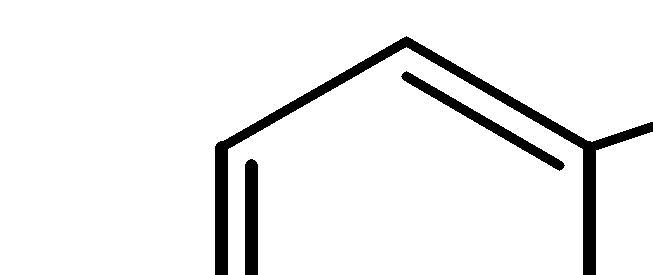
Способы получения ароматических галогенпроизводных с галогеном в ядре
Галогенирование
Хлор- и бромпроизводные бензола получают реакцией галогенирования в присутствии кислот Льюиса (электрофильное ароматическое замещение SE, см. ч.1, лекция №10)

Иодпроизводные получить таким образом невозможно, так как реакция обратима. Реакцию обычно проводят в присутствии окислителя.
Присутствие окислителя (например, HNO3) необходимо, т.к. он окисляет НI до иодноватистой кислоты и способствует протеканию реакции в прямом направлении.

2. Из солей диазония.

Способы получения ароматических галогенпроизводных с галогеном в боковой цепи
Для получения таких соединений пригодны все методы получения алкилгалогенидов.
Прямое галогенирование
Наиболее распространенным является способ прямого галогенирования. Реакция протекает по радикальному механизму:

Можно ввести второй и третий атомы галогена. При этом образуются ди- и тризамещенные производные:

Хлорметилирование
Реакция хлорметилирования в присутствии кислот Льюиса (AlCl3, ZnCl2) - электрофильное замещение.

Параформ - полимер формальдегида, при пропускании HCl деполимеризуется, образуя хлорметильный катион +СН2Сl, реагирующий с ароматическим кольцом.
Практически хлорметилирование целесообразнее, чем алкилирование, с последующим галогенированием, так как при хлорметилировании образуется один продукт, а галогенирование алкилпроизводных бензола дает смесь галогенидов
Замещение
1) Реакции нуклеофильного замещения, характерные для алкилгалогенидов, нехарактерны для арилгалогенидов.
Инертность галогенпроизводных в реакциях нуклеофильного замещения объясняется наличием сопряжения неподеленных электронных пар галогена с π-сопряженной системой бензольного кольца, что приводит к уменьшению частичного положительного заряда атоме углерода бензольного кольца

Реакции нуклеофильного замещения протекают в более жестких условиях
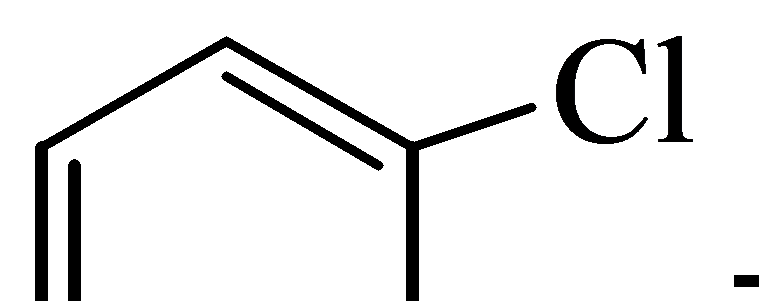
Предполагают, что реакция в этом случае протекает через стадию дегидрирования с образованием дегидробензола и последующим присоединением
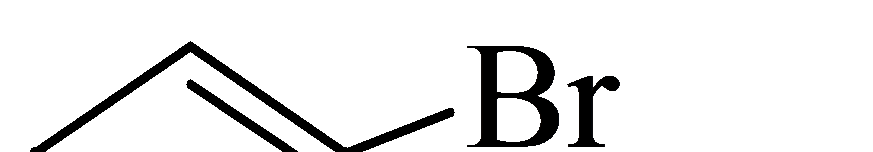
Способность к реакциям нуклеофильного замещения возрастает, если в орто- и пара- положениях к галогену находится сильная электроноакцепторная группа. Это обусловлено тем, что на атоме С, связанным с атомом галогена, увеличивается положительный заряд, и атом углерода легко взаимодействует с нуклеофильными агентами с вытеснением атома галогена:

2) Галоген в ядре дезактивирует бензольное кольцо в реакциях электрофильного замещения и направляет электрофильный агент в орто- и пара-положения.

3) Арилгалогениды легко образуют реактив Гриньяра:

Фенилмагнийбромид - очень реакционноспособное вещество. Группа MgBr легко замещается на другие группировки.
4) Легко получаются и литийпроизводные бензола:
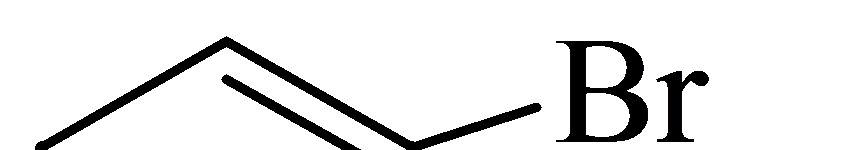
Ариновый механизм замещения:
SN1
При действии сильных нуклеофильных реагентов на галогенарилы сначала отщепляется HHal с образованием очень реакционноспособного, неустойчивого продукта дегидробензола
Скорость отщепления падает в ряду I>Br>Cl>F
SN2
При введении в бензольное кольцо электроноакцепторных групп в орто- и пара- положения приводит к подвижности галогена и лёгкости нуклеофильного замещения. Электроноакцепторные группы приводят к устойчивости сигма-комплекса в отличие от электронодонорных групп






