ѕол€рографический метод качественного и количественного анализа электрохимически активных веществ основан на процессах их окислени€ или восстановлени€, протекающих при пол€ризации рабочего микроэлектрода под действием приложенного напр€жени€. ѕри этом конкретную аналитическую информацию получают при интерпретации пол€ризационных кривых (пол€рограмм), выражающих зависимость силы тока от приложенного посто€нного (по форме) напр€жени€ Ц I = f (E).
”читыва€, что интенсивность пол€ризации электрода возрастает при увеличении плотности тока (отношени€ силы тока к площади поверхности электрода), поверхность рабочего микроэлектрода делают очень маленькой, а поверхность электрода сравнени€ Ц наоборот, достаточно большой, чтобы исключить (или свести к минимуму) его пол€ризацию. ¬ отличие от гальванического элемента, где электрохимическа€ реакци€ протекает самопроизвольно, в пол€рографической (электролитической) €чейке идет обратный процесс Ц электролиз, когда в электролитической €чейке под действием приложенного напр€жени€ на рабочем электроде протекает направленна€ электрохимическа€ реакци€. ѕри этом на пол€ризуемом катоде восстанавливаютс€ вещества-окислители (в том числе и катионы металлов), а на пол€ризуемом аноде Ц окисл€ютс€ вещества, обладающие восстановительными свойствами.
Ёлектроды, примен€емые в пол€рографии
¬ пол€рографии обычно используют электролитическую €чейку с двум€ электродами: рабочим микроэлектродом и электродом сравнени€ с посто€нным значением электродного потенциала. »ногда дл€ стабилизации потенциала электрода сравнени€ примен€ют третий вспомогательный электрод дл€ отвода по нему тока от рабочего электрода. ¬ыбор материала рабочего электрода зависит от типа электрохимической реакции и от природы определ€емого вещества. Ќапример, при восстановлении ионов электроотрицательных металлов (Zn2+, Cd2+, Pb2+ и др.) и многих органических веществ используют ртутный капающий катод, у которого потенциал разложени€ воды с выделением водорода и кислорода составл€ет Ц1.1 ¬. Ќа платиновом вращающемс€ электроде можно проводить восстановление ионов электроположительных металлов (Cu2+, Ag+) и таких сильных окислителей, как KMnO4, K2Cr2O7. Ќа платиновом аноде можно окисл€ть Fe(II) и различные органические соединени€, обладающие восстановительными свойствами. ƒл€ определени€ Fe(III) и Cu(II) используют также графитовые и стеклоуглеродные электроды.
ƒл€ ориентировочной оценки целесообразности применени€ того или иного рабочего электрода можно пользоватьс€ стандартными потенциалами электродных полуреакций. Ќапример,
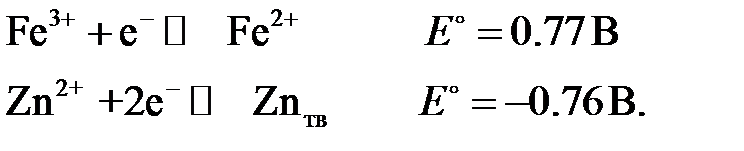
| + E, B |
| Ц E, B |
| Ia |
| Iк |
| 1.0 |
| 1.0 |
| ≠H2 |
| ≠H2 |
| ≠H2 |
| ≠O2 |
| ≠O2 |
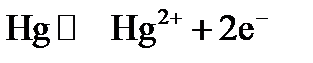
|
| ≠O2 |
–исунок 4.6 Ц ¬ольтамперные кривые процессов выделени€ водорода (катодна€ область) и кислорода (анодна€ область) на платиновом (1), графитовом (2) и ртутном (3) электродах (фоновый раствор Ц 0.2 ћ H2SO4)
|
|
|
Ѕолее строго, необходимо учитывать вли€ние фонового раствора в электролитической €чейке. »з представленных на рис. 4.6 вольтамперных кривых видно, что ртутный электрод пригоден дл€ электрохимических реакций, протекающих при отрицательных значени€х потенциала, а платиновый и графитовый электроды Ц дл€ реакций, протекающих в положительной области потенциала.
ќсновным критерием выбора электрода сравнени€ €вл€етс€ его мала€ пол€ризуемость, т.е. посто€нство потенциала при наложении напр€жени€ на пол€рографическую €чейку, что обеспечиваетс€ большой поверхностью электрода. ¬ыбор электрода сравнени€ зависит от состава раствора в €чейке. „аще других используют насыщенный каломельный и хлоридсеребр€ный электроды. ¬ качестве вспомогательных электродов используют электроды из благородных металлов, анодную (донную) ртуть и др.
ѕол€ризационные кривые
ѕол€ризационна€ крива€, выражающа€ зависимость силы тока от приложенного к €чейке напр€жени€ I = f (E), отражает электрохимический процесс, происход€щий только на рабочем микроэлектроде, так как всЄ накладываемое на €чейку напр€жение расходуетс€ на изменение потенциала только рабочего электрода (потенциал непол€ризуемого электрода сравнени€ остаетс€ неизменным). ѕри увеличении накладываемого напр€жени€ потенциал пол€ризуемого микроэлектрода будет все более возрастать, принима€ все более положительные значени€ дл€ анода (≈ = ≈а) и все более отрицательные Ц дл€ катода (≈ =Ц ≈к). ѕри пол€ризации микроэлектрода в отсутствии электроактивных веществ величина тока не зависит от изменени€ накладываемого напр€жени€ (идеально пол€ризуемый электрод). ¬заимодействие электроактивных веществ (называемых депол€ризаторами) с рабочим микроэлектродом подавл€ет его пол€ризацию и зависимость I = f (E) становитс€ волнообразной (рис. 4.7).
ѕри использовании стационарных (неподвижных) электродов дл€ устранени€ конвективного и миграционного переноса электроактивного вещества электролиз (пол€рографирование) провод€т в неперемешиваемом растворе в присутствии большого избытка (0.1 Ц 1.0 моль×лЦ1) индифферентного фонового электролита (пол€рографического фона), потенциал восстановлени€ или окислени€ которого находитс€ вне области используемых потенциалов анализируемого электроактивного вещества. ѕри этих услови€х единственным способом переноса электроактивного вещества из объема €чейки в приэлектродный слой €вл€етс€ диффузи€, а возникающий ток называют диффузионным.
| A |
| ¬ |
| — |
| D |
| h |
| h 1/2 |
| E 1/2 |
| E |
| I |
–исунок 4.7 Ц ѕол€ризационна€ крива€ (пол€рограмма)
| E, ¬ |
| I, мкј |
–исунок 4.8 Ц ѕол€рограмма обратимо (1) и необратимо (2) восстанавливающегос€ вещества-депол€ризатора
Ќа классической пол€рограмме, полученной с использованием ртутного капающего электрода (катод) (рис. 4.7) с увеличением накладываемого напр€жени€ наблюдаетс€ три характерных участка.
ј¬ Ц нижн€€ ветвь кривой, где наблюдаетс€ небольшой рост тока, обусловленный, в основном, током зар€жени€ двойного электрического сло€, реакци€ на электроде отсутствует. ѕри достижении потенциала восстановлени€ (или окислени€) электроактивного вещества в точке ¬ начинаетс€ процесс электролиза, т.е. рабочий микроэлектрод депол€ризуетс€ вследствие протекани€ на нем электрохимической реакции с электроактивным веществом и на участке ¬— наблюдаетс€ линейный рост так называемого фарадеевского тока пропорционально градиенту концентрации:
|
|
|
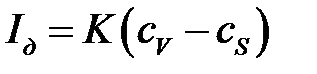 , (4.5)
, (4.5)
где сV и сS Ц концентрации электроактивного вещества в объеме раствора и в приэлектродном слое, соответственно; Ц коэффициент пропорциональности.
»ногда на пол€рограмме по€вл€ютс€ максимумы, обусловленные движением упавшей в раствор капли ртути. »х устран€ют добавлением в €чейку поверхностно-активных веществ (стол€рный клей и др.). ѕомехи от растворенного в воде кислорода устран€ют предварительной реакцией с восстановителем, обычно используют добавление Na2SO3.
Ќа участке CD рост тока практически прекращаетс€, так как скорость диффузии ионов в приэлектродный слой значительно меньше скорости разр€жени€ их на рабочем электроде, поэтому концентраци€ ионов электроактивного вещества в приэлектродном слое стновитс€ близкой к нулю (сS ≈0) и наступает состо€ние так называемой концентрационной пол€ризации. ѕри этом диффузионный ток достигает своего максимального (предельного) значени€ и так как сS ≈0, то уравнение (4.5) принимает простой вид:
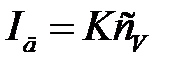 . (4.6)
. (4.6)
онстанта в уравнени€х (4.5) и (4.6) зависит от природы и характеристик рабочего микроэлектрода, на котором протекает электрохимическа€ реакци€. “ак, дл€ ртутного капающего электрода согласно уравнению »льковича
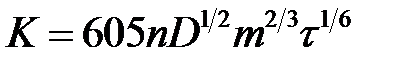 ,
,
где n Ц число электронов, участвующих в электродной реакции; D Ц коэффициент диффузии ионов, см2×сЦ1; m Ц масса капли ртути, вытекающей из капилл€ра за 1 с; τ Ц врем€ образовани€ капли ртути, с.
ƒл€ стационарного твердого электрода
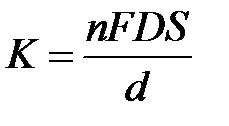 , (4.7)
, (4.7)
где n Ц число электронов, F Ц число ‘араде€, 96487 л×(моль×экв)Ц1; D Ц коэффициент диффузии, см2×сЦ1; S Ц площадь поверхности электрода, см2; d Ц толщина приэлектродного сло€, см.
”равнение (4.7) используетс€ при количественных определени€х в вольтамперометрии с применением стационарных твердых электродов.
¬ тех случа€х, когда самой медленной стадией процесса €вл€етс€ диффузи€, электродный процесс называют обратимым и получаема€ при этом пол€рограмма имеет более крутой линейный участок (рис. 4.8).
ќсобенностью пол€рограмм, получаемых с помощью твердых стационарных электродов, €вл€етс€ наличие максимумов так называемого броскового тока на вольтамперных кривых (рис. 4.9), что обычно св€зывают с замедленным формированием диффузионного сло€ у поверхности стационарного твердого электрода.
| I броск. |
| E |
| I |
| I стаб. |
–исунок 4.9 Ц ѕол€рограмма, полученна€ на твердом электроде: I броск. Ц Ђбросковыйї ток; I стаб. Ц стабильный ток
Ќа высоту максимума вли€ет скорость пол€ризации рабочего электрода. ”меньшение скорости наложени€ напр€жени€ на электроды приводит к снижению максимума и при некоторых значени€х скорости даже к полному исчезновению, но стабильный диффузионный ток остаетс€ неизменным.






