Сущность метода заключается в подсчете жизнеспособных микроорганизмов посевом на питательные среды, где микробные клетки в процессе деления образуют колонии видимые невооруженным глазом.
Метод стандартного подсчета колоний (СПК) предусматривает измельчение и гомогенизацию образца пищевых продуктов, его растворение в растворителе. Затем конкретное количество гомогената, разбавленного в растворителе высевают на агаровую среду (поверхностным или глубинным методами) и инкубируют при соответствующей температуре в течение определенного времени. Потом подсчитывают все видимые колонии с использованием счетчика колоний.
Этот метод наиболее широко используется для определения числа жизнеспособных клеток или колониеобразующих единиц (КОЕ) в пищевых продуктах. Количество жизнеспособных может быть рассмотрено как функция следующих факторов:
систематическая группа микробиоты продукта;
избранный метод исследования;
история пищевого продукта до проведения анализа;
состав плотных питательных сред относительно питательных веществ;
температура и время инкубации;
рН, влажностьи окислительно-восстановительный потенциал плотных питательных сред;
относительное количество микроорганизмов в образце;
наличие других конкурентных или антагонистических организмов.
СПК чаще всего осуществляется глубинным посевом, однако нельзя исключать использование поверхностного посева, потому что результаты обоих методов вполне сравнимы. При поверхностном посеве используются агаровые агаровые пластинки с твердой поверхностью. Растворенный методом серийных разведений образец в количестве 0,1, 0,5 или 1,0 мл наносятся на поверхность питательной среды. Затем с помощью согнутого стеклянного или пластикового шпателя («хоккейные клюшки») тщательно и равномерно распределяется по всей поверхности. При этом методе посева сохраняются чувствительные к высокой температуре психрофилы в пищевых продуктах, потому что микроорганизмы не попадают в контакт с горячим расплавленным мясопептонным агаром. Для строгих аэробов предпочтителен поверхностный посев, но микроаэрофильные организмы при таком посеве имеют тенденцию расти медленнее. При поверхностном посеве возникает проблема растирания, особенно когда поверхность агара влажная. Избежать это неудобство можно кратковременным подсушиванием агаризированной среды в боксе.
СПИРАЛЬНЫЙ ПЛОТТЕР
Метод спирального плоттера (спирального посева) – это метод учета жизнеспособных микроорганизмов. Спиральный плоттер – механическое устройство, которое распределяет жидкий гомогенат по поверхности вращающейся чашки Петри, содержащей соответствующий жидкий или плотный агар (рис.5.2.).

Рис.5.2. Спиральный плоттерEddy Jet 2
От центра пластины к ее краям, распределяя образец по архимедовой спирали, перемещается распределяющее устройство (рука), которое специальным прикрепленным шприцом отливает непрерывно уменьшающийся объем образца так, что концентрация в центре и у края достигает соотношения 10000:1. Инкубация посева в термостате показывает по количеству колоний на более высокую плотность внесенных клеток около центра пластины, с уменьшением к краю.
Подсчет колоний на пластине, подготовленной при помощи спирального плоттера, осуществляется при помощи специальной сетки подсчета (рис. 5.3. ). В зависимости от относительной плотности колоний, подсчитываются колонии, которые появляются в одной или более определенной областях этой сетки.
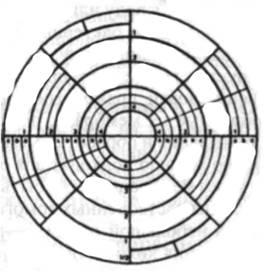
Рис.5.3. Сетка для подсчета колоний
Преимущества спирального плоттера: используется меньше агара; меньше чашек, растворителя и пипеток; и в три-четыре раза больше образцов может быть проанализировано в течение часа. Среди неудобств — проблема того, что частицы образца могут забивать распределитель. В силу этого прибор больше подходит для использования при анализе жидких пищевых продуктов типа молока. Для использования плоттера разработали лазерный счетчик. Из-за высокой стоимости устройства оно не будет применяться в лабораториях, которые не анализируют большое число чашек. Метод описан в работе Сousin, M.A., J.M. Jay, and P.C. Vasavada (2001).
Метод спирального посева образцов является широко распространенной в микробиологии техникой, которая была разработана для сокращения количества чашек Петри с питательной средой, используемых для поверхностных посевов. Метод спирального посева позволяет не выполнять серийные разбавления образца, которые необходимы при традиционном способе посева, и которые отнимают много времени. Один спиральный посев позволяет сэкономить 3 чашки питательной среды, что существенно сокращает время операции и расход материалов.
Спиральный посев образцов проводится по так называемой Архимедовой спирали. Объем пробы, нанесенный вдоль спирали экспоненциально уменьшается так, что один посев содержит несколько концентраций образца, распределенных вдоль спирали. После инкубации, результат учитывают с помощью специальной учетной сетки (вручную) или автоматически с помощью автоматического счетчика колоний Flash & Go.
В приборе Eddy Jet 2 (производитель IUL) реализован новый подход который заключается в использовании для нанесения материала образца стерилизованных γ-радиацией одноразовых микрошприцов, что предотвращает перекрестную контаминацию. Использование стерильных микрошприцев делает ненужными этапы очистки, что позволяет сэкономить большое количество времени.
МЕМБРАННЫЕ ФИЛЬТРЫ
Мембраны с размером пор около 0,45 мкм позволяют при фильтрации растворенной пробы задерживать бактерии, но пропускать воду или растворитель. После сбора на фильтре бактерий мембрану помещают на агаровую пластину или впитывающую подложку, насыщенную средой для культуры, и инкубируют. Затем производят подсчет колоний. Такие методы подходят для образцов, содержащих малое число бактерий.
Эффективность методов мембранных фильтров для определения количества бактерий микроскопированием была улучшена путем введения флуоресцентного окрашивания.
Одними из первых начали использоваться целлюлозные фильтры, однако разработанные позднее поликарбонатные нуклеопоровые фильтры обеспечивали сохранение всех бактерий на поверхности фильтра.
Техника прямого флуоресцентного фильтрования может рассматриваться как улучшенная модификация основного метода.
Растворенные гомогенаты пищевых продуктов фильтруются через 5-мкм нейлоновый фильтр, после чего фильтрат собирается и обрабатывается 2 мл тритона Х-100 и 0,5 мл трипсина. Эти реагенты используются для разложения соматических клеток и предотвращения засорения фильтров. После инкубации обработанные фильтраты пропускаются через нуклеопоровые поликарбонатные мембраны 0,6 мкм, которые затем окрашиваются акридиновым оранжевым красителем. После высушивания окрашенные клетки подсчитывают при помощи флуоресцентной микроскопии и число клеток на грамм рассчитывается умножением среднего числа в поле зрения на коэффициент увеличения микроскопа. Результат получают в течение 20-30 мин. Метод позволяет определять от 6 000 КОЕ/г в мясных и молочных продуктах.
5.4. МИКРОСКОПИЧЕСКИЙ ПОДСЧЕТ КОЛОНИЙ
Метод привлекается при подсчете микроколоний, которые развиваются в агаре, наслоенном на микроскопическое предметное стекло. На площадь 4 см2 предметного стекла распределяется 0,1 мл смеси молока и агара. После инкубирования, высушивания и окрашивания микроколонии подсчитывают с помощью микроскопа. В модефицированном методе 2 мл расплавленного агара смешивается с 2 мл подогретого молока и после смешивания 0,1 мл инокулированного агара распределяется на 4 см площади. Затем окрашенное тиониновым синим стекло просматривается под микроскопом.
Метод агаровых капелек предполагает растворение гомогената пищевого продукта в пробирке с расплавленным агаром (45 °С). При этом для каждого образца используется три пробирки.
В первую пробирку вносят 1 мл гомогената пищевого продукта и смешивают капиллярной пипеткой для перенесения на дно пустой чашки Петри 5-ти капель суспензии (по 0,1 мл)). Той же самой капиллярной пипеткой три капли (0,1 мл) из первой 9-мл пробирки переносят во вторую пробирку и затем перемешивают и помещают 5 капель по 0,1 мл на дно чашки Петри рядом с первыми каплями. Этот шаг повторяется для третьей пробирки агара. Чашки Петри, содержащие агаровые капельки, инкубируют в течение 24 ч, и колонии подсчитывают с помощью х10объектива. Для одного образца нужна только одна чашка Петри.
Петрифильмы. Петрифильмы – это тесты для количественного подсчета микроорганизмов в пищевых продуктах. На подложку тестовой системы наносится питательная среда для роста конкретного вида или группы микроорганизмов. В питательную среду включено специальное вещества, которое при добавлении жидкости превращается в гель при комнатной температуре. Среда для роста микроорганизмов образуется из имеющихся компонентов только в момент посева образца. До этого момента петрифильм не активен и может длительное время храниться. Для сохранения стерильности компоненты питательной среды покрыты сверху непроницаемой пленкой.
Метод п етрифильма - регидратированных сухих пленок- заключается в использовании двух пластиковых пленок, соединенных одной из сторон и покрытых ингредиентами культуральной среды и желирующим агентом холодного растворения, который носит коммерческое название Petrifilm. Метод может быть использован с неселективными ингредиентами для выполнения аэробного подсчета колоний (АПК), и с селективными ингредиентами для подсчета микроорганизмов определенной группы. Опыт использования этого метода показал, что он представляет приемлемую альтернативу методу СПК, который использует чашки Петри.
Для исследования 1 или 5мл жидкой суспензии образца помещается между двумя пленками и распределяется в область питания. После инкубации микроколонии выявляются в неселективной пленке в силу наличия тетразолидина в питательной среде. Помимо использования при аэробным подсчете колоний метод Petrifilm может использоваться для обнаружения и подсчета специфических групп, таких как колиформы и Е. coli.
5.5. НАИБОЛЕЕ ВЕРОЯТНЫЕ ЧИСЛА (НВЧ)
Образцы пищевых продуктов готовятся так же, как и для стандартного подсчета колоний. В 9 или 15 пробирок с соответствующей средой для метода с тремя или пятью сериями пробирок вносят три серии разведений. Численность микроорганизмов в исходном образце определяется с использованием стандартных таблиц наиболее вероятных чисел. Метод является по сути статистическим, и результаты метода наиболее вероятных чисел чаще всего выше, чем при методе стандартного подсчета колоний.
Этот метод анализа не отличается точностью; 95%-й доверительный интервал для экспериментов с тремя пробирками лежит в диапазоне от 21 до 395. При использовании теста с тремя пробирками 20 из 62 возможных комбинаций определяют 99% всех результатов, как и для теста с пятью пробирками. Этот метод анализа все же стал популярным.
Преимущества метода: простота; результаты лабораторий согласуются лучше, чем результаты стандартного подсчета колоний;
возможность определять специфические группы микроорганизмов при использовании соответствующих селективных или дифференциально-диагностических сред; приемлемость для определения плотности фекальных колиформ.
Его недостатки — затраты большого количества стеклянной посуды (особенно в случае пяти пробирок, повторностей), невозможность наблюдать морфологию колоний организмов, а также недостаток его точности.
ВОССТАНОВЛЕНИЕ КРАСИТЕЛЕЙ
В этом методе используются два красителя для того, чтобы установить количество жизнеспособных организмов в соответствующих продуктах: метилен голубой (синий) и резазурин. Подготовленный супернатант из пищевого продукта или жидкий продукт добавляют к стандартному раствору того или другого красителя и выдерживают до исчезновения синего цвета для метиленового синего; и до перехода от серо-голубого синего цвета к розовому или белому для резазурина. Время восстановления красителя обычно пропорционально числу микроорганизмов в образце.
Одна из проблем реакции восстановления красителя для некоторых пищевых продуктов – наличие в них собственных восстанавливающих агентов.
Тесты восстановления красителя давно используются в молочной промышленности для оценки микробиологического качества сырого молока. Преимущества состоят в том, что они просты, быстры и дешевы, а также в том, что красители обесцвечивают только жизнеспособные клетки. Недостатки в том, что не все организмы восстанавливают красители одинаково, а также в том, что метод нельзя применить к продуктам, которые содержат восстанавливающие ферменты, без использования специальной обработки.






