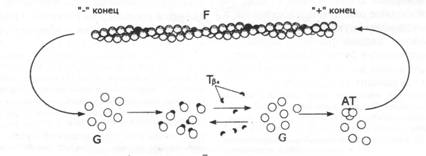
| называют ПЛЮС-КОНЦОМ, полимеризация идет с большей скоростью, чем на другом, минус-конце.
Это обусловлено тем, что на плюс-конце F-актина АТФ еще не гидролизован, а на минус-конце уже гидролизован. Взаимодействие Gактина- А ТФ происходит эффективнее с такой же молекулой, чем с Gактином- АДФ, благодаря чему один конец удлиняется быстрее другого в 4-6 раз.
Процесс полимеризации является динамичным и обратимым. Так, при высоких концентрациях свободного G-актина на плюс-конце за \ сек. присоединяется 70 протомеров и отсоединяются 2, а на минусконце, - соответственно, 20 и \. При снижении концентрации протомеров происходит сдвиг равновесия реакции в сторону диссоциации. В результате этого скорость элонгации снижается и наступает равновесное состояние - полимеризация на плюс-конце уравновешивается деполимеризацией на минус-конце.
В такой ситуации длина F-актина не увеличивается, хотя его состав fl обновляется. Дальнейшее уменьшение концентрации свободного F-актина приводит к тому, что деполимеризация на минус-конце идет быстрее, чем полимеризация на плюс-конце, те. F-актиновая нить укорачивается.
F-актин - структурная основа актиновых МФ, в состав которых входят и неактиновые актинсвязывающие белки (АС Б). Стабилизирующие АСБ представлены белками, которые укрепляют структуру F-актина,. Наиболее универсальным из них является тропомиозин, для которого известно несколько изоформ (а-, ~-, у-, 0- и Е-ТРОПОМИОЗИН). характерных для разного типа клеток.
Молекулы тропомиозина формируют тропомиозиновый тяж, локализованный в спиральных канавках Fактина и стабилизирующий структуру актиновой МФ (рис. 5а). Объединение молекул тропомиозина с Fактином и удлинение тропомиозинового тяжа осуществляется в ходе элонгации. В клетках имеется АСБ кофи лин, который, взаимодействуя с F-актином, блокирует его связывание с тропомиозином. С этой точки зрения, он является дестабилизирующим АСБ.
Тропомиозин - это фибрилпярный белок, состоящий из двух идентичных а-спиральных полипептидов, т.е. гомодимер. Молекула тропомиозина имеет \4 актинсвязывающих центров, благодаря чему взаимодействует с семью молекулами G-актина в составе F-актина, располагаясь в канавке его спирали. На концах молекул тропомиозина расположены центры тандемного (последовательного) взаимодействия друг с другом, т.е. ассоциации по принцилу «голова к хвосту».
Регуляторные АСБ контролируют процесс полимеризации F-актина. Одним из них является профилин, блокирующий стадию инициации. Регуляторные АС Б, функционирующие на этапе элонгации, можно подразделить на 2 группы: кзпирующие и режущие. В отличие от профилина, эти АСБ взаимодействуют не с G-актином, а с F-актином.
Кэпирующие белки в активном состоянии присоединяются к концам МФ и тем самым регулируют процесс элонгации (рис. 5ж).
Известен гетеродимерный белок, взаимодействующий с плюсконцом МФ, - кэп-белок, который останавливает процесс полимеризации на этом конце, т.е. рост МФ.
Обнаружена группа белков, кэпирующих минус-конец: акументин, ~актинин, спектрин и др., - и блокирующих полимеризацию (или деполимеризацию) на этом конце МФ. В зависимости от концентрации свободного С-актина, последствия действия таких белков могут быть разными: уменьшение, стабилизация или удлинение МФ. Таким образом, активируя или синтезируя те или иные кэпирующие белки, клетка способна тонко регулировать длину ахтиновых МФ.
|

 Почему я выбрал профессую экономиста
Почему я выбрал профессую экономиста
 Почему одни успешнее, чем другие
Почему одни успешнее, чем другие
 Периферийные устройства ЭВМ
Периферийные устройства ЭВМ
 Нейроглия (или проще глия, глиальные клетки)
Нейроглия (или проще глия, глиальные клетки)