Анестезин. Метод нитритометрии за счет наличия первичной ароматической аминогруппы в молекуле препарата. Индикатор- тропеолин ОО. Способ титрования – прямой.

Кстех.=1/1 = 1
Титрованный раствор натрия нитрита по ГФ ХI готовится с учетом РЧ.
f экв = Кстех= 1
Э = fэкв * М.м. =1 * М.м.= М.м.= 165,2 г/моль
Т= Э * М / 1000 = 165,2 * 0,1 / 1000 = 0,01652 г/мл
Предварительный расчет объема титранта на количественное определение:
V= a * Y = 0,3 * 5,0 = 3,49 мл 0,1 М раствора натрия нитрита
Т* Р 0,01652 * 26,0
Где а- навеска лекарственной формы в граммах; Y – количество анестезина по прописи в граммах; Т – титр анестезина по 0,1 М раствору натрия нитрита, г/мл; Р - масса лекарственной формы по прописи, гр.
Методика.
Навеска ЛФ – 0,3000 г
Практический объем титранта (Vопр) 3,5 мл К = 1,000
Расчет содержания (Х) в массе лекарственной формы (Р) проводят по формуле прямого титрования:
Х = Т* V* К * Vл.ф = 0,01652 * 3,5 * 1,000 * 26,0 = 5,011 г
а 0,3000
Расчет относительного отклонения.
Еоткл = (Г – Y) *100 = (5,011 – 5,0) * 100 = 0,2 %
Y 5,0
Приказ МЗ РФ № 751 н от 21.04.16 в таблице «Допустимые отклонения в массе навески отдельных лекарственных средств в жидких лекарственных формах при изготовлении методом по массе и в мазях» для прописанной массы 5,0 г составляет + 5%
Висмута нитрат основной. Метод комплексонометрии. При прибавлении индикатора ксиленолового оранжевого (индикатор добавляется в таком количестве, чтобы связать менее 1% ионов металла) к раствору висмута нитрата основного, образуется окрашенный в синий цвет комплекс ионов висмута с индикатором:
H6Ind + Bi3+ ® BiH3Ind + 3H+
желтый синий
При титровании раствором ЭДТА (Н2Y2-) образуется бесцветный комплекс иона висмута с ЭДТА, который более устойчивый, чем комплекс ионов металла с индикатором:

Далее идет разрушение комплекса ионов металла с индикатором, образование более устойчивого комплекса ионов металла с ЭДТА и выделение свободного индикатора:
BiH3Ind + Н2Y2- ® BiY- + H6Ind
синий желтый
В точке эквивалентности выделяется свободный индикатор, и наблюдается переход окраски из синей в желтую.
Кстех = 1/1=1
Титрованный раствор трилона Б по ГФ ХI готовится с учетом РЧ.
f экв = Кстех= 1
Э = fэкв * М.м. =1 * М.м.= М.м. = 233,01 г/моль
Т= Э * М / 1000 = 233,01 * 0,05 / 1000 = 0,01165 г/мл
Предварительный расчет объема титранта на количественное определение:
V= a * Y = 0,5 * 1,0 = 1,65 мл 0,05 М раствора трилона Б
Т* Р 0,01165 * 26,0
Где а- навеска лекарственной формы в граммах; Y – количество анестезина по прописи в граммах; Т – титр анестезина по 0,1 М раствору натрия нитрита, г/мл; Р - масса лекарственной формы по прописи, гр.
Методика.
Навеска ЛФ – 0,5000 г
Практический объем титранта (Vопр) 1,7 мл К = 1,000
Расчет содержания (Х) в массе лекарственной формы (Р) проводят по формуле прямого титрования:
Х = Т* V* К * Vл.ф = 0,01165 * 1,7 * 1,000 * 26,0 = 1,029 г
а 0,5000
Расчет относительного отклонения.
Еоткл = (Г – Y) *100 = (1,029 – 1,0) * 100 = 3 %
Y 1,0
Приказ МЗ РФ № 751 н от 21.04.16 в таблице «Допустимые отклонения в массе навески отдельных лекарственных средств в жидких лекарственных формах при изготовлении методом по массе и в мазях» для прописанной массы 1,0 г составляет + 7%
Заключение. Лекарственная форма удовлетворяет требованиям приказа № 751 н
Виды контроля: обязательные (письменный, органолептический, контроль при отпуске) и выборочные (физический, полный химический и опросный)
Хранят в защищенном от света месте не более 10 дней
Рибофлавина
Тиамина бромида по 0,005г
Кислоты аскорбиновой
Сахара по 0,1 г
Органолептический контроль. Однородный желтый порошок, без запаха.
Физический контроль.
М прописанная 0,21 г.
Норма отклонений (пр.№751 н) + 10%
Рассчитываем сколько грамм составляет 10% от 0,21 г.
0,21 г-----------100%
Х г ---------------10%
Х = 10 * 0,21 / 100 = 0,021 г
находим верхний предел 0,21 + 0,021 = 0,231 г
находим нижний предел 0,21 – 0,021 = 0,189 г
[0,189 – 0,231 ]
Подлинность.
Доказывают наличие кислоты аскорбиновой, рибофлавина, тиамина и сахара
Реакция на рибофлавин.
Окислительно-восстановительные свойства рибофлавина связаны с наличием сопряженной изоаллоксазиновой системы. Восстановление рибофлавина приводит к образованию бесцветного лейкорибофлавина, который, в свою очередь, может окисляться до характерно окрашенного рибофлавина:

Реакция на тиамин.
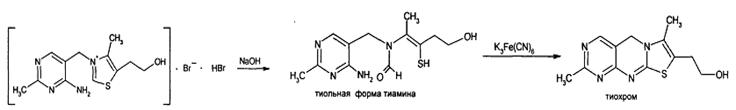
Реакция образование тиохрома. Сущность испытания заключается в постепенном окислении тиамина в щелочной среде (всего затрачивается три эквивалента щелочи) с образованием трициклического производного тиамина (тиохрома), способного давать синюю флуоресценцию в среде бутанола или изоамилового спирта при УФ – освещении: