У глобулярных белков почти все ионизируемые R-группы находятся на внешней поверхности молекулы, а большинство гидрофобных, или неполярных (не ионизируемых) групп, скрыто внутри глобулы. Кислотно-основные свойства нативных неповреждённых глобулярных белков в растворе определяются именно этими ионизируемыми группами.
Для белков, так же как для пептидов и аминокислот, характерны определённые изоэлектрические значения рН, при которых они ведут себя как цвиттерионы и в целом не несут электрического заряда. В электрическом поле при этих значениях рН белки остаются неподвижными. Такое значение рН будет изоэлектрической точкой белка (рΙ) и зависит оно от числа ионизируемых R-групп. Если в белке много основных групп, то рΙ будет высоким, больше 7, если в белке преимущественно кислые R-группы, то рΙ будет относительно низким.
Примеры рΙ для некоторых белков:
Пепсин <1 Гемоглобин 6,8
Яичный альбумин 4,6 Миоглобин 7,0
Сывороточный альбумин 4,9 Химотрипсиноген 9,5
Уреаза 5,0 Лизоцим 11,0
β-Лактоглобулин 5,2
На кислотно-основных свойствах белков основаны такие методы разделения смеси белков, как электрофорез и ионообменная хроматография.
Растворимость белков
Глобулярные белки различаются по своей растворимости в воде. Существенное влияние на растворимость оказывают рН, температура и свойства растворителя. Обычно растворимость белков минимальна при значении рН, которое совпадает с изоэлектрической точкой белка. В изоэлектрической точке молекулы белка не несут заряда, и между соседними молекулами отсутствует электростатическое отталкивание. Если рН станет больше или меньше рI у всех молекул белка будет заряд одного знака, поэтому они отталкиваются друг от друга и слипание их в крупные нерастворимые агрегаты становится невозможным.
Кроме того, растворимость белка зависит от образования гидратной оболочки вокруг гидрофильных групп белковых молекул. Такая оболочка возникают, если у белковой молекулы сформирована гидрофильная поверхность (рис. 5-33).

Рис. 5-33. Гидратная оболочка глобулярного белка
Высаливание белков
На растворимость глобулярных белков заметно влияют нейтральные соли (соли щелочных и щелочноземельных металлов и соли аммония). Высокие концентрации таких солей приводят к осаждению белков из водных растворов. Такое явление называется высаливанием. Наиболее эффективно высаливание в изоэлектрической точке белка.
Механизм высаливания заключается в том, что ионы растворённой соли притягивают диполи воды, уменьшая объём гидратной оболочки белка.


Рис. 5-34. Гидратирование ионов при растворении соли
 При определённой концентрации соли белковые молекулы утрачивают эту оболочку и, образуя крупные агрегаты, выпадают в осадок.
При определённой концентрации соли белковые молекулы утрачивают эту оболочку и, образуя крупные агрегаты, выпадают в осадок.
Важным является то, что осадок высоленного белка – это неповреждённые, нативные белковые молекулы. Удалив из осадка ионы соли с помощью диализа через полупроницаемую мембрану (рис. 5-35), можно опять растворить белок.
Рис. 5-35. Схема диализа через полупроницаемую мембрану
Денатурация белков
Денатурация белка – это такие изменения структуры молекулы, результатом которых будет осаждение белка из раствора и потеря им биологической активности. Под действием денатурирующих факторов в молекуле белка разрушаются нековалентные взаимодействия, которые формируют и поддерживают высшие уровни структуры (четвертичную, третичную и вторичную). Первичная структура денатурированного белка сохраняется.
Денатурацию вызывают различные химические и физические факторы. К ним относятся тепло, ультрафиолетовое излучение, органические растворители, мочевина, солянокислый гуанидин, кислоты, щёлочи и т.д.
Большинство белков денатурируют при нагревании растворов выше 50-60ºС, однако существуют и термоустойчивые белки, способные выдержать более сильное нагревание.
При непродолжительном действии и быстром устранении денатурирующего агента возможен обратный процесс – ренатурация белка с восстановлением исходной структуры и биологической активности (рис. 5-36). Ренатурацию можно наблюдать при действии на раствор белка мочевины, но при тепловой денатурации ренатурация белка невозможна.
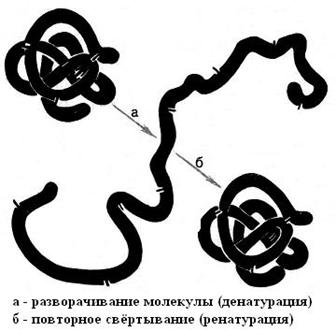
Рис. 5-36. Денатурация–ренатурация белковой глобулы
Методы разделения белков
При изучении смесей различных белков используют такие методы разделения как электрофорез в водном растворе или электрофорез в геле, ионообменную и аффинную хроматографии, гель-фильтрацию, разделение белков на основе различий в растворимости при разных концентрациях нейтральных солей.
После разделения белковых смесей и получения отдельных фракций различных белков, можно изучать их форму, молекулярную массу, пространственную организацию и другие их свойства.
Для обнаружения белка в растворе, а также для определения количества белка в различных биологических жидкостях и растворах белка неизвестной концентрации можно использовать цветные реакции на белок. Одна из широко применяемых цветных реакций, характерных для белков и пептидов, но не для свободных аминокислот, это биуретовая реакция. При обработке белка биуретовым реактивом (щелочной раствор CuSO4) образуется фиолетовое комплексное соединение Cu2+ и белка. Его количество можно определить с помощью спектрофотометра или колориметра.
· Основные биологические функции белков
1. Ферментативная – катализ всех химических реакций в живой клетке
2. Регуляторная – некоторые гормоны и рецепторы гормонов являются белками
3. Структуро-образовательная – участие в построении мембран клетки, тканей и органов
4. Защитная (иммунная)
5. Сократительная – участие в сокращении мышц
6. Специфические функции белков плазмы крови
ТЕСТОВЫЕ ЗАДАНИЯ
Выберите один или несколько правильных ответов
1. АМИНОКИСЛОТЫ ОБЯЗАТЕЛЬНО СОДЕРЖАТ
1) окси- и карбоксигруппы
2) амино- и карбоксигруппы
3) несколько спиртовых групп
4) амино- и амидную группу
2. В КЛАССИФИКАЦИИ АМИНОКИСЛОТ УЧИТЫВАЕТСЯ
1) отношение радикала к воде
2) отношение радикала к воде и его заряд
3) цикличность или ацикличность радикала
4) гетерофункциональность радикала
3. У БЕЛКОВЫХ АМИНОКИСЛОТ АМИНОГРУППА НАХОДИТСЯ ПО ОТНОШЕНИЮ К КАРБОКСИЛЬНОЙ ГРУППЕ
1) в α-положении
2) в β-положении
3) в γ-положении
4) в δ-положении
4. БЕЛКОВЫЕ АМИНОКИСЛОТЫ ИСПОЛЬЗУЮТСЯ ДЛЯ
а) образования гормонов
б) построения органов и тканей
в) синтеза белков
г) образования глюкозы и жиров
5. ПЕПТИДНАЯ СВЯЗЬ ОБРАЗУЕТСЯ ПРИ ВЗАИМОДЕЙСТВИИ
1) радикала с карбоксильной группой
2) радикала с аминогруппой
3) карбоксильной и амино групп
4) карбоксильной и спиртовой групп
6. В КРИСТАЛЛИЧЕСКОМ СОСТОЯНИИ АМИНОКИСЛОТЫ НАХОДЯТСЯ В ВИДЕ
1) аниона
2) катиона
3) биполярного иона
4) нейтральной молекулы
7. ГИДРОФИЛЬНЫМИ (ПОЛЯРНЫМИ) АМИНОКИСЛОТАМИ ЯВЛЯЮТСЯ
1) глутаминовая кислота
2) фенилаланин
3) аланин
4) серин
5) тирозин
8. БЕЛКИ ВЫПОЛНЯЮТ СЛЕДУЮЩИЕ ФУНКЦИИ
1) терморегуляция
2) регуляция процессов в организме
3) защита от механических повреждений
4) образование ферментов
9. ЛЕГЧЕ ВСЕГО РАЗРУШАЕТСЯ
1) первичная структура белка
2) вторичная структура белка
3) третичная структура белка
4) четвертичная структура белка
10. ПРИ ВЫСАЛИВАНИИ БЕЛОК ВЫПАДАЕТ В ОСАДОК, ПОТОМУ ЧТО
1) разрушается его конформация
2) нарушается гидрофильность поверхности молекул
3) теряется гидратная оболочка молекул
4) выходят к поверхности молекулы гидрофобные радикалы аминокислот
11. ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКА ФОРМИРУЕТСЯ, ЕСЛИ В ЕГО СОСТАВ ВХОДИТ
1) одна полипептидная цепь
2) две полипептидных цепи
3) несколько полипептидных цепей
4) пептидная цепь и небелковый лиганд
12. КАЖДАЯ МОЛЕКУЛА БЕЛКА ОБЛАДАЕТ
1) первичной структурой
2) первичной и вторичной структурой
3) третичной структурой
4) третичной и четвертичной структурой
13. ЗА СЧЁТ ПЕПТИДНОЙ СВЯЗИ ФОРМИРУЕТСЯ
1) вторичная структура белка
2) первичная структура белка
3) третичная структура белка
4) контакт с небелковым лигандом
14. ПРИ ДЕНАТУРАЦИИ БЕЛКОВ
1) разрушаются все структуры белка
2) сохраняется первичная структура белка
3) сохраняются биологические свойства белка
4) утрачиваются биологические свойства белка
15. К ДЕНАТУРИРУЮЩИМ АГЕНТАМ ОТНОСЯТСЯ
1) вода
2) высокая температура
3) кислоты и щёлочи
4) раствор поваренноё соли
ЗАДАЧИ И КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Смесь аминокислот, содержащую глицин, аланин, глутаминовую кислоту, лизин, аргинин и серин, разделяли методом элктрофореза на бумаге при рН 6,0. Укажите, какие из этих аминокислот будут двигаться а) к катоду, б) к аноду, в) останутся на линии старта?
2. Имеется смесь из пяти пептидов: а) Лиз-Гли-Ала-Гли
б) Лиз-Гли-Ала-Глу
в) Гис-Гли-Ала-Глу
г) Глу-Гли-Ала-Глу
д) Глн-Гли-Ала-Лиз
Укажите направление движения этих пептидов в процессе электрофореза на бумаге при рН 1,9; рН 3,0; рН 6,5 и рН 10,0
3. Сравните растворимость приведённых ниже пар пептидов при указанных условиях:
а) I – (Гли)20 или II – (Глу)20 при рН 7,0
б) I – (Лиз-Ала)3 или II – (Фен-Мет)3 при рН 7,0
в) I – (Ала-Сер-Гли)5 II – (Асн-Сер-Гис)5 при рН 9,0
г) I – (Ала-Асп-Гли)5 II – (Асн-Сер-Гис)5 при рН 3,0
4. Из токсина змей выделили трипептид, который состоял из трёх незаменимых аминокислот – серусодержащей, гетероциклической и гидроксилсодержащей. Напишите этот трипептид и определите его изоэлектрическую точку
5. Из нормальной мозговой ткани были выделены полипептиды, влияющие на передачу нервного импульса в определённых участках мозга. Они известны под названием «опиоиды». Используя приведённые ниже сведения, определите аминокислотную последовательность опиоида лей-энкефалина.
а) полный гидролиз пептида выявил наличие в нём Гли, Лей, Фен и Тир в молярном соотношении 2:1:1:1.
б) обработка пептида 2,4-динитрофторбензолом (реагент на свободную аминогруппу) выявила наличие динитрофторбензольного производного тирозина. Свободного тирозина не обнаружили
в) при частичном гидролизе пептида химотрипсином (фермент, расщепляющий пептидные связи с карбонильной группой лизина или аргинина) получили свободный лейцин, тирозин и более короткий пептид. Полный гидролиз этого короткого пептида выявил наличие глицина и фенилаланина в соотношении 2:1
г) после действия карбоксипептидазы (фермент, отщепляющий С-концевые аминокислоты) на короткий пептид обнаружили свободный глицин
6. Вычислите длину полипептидной цепи (в нм), содержащей 105 аминокислотных остатков, если вся цепь целиком представляет собой α-спираль
7. Сколько водородных связей должно быть разорвано, чтобы вывести из α-спиральной конфигурации только один аминокислотный остаток?
8. В белке цитохром С весовое содержание атомов Fe составляет 0,426 %. Вычислите минимальную молекулярную массу этого белка
9. По данным количественного аминокислотного анализа в сывороточном альбумине содержится 0,58% триптофана. Его молекулярная масса равна 204. Рассчитайте минимальную молекулярную массу альбумина
10. Укажите, в каком направлении будут двигаться в электрическом поле (к катоду, к аноду или останутся на старте) следующие белки: а) яичный альбумин при рН 5,0; б) β-лактоглобулин при рН 5,0 и 7,0; в) химотрипсиноген при рН 5,0, рН 9,5 и рН 11,0. Значения изоэлектрических точек соответствующих белков приведены на стр. 104
11. При каком значении рН можно наиболее эффективно разделить методом электрофореза следующие белковые смеси: а) сывороточный альбумин и гемоглобин; б) миоглобин и химотрипсиноген; в) яичный альбумин, сывороточный альбумин и уреаза?
12. Выберите из предложенных правильные утверждения:
а) Белки проявляют разнообразные химические свойства;
б) На свойства белков не влияют изменения рН и повышение температуры среды;
в) Белки содержат свободные аминогруппы, принадлежащие радикалу лизина, и свободные карбоксильные группы, принадлежащие радикалам аспарагиновой и глутаминовой кислот;
г) Специфические свойства аминокислот обусловлены наличием различных радикалов в них
13. Подберите правильное сочетание ключевых слов и смысловых фраз:
Ключевые слова:
а) Инсулин;
б) Кератин;
в) Ферритин;
г) Вирус табачной мозаики;
д) Рибонуклеаза
Смысловые предложения:
а) Белок, содержащий 20% железа и являющийся депо железа в организме животных;
б) Рибонуклеопротеин, содержащий 6% РНК;
в) Белок с гормональной активностью;
г) Фибриллярный белок волос;
д) Белок с ферментативной активностью
14. Подберите правильные сочетания ключевых слов и смысловых предложений:
Ключевые слова:
а) Ковалентные связи;
б) Ионные связи и гидрофобные взаимодействия;
в) Внутримолекулярные водородные связи;
г) Межмолекулярные водородные связи
Смысловые предложения:
а) Осуществляют связь между белковой и небелковой составляющими в липопротеиновых комплексах;
б) Обеспечивают соединение аминокислот в белковой молекуле;
в) Принимают участие в поддержании β-структуры в молекулах волокнистых белков;
г) Поддерживают α-спиральную конфигурацию полипептидной цепи
15. В рибонуклеазе весовое содержание лейцина и изолейцина 1,65% и 2,48%, соответственно. Рассчитайте минимальную молекулярную массу белка, предварительно определив молекулярную массу аминокислот по их формуле
16. Препарат церулоплазмина, медь-содержащего белка плазмы крови, содержит 0,29% меди. Молекулярный вес белка равен 151000. Сколько атомов меди находится в одной молекуле этого белка?
17. Вспомните, какие воздействия могут вызвать денатурацию белков? На какие связи в первую очередь действуют каждое из них?
18. В вопросах № 18, 19, 20, 21 и 22 выберите верное завершение для незаконченной фразы:
В процессе гидролиза белка: а) уменьшается количество свободных СООН-групп; б) увеличивается количество свободных аминогрупп; в) резко падает рН раствора; г) образуются пептидные связи; д) выделяется газообразный азот
19. В изоэлектрической точке белок: а) имеет наименьшую растворимость; б) обладает наибольшей степенью ионизации; в) является катионом; г) является анионом
20. При проведении электрофореза в условиях, когда рН буферного раствора выше, чем изоэлектрическая точка белка, он: а) мигрирует к катоду; б) мигрирует к аноду; в) остаётся на линии старта; г) образует биполярный ион
21. Молекулярная масса белков варьирует в пределах: а) от 1 до 500; б) от 500 до 1000; в) от 1000 до 5000; г) от 5000 до 100000; д) от 5000 до десятков миллионов
22. В формировании третичной структуры белковой молекулы участвуют перечисленные ниже связи за исключением: а) ионных связей; б) координационных; в) водородных связей; г) гидрофобных взаимодействий; д) ковалентных связей
Рекомендуемая литература
-Основная
1. Тюкавкина, Н. А. Биоорганическая химия: учебник / Н.А. Тюкавкина, Ю. И. Бауков, С.Э. Зурабян. – М.: ГЭОТАР-Медиа, 2012. – 416 с.: ил.
2.. Слесарев, В. И. Химия: Основы химии живого: учеб. для вузов / В.И. Слесарев. – СПб: Химиздат, 2007. – 784 с.: ил.
-Дополнительная
1 Сорочинская, Е. И., Биоорганическая химия: чеб. пособие / Е. И. Сорочинская, С. И. Чуркина. – СПб.: Изд-во С.-Петерб. ун-та, 2011. – 280 с.
Приложение 1
Основные единицы измерения, множители, приставки и
коэффициенты пересчёта в международной системе (СИ)
Величина






