Изучение конформации глобулярных белков с помощью рентгеноструктурного анализа показало, что она значительно сложнее конформации фибриллярных белков и не имеет пространственной ориентации.
Для описания трёхмерной структуры глобулярных белков пользуются понятием третичной структуры белка, под которой понимают компактное расположение полипептидной цепи в пространстве специфичное для каждого конкретного белка.
Первый белок, для которого выяснили третичную структуру, – это миоглобин мышц кашалота. Это небольшой белок с молекулярной массой 16700. Он содержит 153 аминокислотных остатков в одинарной полипептидной цепи, и гем, как небелковый лиганд. Изучал этот белок Дж. Кендрью с помощью рентгеноструктурного анализа.
Белок представляет собой клубок с восемью α-спиральными участками, разделённых между собой местами сгибов (рис. 5-22).
Сейчас изучена третичная структура нескольких сотен белков. Она зависит от ионной силы, рН, температуры раствора, в которой белок находится, и других показателей.
Третичную структуру стабилизируют в основном нековалентные взаимодействиями между функциональными группами радикалов аминокислотных остатков в полипептидной цепи (рис. 5-23). К ним относятся гидро-
|

Рис. 5-22. Глобула миоглобина
фобные, водородные, диполь-дипольные и электростатические связи. В местах изгибов цепи возникают ковалентные дисульфидные мостики между радикалами цистеина.

Рис. 5-23. Связи, стабилизирующие третичную структуру белков
Основной движущей силой в возникновении третичной структуры белков является взаимодействие радикалов аминокислот с молекулами воды. При этом гидрофобные радикалы погружаются внутрь возникающего клубка, образуя там сухие зоны, а полярные (гидрофильные) радикалы ориентируются наружу, в сторону воды. В результате возникает наиболее термодинамически выгодная конформация молекулы, обладающая минимальной свободной энергией.
Суммируя можно выделить следующие основные особенности третичной структуры миоглобина:
v молекула настолько компактна, что внутри помещается не больше 4 молекул воды;
v все полярные радикалы аминокислот расположены на внешней поверхности глобулы и гидратированы;
v почти все гидрофобные радикалы защищены от контакта с водой, так как расположены в глубине молекулы.
С помощью рентгеноструктурного анализа были исследованы и другие одноцепочечные белки и на рисунке 5-24 приведены модели их структур. На моделях видны отдельные спиральные участки, а также фрагменты с β-складчатой структурой.
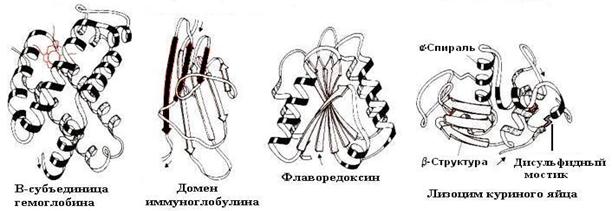
Рис. 5-24. Модели третичной структуры различных белков
4. Четвертичная структура белков – наиболее сложно организованная структура, характерная не для всех белков.
Большинство глобулярных белков с молекулярной массой больше 50000 Да представляют собой олигомерные структуры, т.е. они состоят из двух или более отдельных полипептидных цепей.
Для таких белков способ расположения в пространстве отдельных полипептидных цепей и формирование единого в структурном и функциональном отношении макромолекулярного образования (нативной конформации) называется четвертичной структурой.
Отдельные полипептидные цепи могут обладать одинаковой или разной первичной, вторичной и третичной структурами и называются протомерами или мономерами белковой молекулы. Сформированное ими образование называется мультимером или олигомером.
Протомеры соединяются друг с другом только нековалентными связями (аналогичными связям в третичной структуре). Каждый протомер в отдельности, как правило, не обладает биологической активностью, и она возникает только при определённом соединении мономеров. Число протомеров в белке чаще всего чётное (2, 4, 6, 8 или больше) (рис. 5-25).
|

Рис. 5-25. Модель белка-тетрамера
Одним из первых изученных белков с четвертичной структурой является гемоглобин. Он состоит из четырёх полипептидных цепей двух разных типов (α и β) и содержит 4 содержащих железо кофактора (гем) (рис. 5-26).
|

Рис. 5-26. Модель гемоглобина
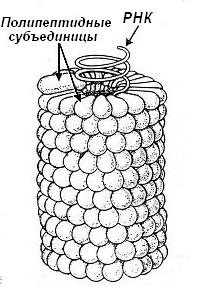
Молекулярная масса таких сложных белков может достигать 100000 Да, хотя есть и более сложные образования как например нуклеопротеиновый комплекс вируса табачной мозаики. Его молекулярная масса – 40 млн Да, количество белковых протомеров нанизанных на цепь РНК – 2130. Весь гигантский нуклеопротеиновый комплекс образуется спонтанно методом самосборки (рис. 5-27). Даже если с помощью специальных методов разъединить молекулу РНК и полипептидные протомеры, то они полностью восстановят исходную структуру при последующем их смешивании.
|
|

Рис. 5-27. Схема строения и процесса самосборки рибонуклеопротеинового комплекса вируса табачной мозаики
Нековалентные связи в олигомерной структуре образуются между контактными площадками отдельных мономеров, которые взаимодействуют друг с другом по принципу комплементарности. Формирование белков в виде сложных комплексов имеет ряд преимуществ:
v уменьшается вероятность ошибок при синтезе белка;
v экономится генетический материал, на основе которого идёт синтез;
v становятся возможными регуляторные взаимодействия, как в случае регуляторных ферментов.
· Физико-химические свойства белков
1. Молекулярная масса белков. Способы её определения
Молекулярная масса белков может очень сильно различаться от нескольких тысяч до сотен тысяч и даже миллионов. Например:
§ Цитохром с – 13000
§ Гормон роста человека – 21500
§ Пепсин – 35500
§ Фибриноген – 330000
§ Гемоцианин осьминога –2800000
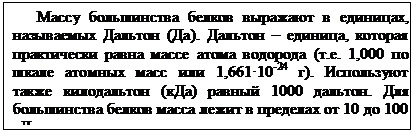

Молекулярная масса белка зависит от количества остатков аминокислот, образующих её молекулу. Для белков, у которых известен их аминокислотный состав, можно точно рассчитать молекулярную массу, но для большинства её определяют с помощью физико-химических методов.
Наиболее часто используют методы седиментационного анализа, гель-хроматографии и электрофореза.
а) Метод седиментационного анализа:
Седиментация – общий термин для обозначения движения в поле центробежной силы. С помощью седиментационного анализа можно получить данные о молекулярной массе (М), плотности и форме молекул.
В 1925 г. Сведберг изобрёл ультрацентрифугу, с помощью которой можно создавать центробежные ускорения в 250 тысяч раз превышающие ускорение земного притяжения (рис. 5-28). Частицы, находящиеся под действием центробежной силы, возникающей при вращении ротора, движутся вдоль действия этой силы с определённой скоростью.
В современных ультрацентрифугах скорость вращения ротора достигает 420000 g. Для поддержания таких скоростей в центрифугах создаётся вакуум и контролируется температура.

Рис. 5-28. Устройство ультрацентрифуги
Скорость осаждения (седиментации) частиц в центрифужной пробирке зависит от:
1. величины центробежной силы
2. размера, формы и плотности частиц
3. плотности и вязкости растворителя.
Выражают скорость седиментации через коэффициент седиментации s и измеряют его в единицах, называемых сведбергами (S). 1 S равен 1 · 10-13 сек.
Чем больше М частицы или молекулы, тем больше коэффициент седиментации s. Для белков коэффициент седиментации s лежит в пределах от 1 · 10-13 до 200 · 10-13. Если для частиц определён коэффициент седиментации, то можно рассчитать их молекулярную массу, используя уравнение:
 ,
,
где s – коэффициент седиментации, R – газовая постоянная, Т – абсолютная температура в кельвинах, D – коэффициент диффузии, ν – парциальный удельный объём растворённого вещества, ρ – плотность частиц. Все величины в этом уравнении можно определить экспериментально.






