К коллоидным поверхностно-активным веществам относятся такие ПАВ, которые в одном и том же растворителе могут находиться одновременно в виде молекул (ионов), образуя истинный гомогенный раствор, и в виде агрегатов молекул - мицелл, давая микрогетерогенную коллоидную систему. Между этими двумя фракциями устанавливается обратимое термодинамическое равновесие истинный раствор ↔ золь.
Растворы мицеллообразувщих ПАВ являются лиофильными коллоидными системами. Они являются также термодинамически равновесными ультрадисперсными системами.
Самопроизвольному образованию лиофильных дисперсных систем отвечает условие
ΔG = ΔH - TΔS <0 (2.1)
или
ΔH - TΔS < 0
Поскольку образуется гетерогенная система, поверхностная энергия должна быть скомпенсирована энтропийной составляющей, т.е. частицы дисперсной системы должны участвовать в молекулярно-кинетическом (тепловом) движении. Отсюда следует, что лиофильные системы могут быть только ультрадисперсными, а поверхностное натяжение на границе частица-среда должно быть очень мало.
Значение поверхностного натяжения, при котором обеспечивается термодинамическая устойчивость дисперсных систем, определяется соотношением Ребендера - Щукина:
σкрит ≤ γ KT / a2 (2.2)
где γ - безразмерный коэффициент;
K - константа Больцмана;
а - средний размер частиц.
Расчёты показывают, что межфазное поверхностное натяжение в лиофильных дисперсных системах в зависимости от размера частиц может иметь значения в пределах от 0,1 до 0,01 мДж/м2.
Опыт показывает, что такие низкие значения межфазного поверхностного натяжения на границе жидкость-жидкость в широком температурном и концентрационном интервале характерны для резко выраженной лиофильности молекул компонента, образующего дисперсную фазу.
Мицеллообразование в растворах коллоидных ПАВ является наиболее термодинамически выгодным процессом по сравнению с процессами образования истинного раствора или разделения фаз. Это обусловлено переходом углеводородной или полярной части дифильных молекул ПАВ в подобную им по полярности фазу. Например, полярные группы молекул ПАВ обращаются к воде, поскольку они гидратированы, а углеводородные радикалы выталкиваются из водной фазы.
Мицеллы характеризуются числом агрегации (числом молекул в мицелле) и мицеллярной массой (суммой молекулярных масс молекул ПАВ, входящих в мицеллу).
Мицеллообразование происходит при кооперативном связывании между собой углеводородных хвостов молекул ПАВ при концентрациях, превышающих узкую
 |
Рис. 2. Зависимость поверхностного натяжения (1), мутности (2), эквивалентной электропроводности (3), осмотического давления (4) от концентрации ПАВ в растворе. Выделена область мицеллообразования.
область, называемую критической концентрацией миделлообразования (ККМ).
ККМ - это концентрация ПАВ, при которой в его растворе возникает большое количество мицелл, находящихся в термодинамическом равновесии с его молекулами (ионами).
Методы определения ККМ основаны на регистрации резкого изменения физико-химических свойств растворов ПАВ в зависимости от концентрации (например, поверхностного натяжения, мутности, эквивалентной электропроводности, осмотического давления.(Рис. 2)
На кривой зависимости свойство-состав в области мицеллообразования обычно появляется излом. Одна из ветвей кривых (при более низких концентрациях) описывает свойства системы в молекулярном состоянии, а другая - в коллоидном. Абсциссу точки излома условно считают соответствующей переходу молекул в мицеллы, т.е. критической концентрации мицеллообразования.
Введение электролитов (индифферентных) снижает ККМ у ионогенных ПАВ и слабо влияет на ККМ неионогенных ПАВ.
Одним из основных характерных свойств мицеллярных растворов ПАВ является их солюбилизирующая способность, т.е. способность к коллоидному растворению практически нерастворимых в данной фазе веществ. Солюбилизацию следует рассматривать как своеобразное равновесное распределение солюбилизируемого вещества между макрофазой (дисперсионной средой) и коллоидной микрофазой (внутренней частью мицелл).
Для количественного определения солюбилизации используют рефрактометрический метод, основанный на том, что показатель преломления водного раствора ПАВ при добавлении солюбилизируемого вещества непрерывно возрастает вплоть до равновесного насыщения раствора солюбилизатом, а затем становится постоянным. Солюбилизирующую способность выражают в мл на 100 мл раствора ПАВ.
Солюбилизацию жидкостей вычисляют по правилу аддитивности для удельной рефракции.
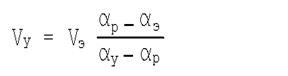 |
Vэ – объём водного раствора ПАВ до солюбилизации.
Vy – объём углеводорода, солюбилизированного водным раствором ПАВ.
αр,αэ,αy – коэффициенты рефракции раствора ПАВ до солюбилизации углеводорода, раствора ПАВ после солюбилизации и углеводорода соответственно.
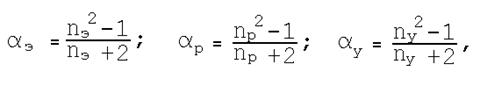 |
где nЭ, nр, ny – коэффициенты преломления раствора ПАВ до и после солюбилизации и углеводорода.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ.
1. Рассчитайте критическое значение межфазного натяжения, определяемого критерием Ребиндера, ниже которого происходит самопроизвольное диспергирование. Температура 20°С, размер образующихся частиц 10-6 см, логарифм отношения числа частиц дисперсной фазы к числу молекул дисперсионной среды равен γ = 15.
РЕШЕНИЕ Межфазное поверхностное натяжение, при котором происходит образование лиофильных дисперсных систем, вычисляется по соотношению Ребиндера-Щукина:
σкрит ≤ γ KT / a2 (2.2)

2. По данным кондуктометрического метода графически определите ККМ водного раствора лаурата натрия.
| Концентрация мыла С, кг/м3 | 2 | 3 | 5 | 10 | 20 | 30 |
|
| Удельная электропроводность, æ∙105, Ом-1∙м-1 | 0,5 | 0,77 | 1,27 | 1,67 | 2,43 | 3,2 |
 |
Рис. 3. Определение ККМ лаурата натрия
РЕШЕНИЕ. По табличным данным строим график в координатах указанных на рис. 3 и находим точку излома, соответствующую ККМ. Как следует из рис. 3, ККМ равна 5 кг/м3.






