Конденсацию и кристаллизацию можно осуществить по-разному: при постоянном давлении, при постоянном объеме.
Наиболее часто на практике встречается изобарный процесс; при конденсации и затвердевании чистого вещества его температура не изменяется, теплота qx выделяется за счет фазового перехода. Следовательно, в криогенном устройстве тепловые процессы подобны процессам термостатирования. Различие заключается в природе возникновения теплового потока, который возникает вследствие фазового перехода.
Ожижение криогенных газов
Ожижение газа при минимальном расходе энергии представлено на рис. 17.
 а)
а)
|  б)
б)
|
| Рис. 17. Идеальное ожижение газов: а) процесс ожижения газа в диаграмме Т− s; б) схема идеального цикла для ожижения газа (сплошные линии − рабочее вещество, штриховая линия − ожижаемый газ) | |
Пусть первоначальному состоянию газа на диаграмме Т − s соответствует точка 1 (рис. 17, а). Если газ сначала сжать в компрессоре при постоянной температуре, равной температуре окружающей среды Т 0, до очень высокого давления р 2(процесс 1−2), а затем расширить в детандере (процесс 2− f при s = const), то можно получить жидкость в состоянии, соответствующем точке 1. Если оба процесса обратимы, то минимально необходимая для ожижения газа работа определяется следующим образом:
 . (35)
. (35)
При изотермическом сжатии требуется затратить работу, которая рассчитывается по формуле:
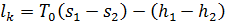 , (36)
, (36)
где h 1и h 2− энтальпия газа соответственно в начале и конце процесса сжатия.
При расширении газа в детандере производится работа:
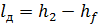 , (37)
, (37)
где  − энтальпия жидкости.
− энтальпия жидкости.
Таким образом,
 . (38)
. (38)
Процесс ожижения газа можно организовать иначе. Пусть ожижение газа происходит по наиболее естественному процессу − изобарному при р 1 = const. Тогда газ необходимо предварительно охладить от состояния 1 до состояния 3 (процесс 1-3), а затем сконденсировать (процесс 3- f). При охлаждении газа от него отнимается теплота  . Этому количеству теплоты на рис. 17, а эквивалентна площадь 1-3- b - c -1. При конденсации отводится теплота
. Этому количеству теплоты на рис. 17, а эквивалентна площадь 1-3- b - c -1. При конденсации отводится теплота  ;площадь f - a - b -3- f на рис. 17, а соответствует теплоте конденсации.
;площадь f - a - b -3- f на рис. 17, а соответствует теплоте конденсации.
Общее количество теплоты, отведенной от единицы массы газа при его ожижении в изобарном процессе 1-3- f составляет:
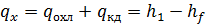 . (39)
. (39)
Вообразить осуществление этих обратимых процессов можно при помощи цикла, называемого идеальным циклом для ожижения газов. Представим себе установку, состоящую из компрессора К, детандера Д и теплообменника Т (рис. 17, б). Рабочее вещество (криоагент) сжимается в компрессоре при постоянной температуре Т 0 (процесс 1-2), расширяется в детандере при постоянной энтропии (s 2 = const) до состояния жидкости f и направляется в теплообменник Т, где вступает в тепловой контакт с ожижаемым газом (криопродуктом); причем во всех сечениях аппарата рабочее вещество и ожижаемый газ имеют одинаковые параметры состояния, но отделены один от другого теплопередающей поверхностью. Уравнение энергетического баланса:
 , (40)
, (40)
где 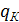 − теплота, отдаваемая в окружающую среду в процессе 1-2, ее можно определить по формуле (28) (см. стр. 32); qx − теплота, отбираемая криоагентом от ожижаемого газа в процессе 1 k -3 k - fk (параметры состояния в точках 1 k, 3 k и fk такие же, как в точках соответственно 1, 3, f).
− теплота, отдаваемая в окружающую среду в процессе 1-2, ее можно определить по формуле (28) (см. стр. 32); qx − теплота, отбираемая криоагентом от ожижаемого газа в процессе 1 k -3 k - fk (параметры состояния в точках 1 k, 3 k и fk такие же, как в точках соответственно 1, 3, f).
Теплота qx численно равна теплоте, отведенной от единицы массы газа при его ожижении, и может быть найдена по формуле (39). Она определяет полезную удельную холодопроизводительность цикла при переменном уровне температуры от Т 0до Tx. После подстановки соответствующих значений в выражение (40) получим:
 .
.
На диаграмме Т − s (рис.17, а) этой работе эквивалентна площадь 1−2− f −3−1.
Минимальная работа 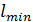 , затрачиваемая на ожижение 1 кг и 1 л различных газов, указана в табл. 1.
, затрачиваемая на ожижение 1 кг и 1 л различных газов, указана в табл. 1.
Для сравнения приведена примерная действительная работа ожижения некоторых газов.
Таблица 1
Минимальная 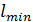 и приблизительная действительная l работа ожижения
и приблизительная действительная l работа ожижения
некоторых газов при р = 0,1013 МПа и Т 0 = 300 К
| Газ | i1−if, кДж/кг | lmin | l | ||
| (кВт×ч)/кг | (кВт×ч)/л | (кВт×ч)/кг | (кВт×ч)/л | ||
| Азот | 433,3 | 0,213 | 0,172 | 1,2¸1,8 | 1¸1,5 |
| Аргон | 273,1 | 0,134 | 0,186 | 0,8¸1 | 1,1¸1,4 |
| Водород | 3953 | 3,31 | 0,235 | 22¸42 | 1,5¸3,0 |
| Воздух | 428,3 | 0,205 | 0,179 | 1,2¸1,8 | 1¸1,5 |
| Гелий | 1563 | 1,9 | 0,237 | 16¸32 | 2¸4 |
| Кислород | 406,9 | 0,177 | 0,202 | 1¸1,5 | 1,2¸1,7 |
| Метан | 912,7 | 0,307 | 0,13 | 0,6¸1 | 0,25¸0,5 |
| Неон | 368,6 | 0,372 | 0,445 | 3,5¸5,5 | 3¸4,5 |
Разделение газовых смесей
Затраты работы при разделении газовой смеси на составные части зависят от применяемого способа. Однако и в этом случае существует минимальный теоретический предел затрат работы.
Состав разделяемой смеси обычно выражают через объемные, массовые или молярные доли.
Молярная доля компонента 1 в смеси определяется по формуле:
 (41)
(41)
где М1,…М n − количество молей компонентов в смеси.
Молярные доли компонентов в смеси связаны равенством:
 . (42)
. (42)
Рассмотрим процесс разделения идеальной газовой смеси. Примем бинарную смесь, состоящую из компонентов 1 и 2.
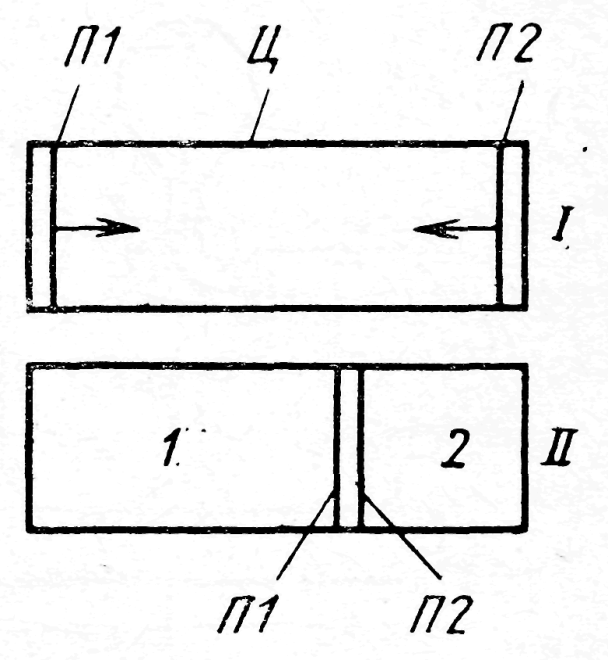
Рис. 18. Схема процесса разделения в цилиндре
с полупроницаемыми поршнями
Пусть в цилиндре Ц (рис. 18) (положение I ) при давлении p 0 и температуре Т 0содержится смесь в количестве М, включающая компонент 1 в количестве  и компонент 2 количестве
и компонент 2 количестве  (рис. 18). Парциальные давления этих газов в смеси можно определить по закону Дальтона:
(рис. 18). Парциальные давления этих газов в смеси можно определить по закону Дальтона:
В цилиндре расположены два полупроницаемых поршня, перемещающихся без трения, причем П1 проницаем для газа 1, а П2 − для газа 2.
Медленно перемещая поршни таким образом, чтобы давление и температура во всех частях системы не изменялись, достигнем положения II. Когда оба поршня сойдутся, тогда в левой части цилиндра соберется чистый компонент 1, давление которого будет р 0, а в правой − чистый компонент 2, давление которого также будет р 0. Таким образом, если процесс изотермичен, то затраты работы равны сумме работ изотермического сжатия составляющих газовых смесей от их парциальных давлений до общего давления р 0.
Если М = 1 моль, то
 . (43)
. (43)
Согласно закону Дальтона  , тогда
, тогда
 . (44)
. (44)
В качестве примера вычислим минимальную работу разделения воздуха на азот и кислород.
Ry = 8,314 Дж/(моль К); x кислород= 0,209; x азот = 0,791; Т = 303.
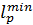 = − 8,314∙303 (0,209 ln0,209+0,791 ln0,791)=1291 Дж/моль.
= − 8,314∙303 (0,209 ln0,209+0,791 ln0,791)=1291 Дж/моль.
Реальные затраты работы существенно больше. Степень термодинамического совершенства установки разделения газовой смеси определяются по формуле:
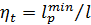 , (45)
, (45)
где l − суммарные затраты работы.
В воздухоразделительных установках часто приходится совмещать процессы разделения смесей и ожижения одного из получаемых продуктов. При определении минимальной работы для получения сжиженного кислорода и газообразного азота из воздуха процесс можно представить в виде двух последовательных процессов: разделение воздуха на газообразный азот и кислород и ожижение кислорода, тогда минимальная работа, отнесенная к одному молю определяется следующим образом:
 (46)
(46)
где  −минимальная работа ожижения воздуха.
−минимальная работа ожижения воздуха.
При разделении воздуха (при р 0 = 0,1 МПа) на азот и кислород и получении из него жидких кислорода или азота для определения минимальной работы l т i п можно использовать данные, приведенные в табл. 2.
Таблица 2
Минимальная работа, кДж/моль, получения 1-го моля жидких кислорода и азота из воздуха при полном его разделении на чистые О2 и N2
(начальная температура Т 0 = 303 К, воздух принят за бинарную смесь О2 − N2)
| Продукт | ( ) i
(разделение воздуха)
кДж/моль ) i
(разделение воздуха)
кДж/моль
|  (ожижение продукта)
кДж/моль
(ожижение продукта)
кДж/моль
|  (получение жидкого продукта из воздуха)
(получение жидкого продукта из воздуха)
|
| Кислород | 6,18 | 20,74 | 26,92 |
| Азот | 1,63 | 22,12 | 23,75 |
Контрольные вопросы и задания:
1. В сосуде Дьюара находится жидкий азот при t ос =20 0С. Определите минимальную мощность криогенной системы для термостатирования 25 кг жидкого криоагента при атмосферном давлении, если теплоприток в сосуд Дьюара составляет 20 Вт/кг.
2. Определите, какое количество теплоты надо отвести от 10 кг воздуха, чтобы охладить его в изобарном процессе от 200 К до 120 К? Определите минимальную работу, которую надо затратить для того, чтобы обеспечить это охлаждение. tос=25 0С.
3. Ожижить воздух, находящийся при атмосферном давлении и температуре 290 К. Определите минимальную работу ожижения килограмма криоагента, количество теплоты, которое надо отвести от килограмма криоагента. Определите работу, которую необходимо затратить для ожижения того же количества воздуха в цикле Карно.
4. Определите минимальную работу разделения 1 моля воздуха для получения чистых кислорода и азота, при этом принять температуру Т0=300 К и давление смеси и продуктов разделения p0=0,1 МПа; считать воздух за бинарную смесь О2–N2; молярная доля N2 в воздухе ya=0,791.






