Органическая химия - химия соединений, содержащих атомы углерода (углерода); изучает соединения углерода - их состав, химические превращения.
Однако не все соединения углерода относят к органическим. Рассмотреные раньше оксиды углерода (СО, СО2), угольная кислота (Н2СО3), ее соли - карбонаты и гидрокарбонаты, карбиды металлов и некоторые другие соединения являются неорганическими веществами.
Кроме углерода в состав органических веществ чаще всего входят водород, кислород, азот, значительно реже - сера, фосфор, галогены и другие элементы. Эти элементы носят название элементы - органогены.
Основные положения теории химического строения органических веществ были высказаны А.М. Бутлеровым в 1861 г. и кратко могут быть сформулированы следующим образом:
1. Атомы в органических молекулах соединены между собой в определенном порядке химическими связями в соответствии с их валентностью. Этот порядок называется химическим строением. Углерод во всех органических соединениях четырехвалентен.
2. Химическое строение можно выразить структурной формулой, в которой химические связи между атомами изображаются черточками. Общее число черточек, отходящих от каждого атома, равно его валентности.
3. Физические и химические свойства веществ зависят не только от их качественного и количественного состава, но и от строения молекул. Например, составу С2Н6О соответствуют два вещества – этанол и диметиловый эфир:

этанол диметиловый эфир
Этанол - жидкость с температурой кипения 78,4 0С; обладает слабовыраженными кислотными свойствами и способен вступать в реакцию с металлическим натрием. Диметиловый эфир – это газ с температурой кипения23,7 0С, он проявляет свойства слабого основания за счет неподеленной электронной пары атома кислорода.
Вещества, описываемые одинаковой молекулярной формулой, но имеющие разное строение и, следовательно, разные физические и химические свойства, называются изомерами.
4. Атомы в молекуле оказывают друг на друга взаимное влияние. Свойства каждого атома зависят не только от его природы, но и от его окружения. Так, в молекуле уксусной кислоты СН3СООН атом водорода в группе СООН, обладая кислотными свойствами, может отщепляться в водном растворе в виде иона Н+, а атом водорода в группе СН3 прочно связан с атомом углерода и не обладает кислотными свойствами. (приложение 1)
Соединения углерода и их особенности. Причиной многообразия органических соединений является уникальность атомов углерода, то есть:
- достаточно высокая валентность - 4;
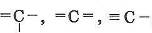
 - возможность образования простых, двойных и тройных ковалентных связей:
- возможность образования простых, двойных и тройных ковалентных связей:

- способность связываться друг с другом:

- возможность образования линейных
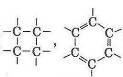
 - разветвленных
- разветвленных
- а также замкнутых цепей, которые называют циклами
Эти уникальные свойства углерода объясняются двумя факторами:
- наличием на внешнем уровне (2s и 2p) четырех электронов (поэтому атом углерода не способен терять и приобретать свободные электроны с образованием ионов)
- малый размер атома (по сравнению с другими элементами IV группы).
В результате углерод образует, главным образом, ковалентные связи, а не ионные, в органических соединениях он четырёхвалентен, то есть, соединен с четырьмя другими одновалентными атомами (атомы углерода могут соединяться с атомами различных элементов и друг с другом).
Состав и химическое строение органических соединений, то есть последовательность связей между атомами в молекуле, изображают химической формулой. Химические формулы бывают трех типов: общие (молекулярные), структурные и сокращенные структурные.
Общие или молекулярные, формулы отражают только количественный и качественный состав молекул вещества и не несут информацию о ее химическом строении, например: С2Н6О. Общие формулы используют только при количественном анализе органических соединений.
Структурные формулы полностью отражают химическое строение молекул вещества, то есть показывают последовательность связей между всеми атомами в молекуле, например:

Структурные формулы несут наиболее полную информацию о химическом строении соединения, однако, вследствие их объемности ими пользуются редко.
Сокращеные структурные формулы отражают связи между атомами углерода в молекуле вещества, за исключением связей с атомами водорода. Атомы водорода записывают у того атома, с которым они соединены, указывая их количество, например: СН3 – СН2 – ОН.
Для соединений циклического строения, а также соединений с большим количеством атомов углерода часто используют упрощенные формулы, в которых изображают только контур карбонового скелета в виде соответствующего цикла или ломаной линии, обозначая в нем только кратные связи, гетероатомы (атомы других элементов) и функциональные группы, например:




Бензол Метилбензол Аминофенол Пиридин
В начале изучения органической химии для записи сокращенных структурных формул соединений рекомендуется следующий порядок:
1) написать соответствующее количество атомов углерода и расставить связи между ними, например: С = С – С – С
2) написать, если есть функциональную группу у соответствующего атома углерода, например: С = С – С – С – ОН
3) написать атомы водорода у атомов углерода и указать их количество, учитывая, что атом углерода должен быть четырехвалентен (количество атомов водорода равна разнице между четырьмя и количеством связей, записанных у этого атома углерода), например: СН2 = СН – СН2 – СН2 – ОН
Изомерия и номенклатура органических соединений. Органические соединения могут иметь одинаковый качественный и количественный состав (одинаковую общую формулу), но отличаться химическим строением и, соответственно, свойствами. Такие соединения называются изомерами, а само явление - изомерией. Различия в строении изомеров могут быть обусловлены различными причинами. Поэтому различают разные виды изомерии:

Номенклатурой органических соединений называется правило, по которому даются названия органическим веществам.
Существуют несколько видов номенклатуры:
1) тривиальная;
2) рациональная;
3) систематическая.
Название органического соединения по систематической номенклатуре строится следующим образом:
1) выбирают и нумеруют самую длинную углеродную цепь;
2) указывают наличие и местоположение определенных функциональных групп;
3) указывают наличие и местоположение боковых углеводородных радикалов. Если радикалов несколько, то сначала называют меньшие радикалы, затем - большие (по номенклатуре IUРАС радикалы называют в алфавитном порядке). Если есть несколько одинаковых радикалов, то их называют один раз, указав их количество (два - ди, три - три, четыре - тетра) и локант для каждого из них;
4) указывают общее количество атомов углерода в самой длинной углеродной цепи;
5) указывают тип связи между атомами углерода в основной цепи и, если есть кратные связи, их количество и местоположение;
6) указывают наличие определенных функциональных групп и, если нужно, их количество и местоположение.
Запись формулы соединения, исходя из ее названия по систематической номенклатуре, начинают с записи самой длинной углеродной цепи и связей между атомами углерода в ней.






