РАБОТЫ:
ОПЫТ 1. Зависимость скорости реакции от концентрации
В пять пробирок налейте из бюретки 0,1 М раствор Na2S2O3, 1, 2, 3, 4, 5 мл и добавьте соответственно 4, 3, 2, 1, 0 мл воды (в сумме в одной пробирке 5 мл). В другие пять пробирок налейте по 5 мл 1 М раствор H2SO4. Вылейте в стакан 5 мл H2SO4 и прилейте Na2S2O3 из одной пробирки. Отсчитайте время в секундах от момента сливания растворов до начала появления помутнения (выпадения серы). Такой опыт проделайте для всех пяти растворов Na2S2O3.
Таблица 4
| № пробирки | 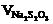 , мл , мл
| 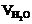 , мл , мл
| 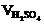 , мл , мл
| Время τ, с | Относит. скорость, 1/τ, с-1 |
| 1 | 1 | 4 | 5 | ||
| 2 | 2 | 3 | 5 | ||
| 3 | 3 | 2 | 5 | ||
| 4 | 4 | 1 | 5 | ||
| 5 | 5 | 0 | 5 |
ВЫВОДЫ:
1. На основании полученных результатов постройте график зависимости условной скорости реакции от концентрации.
2. Сделайте вывод о порядке исследуемой реакции в целом; запишите суммарные уравнения реакции и ее стадии; покажите, какой стадией определяется скорость суммарного процесса.
3. Сделайте вывод о результате, полученном на практике.
ОПЫТ 2. Зависимость скорости реакции от температуры
В две пробирки налейте по 5 мл 0,1 М раствора Na2S2O3, в другие две пробирки – по 5 мл 1 М серной кислоты. Одну пару пробирок с H2SO4 и Na2S2O3 поместите в стакан с водой при температуре 30оС, другую пару пробирок – в стакан с водой при температуре 40оС на 10 минут. Слейте в пустой стаканчик пару пробирок с H2SO4 и Na2S2O3 и отсчитайте время до появления мути.
То же сделайте с другой парой. В этом опыте учтите результат предыдущего опыта при сливании 5 мл H2SO4 и 5 мл Na2S2O3 при комнатной температуре.
Таблица 5
| № пп | t, оС | Время помутнения τ, с | Относит. скорость 1/τ, с-1 |
| 1 | 20 | ||
| 2 | 30 | ||
| 3 | 40 |
ВЫВОДЫ:
1. Постройте график зависимости условной скорости от температуры.
2. Сделайте вывод о влиянии температуры на скорость.
3. Рассчитайте температурный коэффициент реакции по правилу Вант-Гоффа.
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1. Что называется скоростью химической реакции? Математическое выражение скорости гомогенных и гетерогенных реакций.
2. От каких факторов зависит скорость химических реакций?
3. Классификация сложных химических реакций.
4. Закон действующих масс.
5. Молекулярность реакции.
6. Порядок реакции.
7. Как влияет температура на скорость химической реакции? Правило Вант-Гоффа.
8. Теория активации, уравнение Аррениуса.
9. Определите молекулярность и порядок прямой и обратной реакций:
ВаСО3 к ↔ ВаО к + СО2 г.
10. Во сколько раз изменится скорость реакции разложения оксида серы (VI): 2SO3 г ↔ 2SO2 г + СО2 г при уменьшении объема в три раза?
ЛИТЕРАТУРА:
1. С. 396-405; 2. С. 57-58; 3. С. 101-115; 4. С. 59-60, 65-67; 5. С. 32-36; 6. С. 97-106.
РАБОТА 5. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Тема «Химическое равновесие» логически связана с изучением медико-биологических дисциплин: нормальной физиологии, пат.анатомии, эпидемиологии и др. Ее изучение необходимо для понимания сущности равновесных процессов метаболизма. Например, обмен О2 и СО2 между кровью и тканями – равновесные процессы, характеризующиеся определенными константами равновесия (Кр). Изменение парциального давления газов приводит к смещению химических равновесий метаболических процессов. Резкое смещение химических равновесий может вызвать смерть. Например, это может произойти, если больному эмфиземой легких ввести кислород с высокой скоростью.
Цель занятия:
Научиться применять закон действующих масс при расчете равновесных концентраций веществ по значениям констант равновесия обратимых химических реакций; определять направление смещения химического равновесия при изменении условий (С, Т, Р).
Задание:
Выполните три лабораторных опыта и составьте отчет по теме.






