2.3. ††††††SO42- + 8H+ + 6e ↔ S + 4H2O†††††††† †††††††††† ≈о = 0,36 ¬
HClO2 + 3H+ + 4e ↔ Cl- + 2H2O †††††††††† ≈о = 1,56 ¬
2.4. ††††††MnO4- + e ↔ MnO42-††††††††††††††††††††††††††††††††††††††† ≈о = 0,56 ¬
HIO + H+ + 2e ↔ I- + H2O††††††††††† ≈о = 0,99 ¬
2.5. ††††††NO3- + 3H+ + 2e ↔ HNO2 + H2O †††††††††† ≈о = 0,94 ¬
ClO3- + 6H+ + 6e ↔ Cl- + 3H2O††† †††††††††† ≈о = 1,45 ¬
2.6. ††††††HClO + H+ + 2e ↔ Cl- + H2O†††††††† †††††††††† ≈о = 1,5 ¬
CO2 + 2H+ + 2e ↔ HCOOH†††††††††††††††††††††††† ≈о = -0,2 ¬
2.7. ††††††N2 + 8H+ + 6e ↔ 2NH4+††††††††††††††††† †††††††††† ≈о = 0,26 ¬
HClO + H+ + 2e ↔ Cl- + H2O†††††† †††††††††† ≈о = 1,5 ¬
2.8. ††††††H3AsO4 + 2H+ + 2e ↔ HAsO2 + 2H2O††††††††† ≈о = 0,56 ¬
BrO3- + 6H+ + 6e ↔ Br- + 3H2O†† †††††††††† ≈о = 1,45 ¬
2.9. ††††††Fe3+ + e ↔ Fe2+††††††††††††††††††††††††††††††††† †††††††††† ≈о = 0,77 ¬
MnO4- + 4H+ + 3e ↔ MnO2 + 2H2O ≈о = 1,69 ¬
2.10. Bi2O3 + 6H+ + 6e ↔ 2Bi + 3H2O† †††††††††† ≈о = 0,37 ¬
NO3- + 4H+ + 3e ↔ NO + 2H2O††† †††††††††† ≈о = 0,96 ¬
2.11. MnO4- + 8H+ + 5e ↔ Mn2+ + 4H2O †††††††††† ≈о = 1,51 ¬
SO42- + 4H+ + 2e ↔ H2SO3 + H2O †††††††††† ≈о = 0,17 ¬
2.12. SO42- + 8H+ + 6e ↔ S + 4H2O†††††† †††††††††† ≈о = 0,36 ¬
HClO2 + 3H+ + 4e ↔ Cl- + 2H2O †††††††††† ≈о = 1,56 ¬
2.13. MnO4- + 2H2O + 3e ↔ MnO2 + 4OH-†††††††††††††††† ≈о = 0,6 ¬
HClO + H+ + 2e ↔ Cl- + H2O†††††† †††††††††† ≈о = 1,5 ¬
2.14. H¬rO + H+ + 2e ↔ Br- + H2O†††††† †††††††††† ≈о = 1,34 ¬
H2SO3 + 4H+ + 4e ↔ S + 3H2O††† †††††††††† ≈о = 0,45 ¬
2.15. 2HClO2 + 6H+ + 6e ↔ Cl2 + 4H2O †††††††††† ≈о = 1,63 ¬
Cr3+ + e ↔ Cr2+††††††††††††††††††††††††††††††† †††††††††† ≈о =-0,41 ¬
3. акой из приведенных окислителей следует вз€ть, чтобы осуществить превращение
Br2 → 2BrO-††††††††††††††††††††††††††††††††††† ≈о = 0,45 ¬
ќкислители: 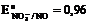 †¬; ††††††††††
†¬; ††††††††††  †¬;††††††††††
†¬;††††††††††
 †¬. —оставьте уравнение реакции.
†¬. —оставьте уравнение реакции.
4. ака€ из двух реакций возможна:
а) Br2 + KClO3 →?†††††††††††††††††††††††††  0,5 ¬
0,5 ¬
б) —12 + KBrO3 →?†††††††††††††††††††††††  1,47 ¬
1,47 ¬
—оставьте уравнение возможной реакции.
†††††††††† 5. Ќапишите уравнение реакции, подтверждающее восстановительные свойства Na2SO3. 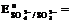 †-0,93 ¬.
†-0,93 ¬.
†††††††††† 6. акой из приведенных окислителей следует вз€ть дл€ перевода Mn2+ → MnO4- Eo = 1,51 ¬. ќкислители: K2Cr2O7, KNO3, K2S2O8. ќтвет мотивируйте. —оставьте уравнение реакции.
†††††††††† 7. —равните окислительную активность H2SO4 и H2SeO4, пользу€сь величинами потенциалов:
 †-0,93 ¬;
†-0,93 ¬;  †0,05 ¬. —оставьте уравнение реакции восстановлени€ селеновой кислоты металлическим скандием.
†0,05 ¬. —оставьте уравнение реакции восстановлени€ селеновой кислоты металлическим скандием.  †
†
-2,086 ¬.
†††††††††† 8. ѕользу€сь таблицей стандартных окислительно-восстано-вительных потенциалов, расположите галогены в пор€дке убывани€ их окислительной способности.
†††††††††† 9. акие из указанных реакций могут протекать самопроизвольно в стандарном состо€нии:
а) Fe2+ + I2 →††††††††††††††††††††††††††††††††† г) Fe3+ + Br- →
|
|
|
б) Fe2+ + Br2 →††††††††††††††††††††††††††††††† д) Fe2+ + Cl2 →
в) Fe3+ + I- →†† †††††††††† †††††††††† е) Fe3+ + Cl- →
†††††††††† 10. ћассова€ дол€ метгемоглобина (в % к общему гемоглобину) измен€етс€ с возрастом следующим образом: у новорожденных 6,22 %, у детей 1-3 мес€цев 2,21 %, у детей 1-3 года 1,13 %, у детей 7-14 лет 1,08 %. ак измен€етс€ при этом редокс-потенциал системы метгемоглобин/гемоглобин? (“ = 310 ).
†††††††††† 11. Ќа каких свойствах (окислительных или восстановительных) основано применение следующих веществ в медицинской практике и санитарии: аскорбинова€ кислота; перманганат кали€; пероксид водорода; хлорна€ известь. ƒайте по€снени€. «апишите уравнени€ окислительно-восстановительных реакций. ƒокажите веро€тность их протекани€ при стандартных услови€х.
†††††††††† 12. ¬ составе препаратов, рекомендуемых дл€ лечени€ железодефицитной анемии, вход€т соли Fe2+, которые легко окисл€ютс€ даже на воздухе. ќпределите, может ли добавл€ема€ в состав лекарственных препаратов аскорбинова€ кислота преп€тствовать их окислению.
“≈ћј ’. ЁЋ≈ “–ќ’»ћ»я » ЁЋ≈ “–ќ’»ћ»„≈— »≈
ћ≈“ќƒџ »——Ћ≈ƒќ¬јЌ»я ¬ ћ≈ƒ»÷»Ќ≈ » —јЌ»“ј–»»
†††††††††† Ёлектрохими€ устанавливает механизмы процессов и €влений, протекающих на границе раздела фаз с участием зар€женных частиц, в том числе электрические €влени€ в живых организмах.
†††††††††† Ѕиологические жидкости и ткани организма обладают определенной электрической проводимостью, и ее измерение широко используют дл€ целей диагностики. ћетод получил название кондуктометри€. Ўирокое распространение получил также метод потенциометрии в клиническом анализе и практике санитарно-гигиенических исследований. — помощью потенциометрии возможно определение концентрации физиологически активных ионов (H3O+, K+, Na+, Ca2+, Cl-, I- и др.) в биологических жидкост€х и ткан€х. ѕри использовании ферментных электродов возможно определение глюкозы, мочевины, аминокислот и других метаболитов.
†††††††††† »зучение механизмов возникновени€ биопотенциалов позвол€ет разобратьс€ в закономерност€х биохимических процессов в организме, в частности, процессов биологического окислени€.
†††††††††† ћетод регистрации биопотенциалов используетс€ при исследовании де€тельности различных органов (электрокардиографи€, электроэнцефалографи€, электромиографи€, электрогастрографи€).
†††††††††† ѕотенциометрическое и кондуктометрическое титрование примен€ютс€ дл€ определени€ концентрации биологически активных и лекарственных веществ.
†††††††††† ѕо теме ’ студент должен знать пон€ти€: электропроводность, удельна€ и мол€рна€ электропроводность; закон ольрауша; механизм возникновени€ потенциалов; устройство и назначение электродов; уметь рассчитывать мол€рную электропроводность растворов, в т.ч. биологических жидкостей; по экспериментальным значени€м удельной электропроводности оценивать степень и константу ионизации электролитов; рассчитывать значени€ потенциалов и э.д.с. гальванического элемента; владеть сущностью электрохимических методов исследовани€; навыками работы на иономерах и кондуктометрах.
¬опросы дл€ подготовки
1. Ёлектродный потенциал, механизм возникновени€ и его расчет по уравнению Ќернста.
2. ќкислительно-восстановительный потенциал, механизм возникновени€, расчет по уравнению ѕетерса.
3. ћембранный и диффузионный потенциалы.
4. Ѕиопотенциалы. ѕотенциал поко€ и действи€.
|
|
|
5. Ёлектроды стандартные и индикаторные. —тандартные: водородный и хлорсеребр€ный. »ндикаторные: рЌ-электроды и ионселективные.
6. √альванические элементы.
7. ”дельна€ и мол€рна€ электропроводности.
8. «акон ольрауша.
9. Ќа чем основан метод кондуктометрии? ѕотенциометрии?
10. ѕрименение кондуктометрии и потенциометрии в медицине и санитарии.
“есты
1. ”кажите обозначение и единицы измерени€ удельного сопротивлени€ проводника:†††††
1.1. L, ќм-1 †††††††††††††† †††††††††††††††††††††††††† 1.2. c, ќм-1м-1
1.3. l, ќм-1×м2/моль †††††††††††††††††††††††††† 1.4. r, ќм× м
2. Ѕуквой lобозначаем:
2.1. электрическую проводимость;
2.2. мол€рную электрическую проводимость;
2.3. удельную электрическую проводимость;
2.4. удельное сопротивление.
3. Ёлектродный потенциал металла при “¹25∞— рассчитываетс€ по формуле:
3.1.  ;
;
3.2. 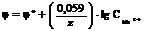 ;
;
3.3.  ;
;
3.4.  .
.
4. степень ионизации слабого электролита можно рассчитать по формуле:
4.1. 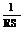 ;††††††††††††††††††††††††††††††††† †††††††††† 4.2.
;††††††††††††††††††††††††††††††††† †††††††††† 4.2.  ;
;
4.3.  ;††††††††††††††††††††††††††††††††† †††††††††† 4.4.
;††††††††††††††††††††††††††††††††† †††††††††† 4.4.  .
.
5. хлорсеребр€ным электродом €вл€етс€:
5.1. Ag½AgNO3;
5.2. Ag | AgCl ½ ЌCl0,1 моль/л ½стекл€нна€ мембрана | Ќ+;
5.3. Hg | Hg2Cl2 ½ KClнас;
5.4. Ag | AgCl ½ KClнас.
6. ¬ качестве индикаторных при измерении рЌ используют:
6.1. стекл€нный, водородный, сурьм€ный электроды;
6.2. хлорсеребр€ный, каломельный электроды;
6.3. стекл€нный, сурьм€ный, хлорсеребр€ный электроды;
6.4. водородный, каломельный электроды.
7. на границе раздела металл-раствор соли металла возникает:
7.1. редокс-потенциал;†††††††††††††††††††††† 7.2. электродный потенциал;
7.3. диффузионный потенциал;††††††† 7.4. мембранный потенциал.
8. Ёƒ— гальванического элемента, составленного из магниевого и цинкового электродов, при 25о—, (концентрации ионов Mg2+ и Zn2+ в растворе равны 0,1 моль ион/л) равна

8.1. -1,63¬;††††††††††††† †††††††††††††††††††††††††† 8.2. +1,63¬;
8.3. -3,11¬;††††††††††††† †††††††††††††††††††††††††† 8.4. +3,11¬.
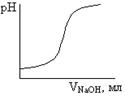
 9. рива€ кондуктометрического титровани€ раствора сол€ной кислоты раствором гидроксида натри€ имеет вид:
9. рива€ кондуктометрического титровани€ раствора сол€ной кислоты раствором гидроксида натри€ имеет вид:
 9.1.†††††††††††††††††††††††††††††††††††† ††††††† 9.2.
9.1.†††††††††††††††††††††††††††††††††††† ††††††† 9.2.

 9.3.
9.3.  †††††††††††††††††††††††††††††††††††††††† 9.4.
†††††††††††††††††††††††††††††††††††††††† 9.4.
10. ƒифференциальна€ крива€ потенциометрического титровани€ раствора Ќ—1 раствором NaOH имеет вид:
 10.1. †††††††††††††††††††††††††††††††††††††††††††††††† 10.2.
10.1. †††††††††††††††††††††††††††††††††††††††††††††††† 10.2.

 10.3.
10.3.  ††††††††††††††††††††††††††††††††††††† 10.4.
††††††††††††††††††††††††††††††††††††† 10.4.
«адачи и упражнени€
†††††††††† 1. онцентрации лактат- и пируват-ионов равны между собой, рЌ = 7, “ = 298 . ак изменитс€ редокс-потенциал при окислении 0,1 части лактат-ионов до пируват-ионов?
†††††††††† 2. –ассчитайте рЌ раствора, в который опущен хингидронный электрод, потенциал которого при 18о— равен 0,46 ¬. ≈охг = 0,699 ¬.
†††††††††† 3. ѕри какой концентрации ионов меди в растворе сульфата меди электродный потенциал медного электрода будет равен нулю? t = 25о—.  †+0,34 ¬.
†+0,34 ¬.
†††††††††† 4. –ассчитайте потенциал водородного электрода, опущенного в раствор, рЌ которого 7, t = 25о—.
†††††††††† 5. ¬ычислите при 25о— потенциал никелевого электрода, погруженного в 0,05ћ раствор NiSO4, счита€ диссоциацию соли полной.  †-0,23 ¬.
†-0,23 ¬.
†††††††††† 6. ¬ычислите при 18о— потенциал медного электрода, погруженного в 0,02ћ раствор CuSO4, счита€ диссоциацию соли полной.  †+0,34 ¬.
†+0,34 ¬.
7. Ёлемент состоит из водородного электрода, опущенного в кровь, и каломельного насыщенного электрода. ќпределите рЌ крови при 25о—, если Ёƒ— элемента равно 0,677 ¬. ≈окал = 0,246 ¬.
8. ќпределите концентрацию Ni(NO3)2, если Ёƒ— элемента, составленного из кобальта, опущенного в 0,1ћ Co(NO3)2, и никел€, опущенного в Ni(NO3)2, равна нулю при 25о—. α солей равна единице.
9. Ёлемент составлен из каломельного и хингидронного электродов, опущенных в исследуемый раствор. –ассчитайте рЌ раствора, если Ёƒ— при 25о— равна 0,278 ¬. ≈охг = 0,699 ¬; ≈кал.нас. = 0,246 ¬.
|
|
|
10. Ёлемент составлен из водородного и насыщенного хлорсеребр€ного электродов, опущенных в раствор. –ассчитайте рЌ раствора, если Ёƒ— при 25о— равна 0,56 ¬. ≈ох.с. нас. = 0,201 ¬.
11. ¬ычислите Ёƒ— концентрационного элемента, состо€щего из двух водородных электродов, погруженных в 0,01ћ и 0,05ћ растворы HNO3; t = 25oC;  1.
1.
12. —оставлена цепь из серебр€ного и кадмиевого электродов. онцентраци€ раствора азотнокислого серебра 0,1 моль/л, а нитрата кадми€ Ц 0,5 моль/л.  0,81;
0,81;  0,48. ¬ычислите Ёƒ— гальванического элемента при 25о—. ≈оAg+/Ag = 0,8 B; EoCd2+/Cd = -0,402 ¬.
0,48. ¬ычислите Ёƒ— гальванического элемента при 25о—. ≈оAg+/Ag = 0,8 B; EoCd2+/Cd = -0,402 ¬.
13. Ёƒ— гальванического элемента, составленного из водородного и насыщенного каломельного электродов, при 25о— равна 0,76 ¬. ¬ычислите рЌ раствора. ≈окал = 0,246 ¬.
14. ƒаны электроды: водородный, серебр€ный. «апишите электроды, составьте из них гальванический элемент, напишите реакции, идущие на электродах. «апишите выражение дл€ расчета Ёƒ—.
15. ак можно измерить рЌ исследуемого раствора, использу€ в качестве индикаторного электрода сурьм€ный? —оставьте гальванический элемент.
16. –ассчитайте рЌ 0,01ћ раствора —Ќ3—ќќЌ, если величина его удельной электропроводности при 25о— равна 1,56∙10-4 ќм-1∙см-1.
†††††††††† 17. ”дельна€ электрическа€ проводимость насыщенного раствора хлорида серебра при 298 равна 3,214∙10-4 ќм-1∙см-1, а воды, на которой он приготовлен, Ц 1,4∙10-4 ќм-1∙см-1. Ќайдете растворимость AgCl, моль/л и величину ѕ–AgCl.
18. †–ассчитайте удельную электрическую проводимость 0,16ћ раствора пропановой кислоты при 25о—.
“≈ћј ’I. ѕќ¬≈–’Ќќ—“Ќџ≈ я¬Ћ≈Ќ»я. јƒ—ќ–Ѕ÷»я
¬се биологические организмы представл€ют системы, которые содержат большое количество различных поверхностей раздела, отдел€ющих одну фазу от другой. “акими поверхност€ми €вл€ютс€, например, кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны, мембраны €дер, митохондрий, лизосом и т.д. Ќа большинстве этих поверхностей протекают различные процессы, которые имеют жизненно важное биологическое значение.
поверхностным €влени€м относ€т поверхностное нат€жение, адсорбцию, поверхностную активность, капилл€рные €влени€, смачивание и др.
ѕоверхностное нат€жение жидких фаз организма вли€ет на протекание биологических процессов. ƒоказано, что изменение поверхностного нат€жени€ на поверхности клеток и органелл играет важную роль в таких €влени€х, как деление клеток, амебоидное движение, изменение проницаемости клеточных мембран.
јдсорбци€ (отрицательна€ и положительна€) различных веществ в крови и в протоплазме клеток имеет большое значение дл€ обмена веществ. “ак, кислоты жирного р€да, стероиды накапливаютс€ у стенок сосудов, клеточных мембран, что облегчает их проникновение сквозь эти поверхности. явление адсорбции нашло практическое применение при выведении из организма €довитых веществ, аллергенов. “ак, при отравлени€х в медицинской практике примен€етс€ активированный уголь и другие энтеросорбенты, которые способны адсорбировать газы, алкалоиды, барбитураты, токсины из пищеварительной системы. ¬ санитарно-гигиенической практике €вление адсорбции используетс€, например, дл€ очистки питьевой и сточных вод.
†††††††††† ѕо теме ’I студент должен знать пон€ти€: поверхностна€ энерги€, поверхностное нат€жение; положительна€ и отрицательна€ адсорбци€; адсорбент, адсорбтив; термодинамические принципы адсорбции; классификацию веществ: ѕј¬, ѕ»ј¬, ѕЌ¬; виды и механизмы адсорбции на твердых адсорбентах; уметь оценивать природу адсорбтивов, адсорбентов и механизм адсорбции; анализировать факторы, вли€ющие на полноту адсорбции; владеть экспериментальными методами определени€ поверхностного нат€жени€; навыками определени€ краевого угла смачивани€.
|
|
|
¬опросы дл€ подготовки
1. –оль †поверхностных †€влений †в †организме †и †медицинской ††практике.
2. ѕоверхностна€ энерги€ √иббса. ѕричины ее возникновени€. Ёнерги€ поверхностного нат€жени€. ¬ли€ние температуры, природы жидкости и пограничной фазы, наличи€ примесей на величину энергии поверхностного нат€жени€.
3. ѕути снижени€ поверхностной энергии. јдсорбци€ (физическа€ и химическа€), адсорбент, адсорбтив. “ермодинамика адсорбции.
4. ѕоверхностно-активные и поверхностно-инактивные вещества. »зотерма поверхностного нат€жени€. ѕоверхностна€ активность. ѕравило ƒюкло-“раубе.
5. ћетоды измерени€ поверхностного нат€жени€. —талагмометри€, ее суть.
6. ѕоверхностно-активные вещества (ѕј¬). »оногенные и неионогенные. атион- и анионактивные ѕј¬. Ѕактерицидные свойства, применение в медицине и санитарии. Ћиофильные коллоидные растворы ѕј¬. ћицеллообразование в растворах ѕј¬. критическа€ концентраци€ мицеллообразовани€ (ккм), методы ее определени€. Ћипосомы. ћикрокапсулирование.
7. јдсорбци€ на границе раздела газ-жидкость. ”равнени€ √иббса. ѕоложительна€ и отрицательна€ адсорбци€. »зотермы поверхностного нат€жени€. —хемы адсорбции.
8. јдсорбци€ на границе раздела твердое тело-газ и твердое тело-жидкость. ‘акторы, вли€ющие на величину адсорбции. ”равнени€ Ћэнгмюра и ‘рейндлиха. »зотерма адсорбции. —хемы адсорбции. Ёнтеросорбенты. Ёфферентна€ медицина. ¬ыведение металлов-€дов и токсинов из организма.
9. †ћолекул€рна€ адсорбци€ из растворов на твердых адсорбентах. ѕравило –ебиндера.
10. »збирательна€ ионна€ адсорбци€. ѕравила ѕанета-‘а€нса.
11. »онообменна€ адсорбци€. »ониты. —тадии ионного обмена. ќбменна€ емкость. –егенераци€ ионитов.
12. огези€ и адгези€. јдгезив, субстрат. –абота когезии и адгезии. ”слови€ смачивани€, краевой угол смачивани€. Ѕондинговые системы в стоматологии.
“есты
1. ”кажите единицу измерени€ поверхностного нат€жени€ жидкости:
1.1. ƒж/м2;†††††††††††††††††††††††††††† †††††††††† 1.2. ƒж/моль;
1.3. Ќ/м2;††††††††††††††††††††††††††††††††††††††††††††††† 1.4. моль/м2.
2. ака€ из жидкостей, граничащих с воздухом, имеет наибольшее значение σ?
2.1. —2Ќ5ќЌ;†††††††††††††††††††††††††††††††††††††††† 2.2. Ќ2ќ;
2.3. раствор NaCl;†††††††††††††† †††††††††† 2.4. —4Ќ9ќЌ.
3. акое из веществ €вл€етс€ ѕј¬ по отношению к воде?
3.1. NaCl;†††††††††††††††††††††††††††††††††††††††††††††† 3.2. (NH4)2SO4;
3.3. KCl;††††††††††††††††††††††††††††††††††††††††††††††††† 3.4. мочева€ кислота.
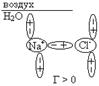
4. ака€ схема иллюстрирует адсорбцию ѕ»ј¬?

 4.1.†††††††††††††††††††††††††;†††††††††† 4.2. †††††††††††††††††††††††††††††††;
4.1.†††††††††††††††††††††††††;†††††††††† 4.2. †††††††††††††††††††††††††††††††;
4.3. ††††††††††††††††††††††††††††††††††††††††† †††††4.4.
 |  | ||
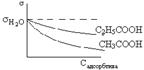
5. ака€ изотерма σ иллюстрирует правило ƒюкло-“раубе?

 5.1. ††††††††††††††††††††††††††††††††††††††††† ††††††5.2.
5.1. ††††††††††††††††††††††††††††††††††††††††† ††††††5.2.
 5.3. ††††††††††††††††††††††††††††††††††††††††† †††††5.4. ††††††††††††††††††††††††††††††††††
5.3. ††††††††††††††††††††††††††††††††††††††††† †††††5.4. ††††††††††††††††††††††††††††††††††
6. акое значение σ соответствует повышенному, по сравнению с нормой (57-68 Ёрг/см2), содержанию солей желчных кислот в моче?
6.1. 78;††††††††††††††††††† 6.2. 71;†††††††††††† 6.3. 63;†††††††††††† 6.4. 53.
7. ака€ схема иллюстрирует избирательную адсорбцию из водного раствора на поверхности BaSO4?

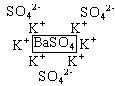 7.1. ††††††††††††††††††††††††††††††††††††††††† 7.2.
7.1. ††††††††††††††††††††††††††††††††††††††††† 7.2.

 7.3. ††††††††††††††††††††††††††††††††††††††††† 7.4.
7.3. ††††††††††††††††††††††††††††††††††††††††† 7.4.
8. ”кажите, в каких единицах не измер€етс€ адсорбци€ на твердом сорбенте:
8.1. ƒж/м2;†††††††††††††††††††††††††††† †††††††††† 8.2. моль/г;
8.3. моль/м2;††††††††††††††††††††††††††††††††††††††††† 8.4. г/м2.
9.  ”кажите пару Ђрастворитель + адсорбентї, необходимые дл€ полного разделени€ смеси дифильного () и пол€рного (о) веществ, исход€ из следующего услови€: растворитель раствор€ет оба вещества, а на твердом адсорбенте полностью адсорбируетс€ только одно из них:
”кажите пару Ђрастворитель + адсорбентї, необходимые дл€ полного разделени€ смеси дифильного () и пол€рного (о) веществ, исход€ из следующего услови€: растворитель раствор€ет оба вещества, а на твердом адсорбенте полностью адсорбируетс€ только одно из них:
| ќтвет | 9.1. | 9.2. | 9.3. | 9.4. |
   –астворитель –астворитель
| †† | | |||
| јдсорбент | уголь | уголь | мел | мел |
10. акой фактор €вл€етс€ одной из причин неполной адсорбции на поверхности твердого адсорбента?
10.1. сродство адсорбента и растворител€;
10.2. наличие активных центров на поверхности адсорбента;
10.3. сродство адсорбтива и адсорбента;
10.4. поверхностна€ энерги€ твердого адсорбента.
11. –абота адгезии дл€ жидких адгезивов рассчитываетс€ по формуле:
11.1. W = nFΔE;††††††††††††††††††† †††††††††† 11.2. W = 2σ;
11.3. W = (σт-г + σж-г) Ц σт-ж;††††††††††††††† 11.4. W = 2γ.
12. ”словие полного смачивани€ субстрата адгезивом:
|
|
|
12.1. ††Wc > Wa†††††††††††††††††††††† θ > 90o;
12.2. Wa > Wc†††††† †††††††††† θ > 90o;
12.3. Wa > ½Wc†††††††††††††††††† θ << 90o;
12.4. Wa < ½Wc†††††††††††††††††† θ >> 90o.
«адачи и упражнени€
1. ќцените природу следующих веществ: KNO3, BaCl2, пропанол, стеарат натри€. —равните поверхностное нат€жение водных растворов указанных веществ и воды.
2. –асположите в пор€дке уменьшени€ поверхностного нат€жени€ следующие вещества: толуол, гептиловую кислоту, уксусную кислоту, воду, бензол.
3. чистой воде добавили: а) серную кислоту; б) масл€ную кислоту. ак изменитс€ поверхностное нат€жение воды? ќпределите знак адсорбции.
4. —оставьте схемы адсорбции и исследуйте вли€ние природы сорбента и сорбтива на процессе адсорбции на угле и меле из водного раствора хлорида железа(Ў), метиленовой сини C16H18N+Cl- и эозина C20H8O5Br4.
5. –асположите ионы ¬а2+, +, Fe3+ в пор€дке уменьшени€ адсорбционной активности на пол€рном адсорбенте.
6. акие из перечисленных веществ будут поглощатьс€ на меле из водного раствора хлорида кальци€, нитрата натри€, муравьиной кислоты?
7. »сследуйте вли€ние природы растворител€ и адсорбента на процессе адсорбции на примере: адсорбент Ц мел, уголь; адсорбтив Ц краситель тимоловый синий (R-SO3H); растворитель Ц вода, —2Ќ5ќЌ.
8. –азделите водные растворы хлорида кальци€, масл€ной кислоты и хлорида натри€ на сорбентах: мел, уголь, катионит.
9. ¬о сколько раз способность к положительной адсорбции пропанола отличаетс€ от способности метанола? ћол€рные концентрации разбавленных водных растворов спиртов одинаковы.
10. »зобразите схему адсорбции на угле, когда имеет место конкуренци€ сорбтивов.
11. »зобразите схему адсорбции, соответствующую максимальной. акое правило вы используете при этом?
12. ѕриведите изотерму адсорбции этилового спирта, сделайте вывод о его поверхностной активности относительно воды. »зобразите положени€ молекул этилового спирта по отношению к поверхности воды. акой знак будет иметь адсорбци€?






