Значение темы:
Изучение темы будет способствовать формированию следующих компетенций ОК–1; ОК–5; ОПК-1; ОПК-7; ОПК-9; ПК-5
Цель занятия: после изучения темыстудент должен
Знать:
4. основные типы химических равновесий (протеолитические, гетерогенные, лигандообменные, окислительно-восстановительные) в процессах жизнедеятельности;
5. строение и химические свойства основных классов биологически важных органических соединений;
6. роль коллоидных поверхностно-активных веществ в усвоении и переносе малополярных веществ в живом организме, в процессах жизнедеятельности;
7. физико-химические методы анализа в медицине (титриметрический, электрохимический, хроматографический, вискозиметрический).
Уметь:
ü прогнозировать направление и результат физико-химических процессов и химических превращений биологически важных веществ;
ü пользоваться учебной, научной, научно-популярной литературой, сетью Интернет для профессиональной деятельности.
Форма организации учебного процесса: лабораторное занятие.
Место проведения занятия: учебно-научная химическая и биохимическая лаборатория.
Оснащение занятия: химическая посуда и реактивы, интерактивная доска, проекционное оборудование, инструкция по охране труда, справочная литература, средства индивидуальной защиты.
План проведения занятия:
| 1. | Организационная часть | 5 мин |
| 2. | Разбор тематического материала | 40 мин |
| 3. | Выполнение ситуационных задач | 60 мин |
| 4. | Выполнение и оформление лабораторной работы | 40 мин |
| 5. | Выполнение контрольной работы | 30 мин |
| 6. | Домашнее задание | 5 мин |
Вопросы для изучения темы:
1. Дисперсные системы. Классификация дисперсных систем.
2. Условия и методы получения коллоидных растворов. Особенности коллоидного состояния. Методы очистки коллоидных растворов. Диализ, электродиализ, ультрафильтрация. Принцип работы искусственной почки.
3. Строение коллоидной частицы. Мицелла, гранула, адсорбционный и диффузный слой.
4. Молекулярно-кинетические, оптические и электрокинетические свойства коллоидно-дисперсных систем.
5. Устойчивость и коагуляция коллоидных систем. Порог коагуляции. Явление коллоидной защиты и пептизации в медицине.
6. Коллоидные ПАВ. Мицеллообразование в растворах ПАВ. Липосомы, применение в медицине.
7. Классификация высокомолекулярных соединений. Химическое строение и пространственная форма молекул.
8. Особенности растворения ВМС. Термодинамика, механизм набухания и растворения ВМС. Зависимость степени набухания от различных факторов.
9. Влияние рН среды на набухание для амфотерных полиэлектролитов. Изоэлектрическое состояние макромолекул, изоэлектрическая точка, свойства амфотерных полиэлектролитов в изоэлектрическом состоянии.
10. Методы определения изоэлектрической точки белков. Электрофорез, сущность метода, практическое применение.
11. Вязкость растворов ВМС, уравнение Штаудингера. Вязкость крови и других биологических жидкостей. Вискозиметрия. Коллигативные свойства растворов ВМС. Уравнение Галлера.
12. Мембранное равновесие Доннана. Онкотическое давление плазмы и сыворотки крови.
13. Устойчивость растворов биополимеров. Застудневание, высаливание, коацервация растворов ВМС.
Вопросы для самоконтроля знаний:
1. Подберите соответствие между названием дисперсной системы и кратким обозначением:
| № | Название дисперсной системы | Краткое обозначение | |
| 1. | Эмульсия | А | ж/ж |
| 2. | Аэрозоль | Б | ж/г |
| 3. | Пена | В | г/ж |
| 4. | Золь | Г | т/ж |
| 5. | Суспензия | Д | г/г |
2. Назовите методы очистки коллоидных растворов от примесей:
А – растворенных низкомолекулярных частиц;
Б – грубодисперсных частиц.
3. Какой процесс изображен на рисунке? Приведите примеры использования процесса в медицине.

4. Раствор хлорида натрия или гидрозоля канифоли будет окрашен в красный цвет в проходящем свете?
5. Какой световой эффект изображен на фотографии? Чем он обусловлен?

Назовите фрагменты строения мицеллы, выделенные красным цветом:
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
{mAgJ nAg+ (n-x)NO3-}x+ xNO3- …………………….............................................
6. Какова зависимость порога коагуляции от заряда коагулирующего иона?
7. Подберите соответствие:
| № | Закономерности коагуляции смесями электролитов | Термин | |
| 1. | Усиление коагулирующего действия | А | Антагонизм |
| 2. | Суммирование коагулирующего действия | Б | Синергизм |
| 3. | Вычитание коагулирующего действия | В | Аддитивность |
8. Какие ионы электролитов гексацианофферата (II) калия или сульфата натрия являются коагулирующими для гидрозоля железа (III)?
9. Особенности растворения ВМС? Какой процесс называют набуханием?
10. Какие факторы и как влияют на набухание ВМС?
11. Как определяют степень набухания? Назовите основные этапы эксперимента.
12. Что называют изоэлектрической точкой белка?
13. Приведите схематическую формулу макромолекулы белка находящегося в изоэлектрическом состоянии.
14. Какие свойства белка резко меняются в изоэлектрическом состоянии?
15. Вставьте недостающие выражения: «Коллоидная защита – предохранение коллоидных растворов от …………. и, следовательно, повышение их …………….. добавлением небольших количеств высокомолекулярных веществ (белков, крахмала, агар-агара и др.), так называемых …………………..».
16. Какие процессы, характерные для белков, изображены на рисунке?

17. Перечислите факторы, вызывающие денатурацию белков.
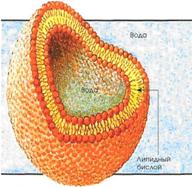
18. Что изображено на рисунке? Биологическая роль, практическое применение в биологии и медицине.
19. Результат, какого процесса исследования плазмы крови изображен на картинке?

Ситуационные задачи:
1. Напишите строение мицеллы сульфида меди, йодида серебра и карбоната кальция, если при электрофорезе они движутся к катоду. Определите заряд гранулы.
2. Расположите в ряд электролиты по увеличению порога коагуляции: фосфат натрия, тиоцианат калия, йодид цезия, сульфат натрия, хлорид натрия.
3. Изоэлектрическая точка миозина мышц равна 5. При каких значениях рН: 2; 4; 5 или 7 набухание будет наименьшим? С чем это связано?
4. При рН = 6 инсулин остается на старте при электрофорезе. К какому электроду инсулин будет перемещаться в растворе хлороводородной кислоты с концентрацией 0,1 моль/л?
5. К какому электроду будут передвигаться частицы белка (рI = 4,0) при электрофорезе в ацетатном буферном растворе, приготовленном из 100 мл раствора ацетата натрия с концентрацией 0,1 моль/л и 25 мл раствора уксусной кислоты с концентрацией 0,2 моль/л?
6. Будет ли происходить набухание желатина (рI = 4,7) в ацетатном буфере с равным содержанием компонентов при температуре 00C? Как можно интенсифицировать процесс набухания желатина?
7. Рассчитайте онкотическое давление раствора белка (относительная молекулярная масса 10000) с массовой долей 10% при температуре физиологической нормы.
Лабораторная работа № 7. «Свойства ВМС и их растворов».
Вопросы для контрольной работы:
1. Поверхностные явления и поверхностное натяжение жидкостей. Единицы измерения.
2. Поверхностно-активные, поверхностно-инактивные и поверхностно нейтральные вещества. Строение молекулы ПАВ. Изотерма поверхностного натяжения. Поверхностная активность. Правило Дюкло-Траубе. Применение ПАВ в медицине.
3. Строение мицелл Гартли и Мак-Бена. Явление солюбилизации.
4. Явление адсорбции. Понятие адсорбента и адсорбтива. Адсорбция на границе раздела жидкость – газ, жидкость – жидкость. Уравнение Гиббса. Изотерма адсорбции. Строение адсорбционного слоя. Особенности адсорбции на границе твердое тело-газ, твердое тело-жидкость. Уравнение Лэнгмюра.
5. Молекулярная адсорбция из растворов. Ионообменная адсорбция. Применение адсорбции в медицине (гемосорбция, иониты).
6. Дисперсные системы. Классификация дисперсных систем.
7. Условия и методы получения коллоидных растворов. Особенности коллоидного состояния.
8. Молекулярно-кинетические, оптические и электрокинетические свойства коллоидно-дисперсных систем.
9. Методы очистки коллоидных растворов. Диализ, электродиализ, ультрафильтрация. Принцип работы искусственной почки.
10. Строение коллоидной частицы. Мицелла, гранула, адсорбционный и диффузный слой. Устойчивость и коагуляция коллоидных систем. Порог коагуляции. Явление коллоидной защиты и пептизации в медицине.
11. Классификация высокомолекулярных соединений. Химическое строение и пространственная форма молекул.
12. Особенности растворения ВМС. Термодинамика, механизм набухания и растворения ВМС. Зависимость степени набухания от различных факторов. Влияние рН среды на набухание для амфотерных полиэлектролитов.
13. Изоэлектрическое состояние макромолекул, изоэлектрическая точка, свойства амфотерных полиэлектролитов в изоэлектрическом состоянии.
14. Методы определения изоэлектрической точки белков. Электрофорез, сущность метода, практическое применение.
15. Вязкость растворов ВМС, уравнение Штаудингера. Вязкость крови и других биологических жидкостей. Вискозиметрия.
16. Коллигативные свойства растворов ВМС. Уравнение Галлера. Мембранное равновесие Доннана. Онкотическое давление плазмы и сыворотки крови.
17. Устойчивость растворов биополимеров. Застудневание, высаливание, денатурация белков, коацервация растворов ВМС.
Примерные вопросы тестовых заданий к контрольной работе № 3:
Тестовые задания с выбором одного правильного ответа
1. Величина поверхностной энергии уменьшается при: а) увеличении поверхности; б) уменьшении поверхности; в) увеличении поверхностного натяжения; г) уменьшении поверхностного натяжения.
1) б, г
2) б, в
3) а, в
4) а, г
2. Из перечисленных веществ минимальным поверхностным натяжением обладает:
1) вода
2) муравьиная кислота
3) уксусная кислота
4) олеиновая кислота
3. Какую зависимость отражает изотерма адсорбции на подвижной поверхности раздела: а) величины адсорбции от равновесной концентрации вещества в интервале температур; б) величины адсорбции от температуры при постоянной концентрации вещества; в) величины адсорбции от равновесной концентрации вещества при постоянной температуре; г) величины адсорбции от начальной концентрации вещества при постоянной температуре?
1)а
2) б
3) в
4) г
4. Из полярных растворителей с ростом длины гидрофобного радикала величина адсорбции:
1) увеличивается
2) уменьшается
3) не меняется
4) одинакова
5. Ионы лучше адсорбируются на:
1) полярных адсорбентах
2) природа адсорбента значения не имеет
3) неполярных адсорбентах
6. Расположите спирты в порядке увеличения величины поверхностной активности: а) метанол; б) бутанол-1; в) этанол; г) пропанол-1.
1) а, в, г, б
2) б, г, в, а
3) а, б, г, в
4) б, в, г, а
7. К электрокинетическим свойствам дисперсных систем относят: а) электродиализ; б) электроосмос; в) электрофорез; г) эффект Тиндаля; д) опалесценцию.
1) а, б, в
2) б, в, г
3) б, в
4) а, б, д
8. В виде студня (геля) находятся: а) цитоплазма клетки; б) вещество мозга; в) глазное яблоко; г) цельная кровь; д) слюна.
1) а, в
2) б, в
3) а, б, в
4) в, г, д
9. Сгусток крови – это...
1) золь
2) гель
3) эмульсия
4) суспензия
10. Адсорбционный слой мицеллы составляют: а) потенциалопределяющие ионы; б) противоионы; в) молекулы электролита; г) молекулы неэлектролита.
1) а, б
2) б, в
3) в, г
4) а, в
11. Коагуляцию вызывают следующие факторы: а) температура; б) добавление электролита; в) ультразвук; г) механические воздействия.
1) а, б, г
2) б, в, г
3) а, б, в
4) а, б, в, г
12. Порог коагуляции – это: а) переход скрытой коагуляции в явную; б) переход явной коагуляции в скрытую; в) максимальное количество электролита, которое нужно добавить к 1 л золя, чтобы вызвать коагуляцию; г) минимальное количество электролита, которое нужно добавить к 1 л золя, чтобы вызвать явную коагуляцию.
1) а
2) а, в
3) г
4) б, в
5) б, г
13. Антагонизм – это:
1) суммирующее коагулирующее действие электролитов;
2) один электролит ослабляет действие другого;
3) один электролит усиливает действие другого;
4) взаимная коагуляция.
14. Растворы ВМС – это системы: а) гомогенные; б) гетерогенные; в) равновесные; г) образующиеся самопроизвольно; д) образующиеся не самопроизвольно, требуют стабилизатора.
1) а, в,д
2) а, в, г
3) б, в, г
4) б, г
5) а, г
15. Процессу растворения ВМС предшествует следующая стадия:
1) ограниченное набухание;
2) растворение происходит без набухания;
3) неограниченное набухание;
4) тиксотропное набухание.
16. Набухание, которое заканчивается растворением полимера называется:
1) неограниченным;
2) ограниченным;
3) тиксотропным.
17. Онкотические отеки возникают при: а) понижении концентрации белков в плазме; б) снижении онкотическго давления; в) повышении концентрации белков в крови; г) снижении концентрации электролитов.
1) а, б;
2) а, в, г;
3) а, б, в, г;
4) а, в.
18. В ИЭТ белки имеют заряд:
1) отрицательный;
2) положительный;
3) равный нулю.
19. К грубодисперсным системам относят: а) суспензии; б) эмульсии; в) пены; г) порошки; д) аэрозоли.
1) а, б, в;
2) а, в, г;
3) а, в, д;
4) все.
20. К эмульсиям относятся: а) молоко; б) сливки; в) сметана; г) сливочное масло.
1) а, б, в;
2) а, б, г;
3) б, в, г;
4) все.
Тема №13.
Зачетное занятие.
Значение темы: Проведение занятия направлено на контроль сформированности следующих компетенций
Форма организации учебного процесса: практическое занятие.
Место проведения занятия: учебно-научная химическая и биохимическая лаборатория.
Оснащение занятия: справочная литература.
План проведения занятия:
| 1. | Организационная часть | 5 мин |
| 2. | Подготовка к сдаче зачета | 145 мин |
| 3. | Выполнение заданий теста | 30 мин |
Вопросы, ситуационные задачи к зачету
Раздел 1. Строение вещества. Основы количественного анализа. Основные закономерности протекания химических процессов. Основные типы равновесий и процессов в жизнедеятельности. Химия биогенных элементов.
Тема №1. Введение в практикум. Основные законы химии. Классификация и номенклатура неорганических соединений. Способы выражения концентрации растворов. Основы количественного анализа.
1. Техника безопасности и правила работы в химической лаборатории. Меры оказания первой помощи и правила поведения при несчастных случаях.
2. Предмет и задачи химии. Место химии в системе естественных наук Связь химии с медициной. Основные этапы развития химии. Вклад отечественных и зарубежных ученых в развитие химии.
3. Современные представления о природе электрона. Характеристика энергетического состояния электрона с использованием квантовых чисел. Квантово-механическая модель атома. Электронные и графические формулы для атомов и ионов.
4. Типы химических связей. Принцип образования ковалентной химической связи. Метод валентных связей. Природа σ- и π-связей. Понятие о гибридизации атомных орбиталей. Взаимосвязь типа гибридизации и структуры молекул. Межмолекулярные взаимодействия.
5. Определение понятий: эквивалент, фактор эквивалентности, количество вещества эквивалента, молярная масса эквивалента.
6. Способы выражения концентрации растворов: а) массовая доля; б) молярная концентрация; в) молярная концентрация эквивалента; г) молярная доля растворенного вещества; д) моляльная концентрация; е) титр вещества. Формулы перехода от одних способов выражения концентрации к другим. Закон эквивалентов.
7. Правила приготовления растворов различных концентраций. Виды мерной химической посуды и приемы работы с ними.
8. Задачи количественного анализа. Классификация методов количественного анализа.
9. Разновидность количественного анализа – титриметрический анализ Требования к реакциям, применяемым в титриметрическом анализе. Классификация титриметрического анализа по типу химической реакции (кислотно-основное, осадительное, окслительно-востановительное, комплексонометрическое); по типу титранта.
10. Основные понятия: титрант, титрование, точка эквивалентности, точка конца титрования. Способы проведения анализа (прямое, заместительное, обратное), приемы проведения анализа (отдельных навесок, аликвотных проб (пипетирования)).
11. Способы выражения концентрации титрованных растворов, способы их приготовления. Стандартные (установочные, исходные) вещества. Требования, предъявляемые к стандартным веществам.
12. Теоретические основы, сущность алкалиметрического, ацидиметрического, перманганатометрического, йодометрического титрования. Используемые титранты, концентрация, способы их приготовления, стандартные вещества, способы фиксирования точки эквивалентности, индикаторы.
13.Индикаторы метода кислотно-основного титрования. Интервал перехода окраски индикаторов.
14.Оборудование в титриметрическом анализе. Правила работы с оборудованием.
15.Расчетные формулы, используемые в титриметрическом анализе согласно системе СИ.
16.Понятие о физико-химических методах анализа.
17.Сколько мл раствора серной кислоты с массовой долей 98% (r = 1,84 г/мл) необходимо взять для приготовления 200 мл раствора с массовой долей 10% (r = 1,05 г/мл)?
18. Вычислите массовую долю и молярную концентрацию раствора глюкозы, содержащего 75 г вещества в 500 г воды.
19.Чему равна молярная концентрация 0,9% раствора хлорида натрия (r = 1,0 г/мл)?
20.Как приготовить 5% раствор глюкозы из 20% раствора?
21.Концентрация глюкозы в сыворотке крови равна 3,5 ммоль/л, выразите концентрацию в мг%.
22.Гидроперит (содержит перекись водорода и мочевину) применяют как антисептическое средство. Одна таблетка соответствует 15 мл 3% раствора перекиси водорода. Сколько таблеток необходимо растворить в 100 мл воды для получения 1% раствора?
23.Для лечения впервые выявленных больных деструктивным туберкулезом вводят внутривенно 10% раствор изониазида из расчета 15 мг/кг массы тела. Рассчитайте объем в мл 10% раствора изониазида (r = 1,0 г/мл), который необходимо ввести больному массой 75 кг.
24.Тактивин – лекарственный препарат полипептидной природы используется в медицинской практике как иммуномодулирующее средство. Форма выпуска: 0,01% раствор во флаконах по 1 мл. При офтальмогерпесе препарат назначают в виде подкожных инъекций по 0,010-0,025 мг один раз в сутки. Рассчитайте объемы 0,01% раствора тактивина, которые соответствуют суточной дозе препарата.
25.Ампициллин – полусинтетический антибиотик. Форма выпуска: таблетки и капсулы по 0,25 г. Суточная доза для детей составляет из расчета 100 мг/кг. Суточную дозу делят на 4-6 приемов. Рассчитайте, какую часть таблетки нужно дать ребенку массой 10 кг на один прием: а) при четырехкратном приеме; б) при шестикратном приеме препарата в сутки?
26.Для определения общей кислотности желудочного сока 5 мл сока оттитровали раствором щелочи с концентрацией 0,095 моль/л в присутствии фенолфталеина. На реакцию израсходовано 2,5 мл раствора щелочи. Рассчитайте кислотность анализируемого сока в моль/л.
27.Рассчитайте массу навески КMnO4, необходимую для приготовления: а) 1 л раствора KMnO4 с молярной концентрацией эквивалента 0,1 моль/л, б) 0,5 л раствора KМnO4 c молярной концентрацией эквивалента 0,05 моль/л для проведения работ по перманганатометрическому титрованию.
28. Для определения кальция в сыворотке крови его осаждают в виде СаС2О4, добавляя к 0,5 мл сыворотки оксалат аммония в избытке. Осадок отфильтровывают, промывают и растворяют в серной кислоте. Раствор титруют раствором KMnO4 c молярной концентрацией эквивалента 0,01 моль/л до неисчезающего розового окрашивания. Вычислите содержание кальция в миллимолях на 1 л сыворотки, если на титрование 0,5 мл сыворотки израсходовано 5 мл KMnO4.
29. Рассчитайте массовую долю (%) уксусной кислоты, если на 10 мл ее раствора израсходовано при титровании 20 мл 0,2 моль/л раствора гидроксида натрия.
30. На титрование 2,5 мл раствора щавелевой кислоты с концентрацией С(1/2Н2С2О4) = 0,1 моль/л израсходовано в среднем 27,5 мл раствора KMnO4. Рассчитайте С(1/5KMnO4), моль/л.






